
在眼科疾病治疗领域,基因治疗有着显著优势。首先,人眼具备免疫豁免特征,可以使得眼睛不对外来抗原如疾病或病毒载体产生强烈的免疫反应。并且针对眼科疾病已经定位的致病基因较多,这意味着基因治疗可选择的靶点也更多。
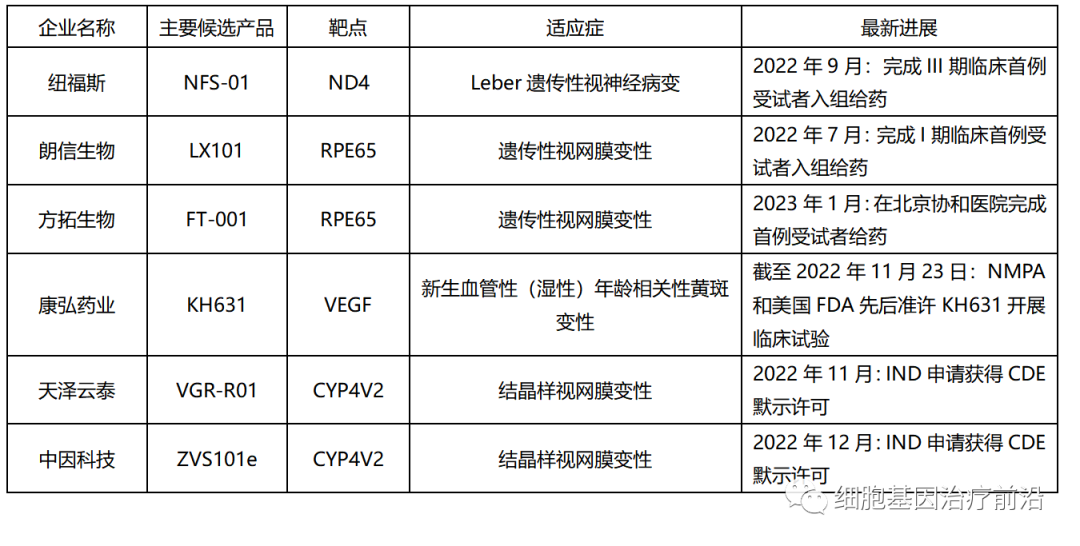
近几年,越来越多的国内药企布局眼科基因治疗这一赛道,其中,纽福斯、朗信生物、方拓生物等企业进展较快。
一、纽福斯
目前,纽福斯是国内走在眼科基因治疗领域前列的企业。其核心产品NFS-01(rAAV2-ND4, NR082),用于治疗ND4突变引起的Leber遗传性视神经病变(ND4-LHON)。2022年9月,NFS-01的III期临床试验在中国完成首例患者入组给药。
NFS-01各国研发现状(active)
截图来源:药融云全球药物研发数据库
NFS-01作用机制为采用基因治疗策略,以rAAV2作为载体,通过单次玻璃体内注射,将正确的基因通过玻璃体腔注射递送至患者受损的视神经节细胞,修复线粒体生物呼吸链,使视神经节细胞恢复活力与视功能。
2022年12月,纽福斯第二款眼科基因治疗药物NFS-02(rAAV2-ND1),用于治疗ND1突变引起的Leber遗传性视神经病变(ND1-LHON),获得了美国FDA的IND许可,并将在美国开展临床试验(《纽福斯:第二款眼科基因治疗药物获美国FDA临床试验许可》)。
纽福斯目前已建立丰富的眼科基因治疗产品管线,包含针对视神经损伤疾病、血管性视网膜病变等多种眼科疾病的10余个在研项目。
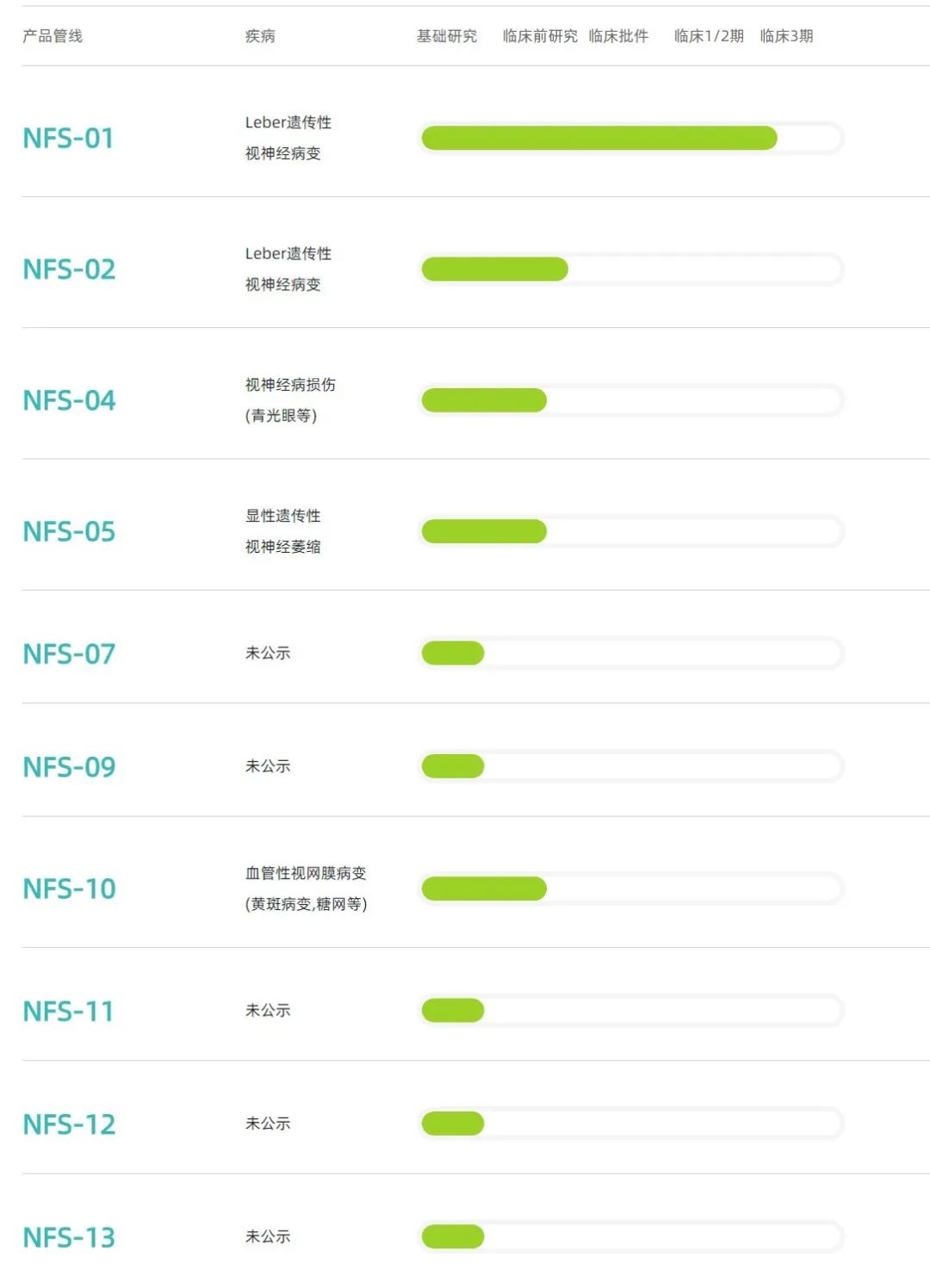
纽福斯研发管线(来源:官网)
二、朗信生物
朗信生物旗下上海朗昇生物科技有限公司自主研发的眼科基因治疗药物LX101注射液,旨在治疗RPE65双等位基因突变相关的遗传性视网膜变性(IRD)。2022年7月,LX101注射液I期临床研究在国家眼部疾病临床医学研究中心顺利完成首例患者入组及给药。
LX101通过AAV2携带正常RPE65基因,能特异识别并转染病变的视网膜色素上皮细胞,并在细胞内持续高效表达患者缺少的RPE65蛋白,恢复正常视循环,达到提升视功能的治疗目的。
据药融云数据库显示,上海朗昇生物向药审中心递交的LX101注射液新药临床申请于2022年1月16日被承办,4月20日批准临床(默示许可),总共用时84天。
LX101注射液审评时间轴
截图来源:药融云中国药品审评数据库
2022年12月,朗信生物旗下朗信启昇(苏州)生物制药有限公司的眼科基因治疗药物LX102注射液,用于治疗湿性老年性黄斑变性患者的临床试验申也请获得了CDE批准。
三、方拓生物
方拓生物的首款基因治疗产品FT-001注射液是一款针对RPE65双等位基因变异导致的遗传性视网膜变性的AAV眼科基因治疗药物。FT-001注射液已分别获得美国FDA和NMPA的临床试验许可。
2023年1月9日,FT-001注射液在北京协和医院完成首例受试者给药。该试验是一项单臂、开放标签、多中心的I/II期临床研究,旨在评价FT-001对RPE65双等位基因变异相关的视网膜变性受试者的安全性、耐受性和有效性。
2023年1月11日,方拓生物的第二款眼科基因治疗药物FT-003注射液,旨在治疗新生血管性年龄相关性黄斑变性(nAMD),在天津医科大学眼科医院顺利完成首例受试者给药。
方拓生物眼科研发管线
截图来源:药融云全球药物研发数据库
四、康弘药业
康弘药业的KH631眼用注射液是通过AAV递送目标基因用于治疗新生血管性(湿性)年龄相关性黄斑变性(nAMD),是具有自主知识产权的治疗用生物制品1类新药。
截至2022年11月,康弘药业子公司成都弘基生物科技有限公司先后收到NMPA和美国FDA的通知,准许KH631眼用注射液开展临床试验。其中在15日,弘基生物在中国总共有5条受理号获批。
KH631眼用注射液批准临床受理信息
截图来源:药融云中国药品审评数据库
五、天泽云泰
天泽云泰自主研发的VGR-R01注射剂是一款针对CYP4V2基因突变导致的结晶样视网膜变性(BCD)患者的眼科基因治疗药物。2022年11月,VGR-R01注射剂临床试验(IND)申请获得CDE默示许可(《天泽云泰:全球首个结晶样视网膜变性新药IND申请获受理》)。
VGR-R01通过视网膜下腔注射给药后,AAV衣壳蛋白介导RPE细胞的转导,将VGR-R01基因表达盒递送至细胞核。VGR-R01表达盒以游离DNA的形式存在,在RPE细胞表达CYP4V2蛋白,以重建细胞的脂肪酸羟化酶活性。
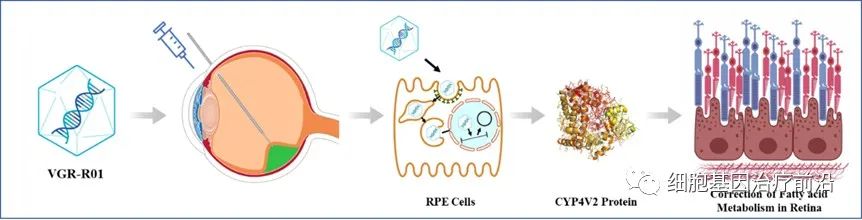
VGR-R01作用机制(来源:天泽云泰官网)
VGR-R01通过纠正患者视网膜内的脂肪酸代谢障碍,以期达到预防或改善RPE细胞、感光细胞及脉络膜的结构和/或功能损伤,并实现纠正视力损伤、保护残存视功能、或延缓视力恶化的临床效果。
天泽云泰于2020年3月成立于上海,致力于将前沿的基因及细胞治疗技术,转化为临床可及的治疗方法。
六、中因科技
中因科技/北京大学第三医院自主研发的ZVS101e注射液是一款治疗由CYP4V2基因突变所致的结晶样视网膜变性(BCD)患者的眼科基因治疗药物。2022年12月,ZVS101e注射液临床试验申请(IND)获得CDE默示许可。
ZVS101e所含治疗载体(rAAV8)对视网膜细胞有特殊嗜性,注射入患者视网膜下腔后,可高效感染视网膜的视网膜色素上皮(RPE)细胞,并在RPE细胞中特异性表达CYP4V2蛋白,弥补由于基因突变导致的蛋白功能缺失,从而对BCD患者的视网膜功能恢复起到有效治疗作用。
截图来源:药融云全球药物研发数据库
中因科技是一家专业从事遗传性眼病临床基因诊断和基因治疗药物研发的国家高新技术企业,是国内率先进行眼科基因治疗药物研发的企业。
总结
眼科疾病作为药企重点关注的领域,自2017年12月,第一款眼科基因治疗药物Luxturna获批上市,正式敲开了眼科基因治疗的大门。国内多家药企布局眼科基因治疗赛道,其中纽福斯一骑绝尘,是国内当前进度最快的企业。同时,多家药企获批临床,可以预计未来几年国内眼科基因治疗领域会出现新的突破。
信息参考:
[1] 各公司官网
[2] 鸿翊资本
[3] 药融云数据库
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、申报审批情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论