血液制品指各种人血浆蛋白制品,包括人血白蛋白、人免疫球蛋白、人凝血因子Ⅷ、人纤维蛋白原、抗人淋巴细胞免疫球蛋白等。人血浆中有92% - 93%是水,仅有7% - 8%是蛋白质,血液制品就是从这部分蛋白质分离提纯制成的。
说到血液制品,就不得不提澳大利亚的血液制品龙头CSL,作为一家领先的生物技术公司,致力于开发和提供创新的生物疗法和流感疫苗,专注于罕见病、严重疾病、疫苗等。业务涉及免疫缺陷、出血性疾病、遗传性血管性水肿、α1-抗胰蛋白酶缺乏症、神经系统疾病和流感疫苗等,治疗领域包括免疫学、血液学、心血管系统和代谢系统、呼吸系统和移植系统。

CSL拥有一百多年的历史。1916年,CSL的前身,即联邦血清实验室(The Commonwealth Serum Laboratories)成立,此后联邦血清实验室为澳大利亚提供了胰岛素、青霉素,以及流感疫苗、脊髓灰质炎疫苗和其它传染病疫苗等。1994年,原属联邦的CSL实现私有化,改名为CSL Limited,并于当年6月在澳大利亚证券交易所(ASX)上市。
1905年,历史上第一位诺贝尔生理医学奖获得者,德国医学家埃米尔·阿道夫·冯·贝林(Emil Adolf von Behring)博士在德国马尔堡附近创立Behring Werke。如今已是CSL Behring旗下全球最具规模的研究及生产基地之一。

Emil Adolf von Behring
图源:nobel prize
1981-2000年,CSL的4家前身公司完成了两两合并,其中CSL收购瑞士血浆蛋白生产商ZLB,并成立了ZLB Bioplasma;Armor和Behring Werk合并成为了Aventis Behring。这两家合并后的公司同时在2001年进行了大规模的浆站收购,其中CSL收购了Nabi血浆采集中心(美国)运营的47个血浆采集中心和实验室,成立了ZLB 血浆服务机构;Aventis Behring从Serologicals收购了42个血浆采集中心,组成世界上最大的血浆采集商业机构。
2004年CSL收购Aventis Behring并与ZLB Bioplasma重组后成立了CSL Behring,自此成为世界第一大血制品生产商。
对于原材料生产的上游和药物制造的中游高度整合的血液制品行业来说,规模意味着低成本和竞争力,产品线越丰富则利润率越高,如果能从同一批血浆中提取更多种产品就能够有效地摊薄成本。因此并购是血液制品企业扩大规模的最常用手段。
2014年,CSL宣布收购诺华(Novartis)旗下的全球流感疫苗业务部,并于2015年将该部门与CSL的子公司bio CSL合并,联合企业更名为Seqirus,成为全球第二大流感疫苗生产商;2017年CSL收购体外造血干细胞基因治疗公司Calimmune;2020年CSL收购从事IL-6单克隆抗体开发的Vitaeris。通过不断扩张,CSL奠定了自己在血液制品和流感疫苗方面的优势。
目前,CSL在全球拥有270多个血浆采集中心,主要分布于中国、欧洲和北美,在全球拥有27000多名员工、1700多名研发人员。公司的业务分为两个部分,CSL Behring(杰特贝林)致力于开发和提供治疗罕见和严重疾病患者的高质量药物,业务涵盖了免疫学、血液学、心血管和代谢、呼吸系统和移植治疗领域,市场分布于亚太地区、欧洲、拉丁美洲和北美的100多个国家;Seqirus是全球最大的流感疫苗提供商之一,运用基于鸡胚和细胞的制造技术与知识产权在美国、英国和澳大利亚经营着先进的生产设施,并在20多个国家拥有领先的研发能力、广泛和差异化的产品组合和商业运营能力。
一、2019/2020财年业绩
2020年8月19日,CSL公布其2019/2020财年业绩。根据财报,CSL公司2019/2020财年(2019年7月1日至2020年6月30日)销售业绩达87.97亿美元,以固定汇率计算,同比增长9%;税后净利润为21.03亿美元,以固定汇率计算,同比增长17%。这得益于免疫球蛋白产品组合的强劲增长;在B型血友病药物IDELVION®(albutrepenonacog alfa,凝血因子IX[重组],白蛋白融合蛋白,rFIX-FP)的推动下,血友病产品组合的成功商业化;中国业务分销模式的转变;以及子公司Seqirus实施了产品差异化策略,利润增长强劲。
注:澳大利亚企业的财政年度自7月1日起至次年6月30日止。
CSL Behring业务
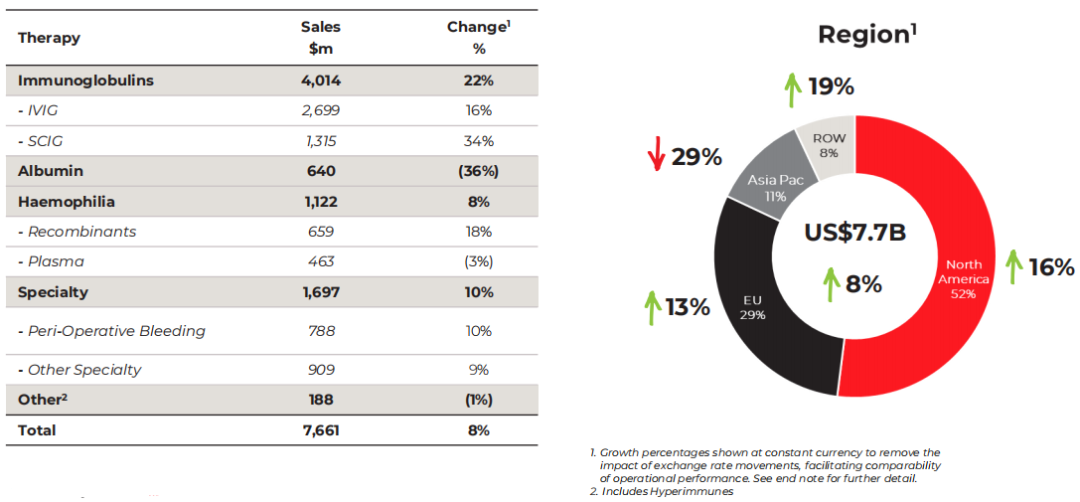
图源:CSL财报
CSL Behring业务总营收为76.61亿美元,以固定汇率计算,同比增长8%。
其中,免疫球蛋白产品营收达40.14亿美元,同比增长22%。静脉注射用免疫球蛋白制剂(IVIG)营收为26.99亿美元,同比增长16%;皮下注射用免疫球蛋白制剂 (SCIG)营收为13.15亿美元,同比增长34%。这是由于全球对人免疫球蛋白产品的需求持续增长,人们的疾病意识和医疗机构的诊断能力不断提高,以及免疫球蛋白用于治疗慢性疾病和原发性免疫缺陷的使用量增加。此外,PRIVIGEN®(Immune Globulin Intravenous,静脉注射用人免疫球蛋白)和HIZENTRA®(Immune Globulin Subcutaneous,皮下注射用人免疫球蛋白)于2018年在美国获批用于治疗炎症性脱髓鞘性多发性神经病(CIDP),2019/2020财年业绩分别同比增长20%和34%。HIZENTRA®继续保持着其市场领导地位,该产品是唯一被批准用于治疗CIDP的皮下注射产品,且在美国被授予针对该病的孤儿药独占(ODE)资格。
白蛋白产品营收为6.4亿美元,同比下降36%,这是因为CSL于2020财年在中国市场转为自主分销模式,并自持经营相关的《药品经营质量管理规范》(GSP)许可证,这有利于提升公司为患者服务的能力,扩大产品范围。但是除中国外,白蛋白业务在全球其他地区的成交量增长16%,其中欧盟地区增长24%,北美地区增长6%,除中国外的新兴市场销量增长28%,总体来说符合预期。
血友病产品营收11.22亿美元,同比增长8%。CSL Behring的血友病产品组合持续发展,重组凝血因子产品业绩达6.59亿美元,同比增长18%;由于竞争的不断加剧,血源凝血因子产品业绩为4.63亿美元,同比降低3%。
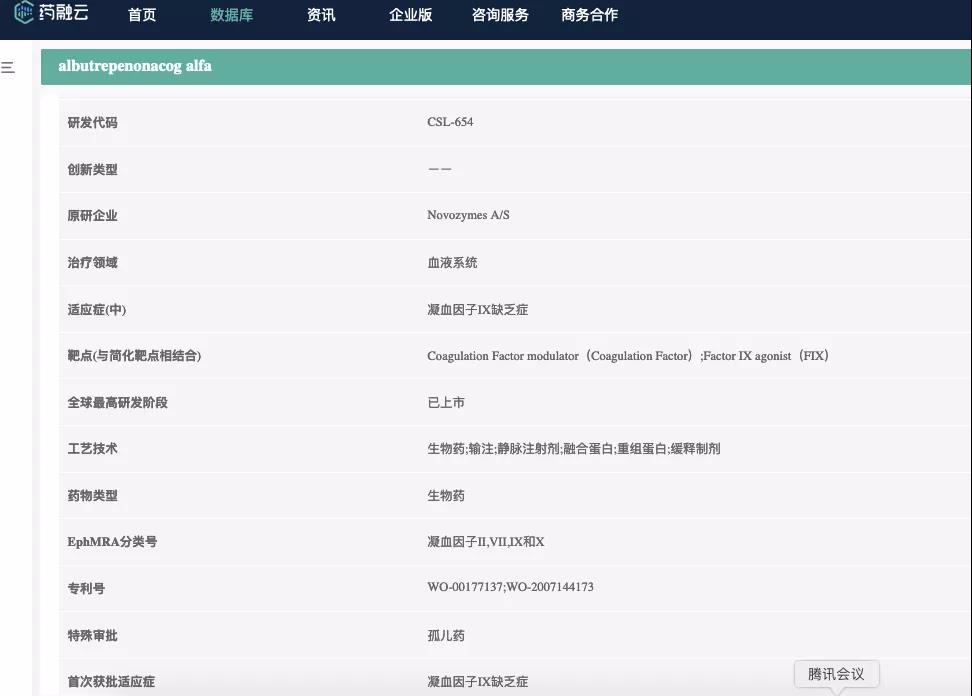
药融云数据,www.pharnexcloud.com
IDELVION®(albutrepenonacog alfa,凝血因子IX[重组],白蛋白融合蛋白,rFIX-FP)是用于治疗B型血友病的新型长效重组凝血因子IX产品,也是第一个可用于21天给药方案的凝血因子IX产品,已成为治疗B型血友病最常用的预防性治疗药物,其市场继续保持强劲增长,2019/2020财年业绩同比增长25%。AFSTYLA®(lonoctocog alfa,重组单链凝血因子VIII,rFVIIISingleChain)是一种用于治疗A型血友病的新型重组凝血因子VIII产品,是首个获批治疗A型血友病的单链凝血因子产品,具有非常卓越的治疗出血和预防出血效果,由于其对血管假性血友病因子(VWF)具有极强的亲和性,因而具有更高的分子稳定性和更长的疗效持续时间。尽管市场竞争激烈,但该产品也实现了21%的强劲增长。
特殊产品营收为16.97亿美元,同比增长10%。主要驱动因素来源于KCENTRA®(Prothrombin Complex Concentrate, Human,人凝血酶原复合物)和HAEGARDA®(C1-INH,皮下注射型[人]C1酯酶抑制剂)的强劲业绩表现。KCENTRA®用于成人因维生素K拮抗剂(VKA)抗凝治疗所致的急性大出血的紧急逆转性治疗,2019/2020财年业绩同比增长12%。HAEGARDA®是首个预防遗传性血管性水肿(HAE)发作的皮下治疗选择,且在2017年被FDA授予了7年的孤儿药独占(ODE)资格。
Seqirus业务

图源:CSL财报
Seqirus业务总营收为12.97亿美元,以固定汇率计算,同比增长11%。主要是受到了季节性流感疫苗业务推动,该部分业务同比增长21%。公司表示,其差异化的产品组合推动了出色的业务表现。FLUAD®(MF59-Adjuvanted Influenza Vaccine,含佐剂流感疫苗)是第一种佐剂四价流感疫苗,用于帮助65岁及以上老年群体抵御季节性流感,该产品与针对成人和儿童的FLUCELVAX®四价流感疫苗的需求均显著增加。同时,真实世界证据持续表明了这些产品的有效性。
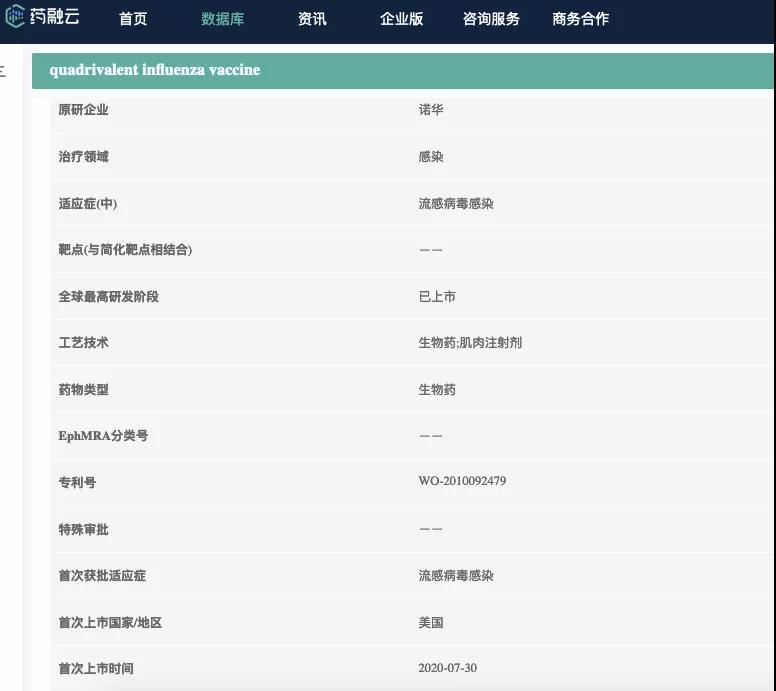
药融云数据,www.pharnexcloud.com
二、2020/2021财年上半年业绩
2021年2月18日,CSL披露了2020/2021财年上半年(2020年7月1日至2020年12月30日)业绩,据公告,公司上半年销售业绩达55.12亿美元,以固定汇率计算,同比增长17%,总营收为56.53亿美元,同比增长15%,税后净利润为17.94亿美元,同比增长44%。
CSL Behring业务
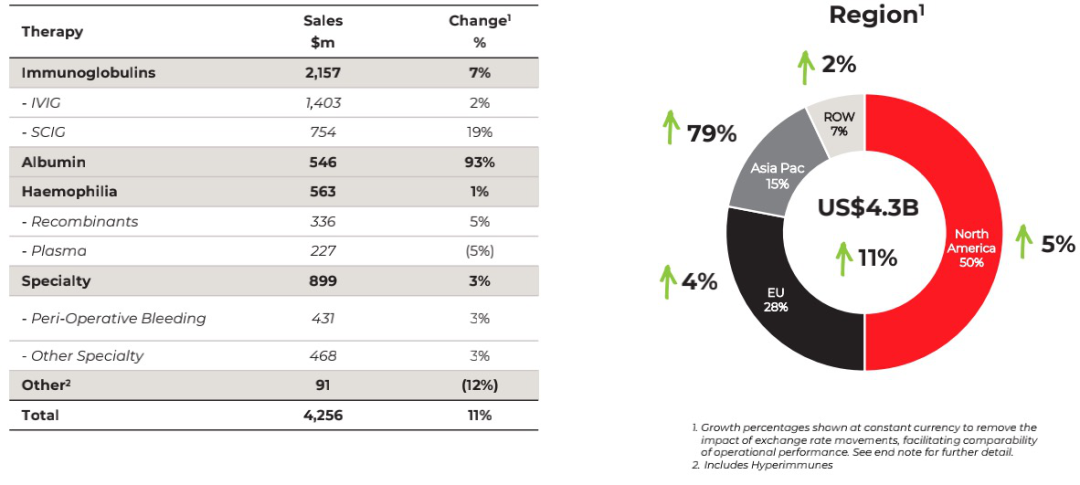
图源:CSL财报
CSL Behring业务总营收为42.56亿美元,以固定汇率计算,同比增长11%。其中,免疫球蛋白产品营收达21.57亿美元,同比增长7%,这主要是由于免疫球蛋白用于治疗慢性疾病和的使用量稳定增长。HIZENTRA®(Immune Globulin Subcutaneous,皮下注射用人免疫球蛋白)业绩同比增长19%,这得益于该产品灵活的给药方式,以及扩大了适应症范围。同时,该产品在美国持续推进针对炎症性脱髓鞘性多发性神经病(CIDP)的市场,据悉,目前已有60%的目标医师采用HIZENTRA®来治疗CIDP。此外,PRIVIGEN®(Immune Globulin Intravenous,静脉注射用人免疫球蛋白)业绩也有小幅增长。
白蛋白产品营收与去年同期相比几近翻倍,达5.46亿美元,同比增长93%,主要是因为这部分业务在中国实现了自持经营相关《药品经营质量管理规范》(GSP)许可证的过渡,先前因为新冠疫情导致的医院内手术数量减少也随着中国疫情的缓和恢复到了90%的正常水平。此外,欧盟和新兴市场增长强劲,而美国市场与去年同期相比持平。
血友病产品收入为5.63亿美元,同比增长1%。其中,IDELVION®(albutrepenonacog alfa,凝血因子IX[重组],白蛋白融合蛋白,rFIX-FP)显著的临床疗效持续推动了患者需求,该产品业绩同比增长6%。HUMATE®(Antihemophilic Factor/von Willebrand Factor Complex (Human), Dried, Pasteurized,抗血友病因子/血管性血友病因子复合物[人])成为了治疗血管性血友病(vWF)的领导者,业绩同比增长6%。但由于持续的市场挤压,A型血友病产品AFSTYLA®(lonoctocog alfa,重组单链凝血因子VIII,rFVIIISingleChain)营收相比去年同期持平,BERIATE® 和HAEMATE®的需求量持续下跌。
特殊产品营收为8.99亿美元,同比增长3%。主要驱动因素仍然来源于KCENTRA®(Prothrombin Complex Concentrate, Human,人凝血酶原复合物)和HAEGARDA®(C1-INH,皮下注射型[人]C1酯酶抑制剂)。KCENTRA®业绩同比增长6%。HAEGARDA®在欧盟与澳大利亚相继获批,患者需求增长,其业绩相比去年同期增长16%。不过,由于在美供应中断,α1蛋白酶抑制剂业绩同比降低7%,激烈的市场竞争使创伤愈合产品业绩降低26%。
Seqirus业务

图源:CSL财报
Seqirus业务总营收为14.25亿美元,以固定汇率计算,同比增长38%。季节性流感疫苗业务增长强劲,与去年同期相比增长44%。公司表示正在持续推进差异化的产品组合,FLUAD®(MF59-Adjuvanted Influenza Vaccine,含佐剂流感疫苗)与FLUCELVAX®四价流感疫苗业务在德国重新开展,FLUAD® QIV在美获批,同时公司还为新冠疫苗开发提供了MF59®佐剂技术。
三、最新研发管线
CSL在全球共有1700多名研发人员,其研发足迹分布于澳洲、亚洲、欧洲、北美洲等地区。
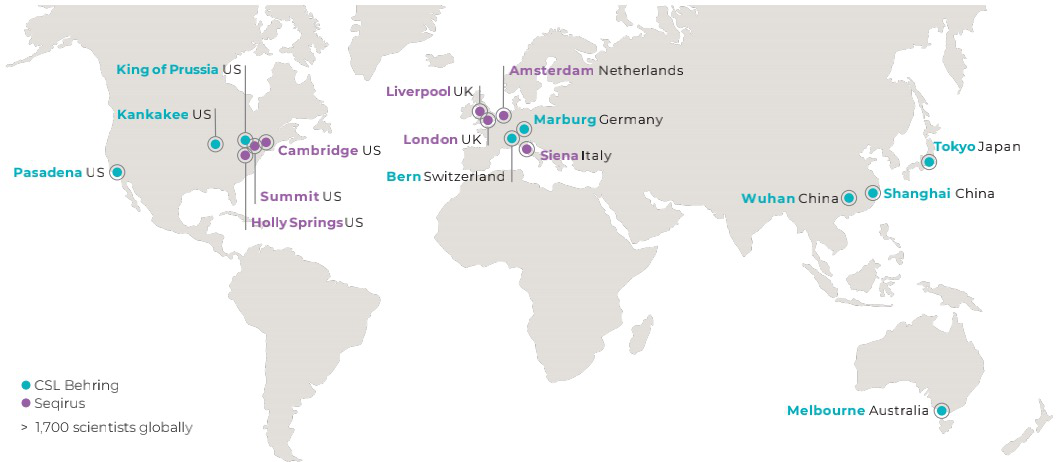
图源:CSL
据药融云数据(www.pharnexcloud.com)与CSL官网公布的最新研发管线,公司目前共有45个在研项目,利用血浆成分平台、重组技术、细胞与基因治疗平台、以及基于细胞或鸡胚的疫苗开发平台,专注于免疫学、血液学、呼吸系统、心血管与代谢、移植系统以及流感与传染病疫苗的开发。
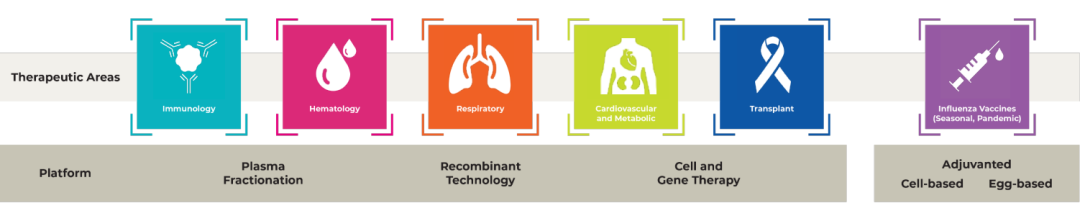
图源:CSL
所有在研项目中,血液领域候选产品最为丰富,有10项;其次为免疫学产品共9项;流感疫苗产品有6项;呼吸系统、移植系统产品分别有5项;心血管与代谢3项;COVID-19相关药物有3项;以及4个out-licensed项目。其中,处于药物发现阶段的6项,临床前研究阶段6项,临床1期阶段的有8项,临床2期7项,临床3期阶段10项,处于申报与审批阶段的产品有8项。
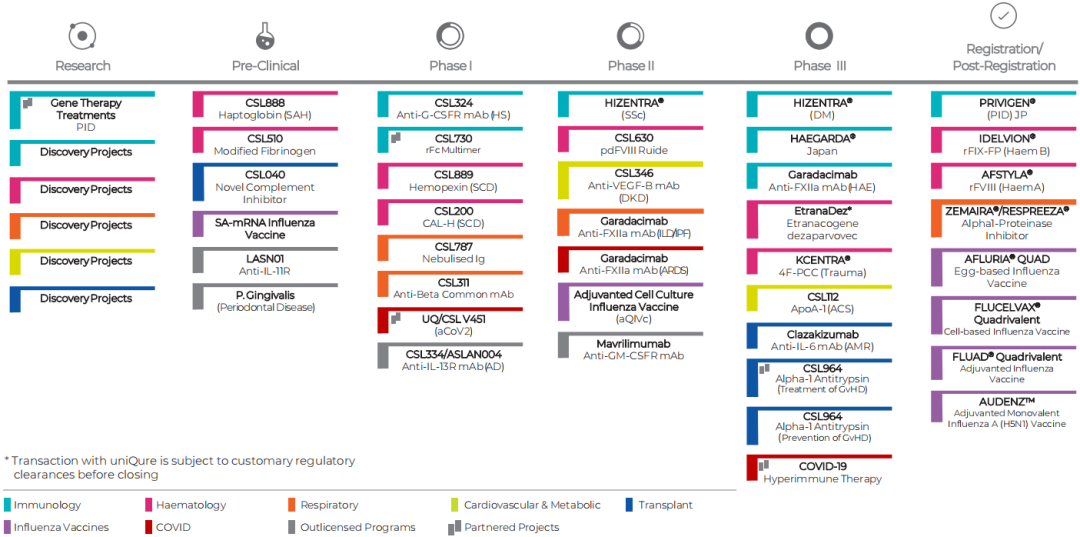
图源:CSL
四、免疫学
免疫球蛋白(Ig)是CSL公司免疫学治疗领域的基础,适应症涉及原发性和继发性免疫缺陷(PID/SID)和慢性炎症性脱髓鞘性多发性神经病(CIDP)等。HIZENTRA®(Immune Globulin Subcutaneous,皮下注射用人免疫球蛋白)除了用于治疗CIDP之外,正在拓展其他适应症,该产品正在被研究用于治疗系统性硬化症(SSc),也即硬皮病,以及皮肌炎(DM),并且已分别开展了2期和3期临床试验。遗传性血管性水肿(HAE)产品HAEGARDA®(C1-INH,皮下注射型[人]C1酯酶抑制剂)正在日本开展3期临床试验。Garadacimab是一种新型因子XIIa抑制性单克隆抗体(FXIIa-mAb),目前正开发作为一种每月一次皮下注射药物,用作遗传性血管水肿(HAE)的一种预防性疗法,且已进入3期临床试验。PRIVIGEN®(Immune Globulin Intravenous,静脉注射用人免疫球蛋白)已在日本提交申请用于治疗原发性免疫缺陷病(PID)。
五、血液病学
2020年6月24日,CSL Behring宣布以20.5亿美元引进uniQure的B型血友病基因疗法EtranaDez(Etranacogene dezaparvovec)的全球开发和商业化权益,B型血友病患者由于编码凝血因子IX(FIX)的基因出现突变,导致FIX缺失或缺陷,该疗法旨在使用AAV5载体递送表达FIX Padua变体的转基因,目前,该项目正处于3期临床试验。KCENTRA®是一款4因子凝血酶原复合浓缩物(4F-PCC),目前公司正在开发该产品应用于创伤愈合,且已进入3期临床试验。此外,IDELVION®(albutrepenonacog alfa,凝血因子IX[重组],白蛋白融合蛋白,rFIX-FP)已在日本获批作为治疗B型血友病的21天给药方案。
六、呼吸系统
α1抗胰蛋白酶缺乏症(AATD)是一种遗传性代谢疾病,可严重影响患者的肺功能,该病特点是AAT缺乏或水平低,AAT是一种抑制中性粒细胞弹性蛋白酶的天然蛋白质,可防止肺组织的破坏,CSL Behring开发的Zemaira®(α1蛋白酶抑制剂[人])是一种天然的、人血浆来源的α1抗胰蛋白酶(AAT),已被批准用于存在肺气肿临床证据的AATD成人患者的慢性增强和维持治疗,在欧洲,该产品以品牌名Respreeza®上市销售。CSL787(Nebulised Ig)是一种通过雾化器给药的人血浆免疫球蛋白,用于潜在预防慢性呼吸道感染和慢性肺病的进展,目前已开启1期临床试验。
七、心血管与代谢
CSL112 (ApoA-1)是一种来自血浆的重组人体ApoA-I制剂,用于调节胆固醇从动脉中抽离,迅速减少负载胆固醇的斑块,从而降低心血管事件的发生,针对该产品的3期临床试验已纳入11500例患者,并已成功完成首次无效性检验分析(futility analysis)。CSL346 (Anti-VEG-B)是一种靶向VEGF-B的人源化单克隆抗体,可用于治疗糖尿病肾病(DKD),目前已开启2期临床试验。
八、移植系统
CSL964(Alpha-1Antitrypsin)是一种α1-抗胰蛋白酶(AAT),通过下调炎症和增加调节性T细胞与效应T细胞的比率来抑制移植物抗宿主病(GvHD),目前该产品预防与治疗接受异基因造血干细胞移植 (HSCT) 的高危患者的类固醇难治性急性移植物抗宿主病 (GvHD)的研究均已进入3期临床试验。人源化抗IL-6单克隆抗体Clazakizumab(克拉扎珠单抗),被开发用于潜在治疗慢性活动性抗体介导的排斥反应 (AMR),这是肾移植受者长期排斥反应的主要原因,目前该研究已进入3期临床试验。
九、流感疫苗
AUDENZ™(甲型流感[H5N1]单价疫苗,佐剂)结合了MF59佐剂和基于细胞的抗原制造技术,目前已被批准用于6个月及以上的人群的主动免疫,帮助保护免受甲型流感(H5N1)的侵害,该产品是用于大流行时预防甲型H5N1流感的首个佐剂、基于细胞的流感疫苗。4价流感疫苗Afluria® Quadrivalent已被批准用于6个月及以上群体,预防由2种甲型流感病毒和2种乙型流感病毒引起的流感疾病。此外,以MDCK细胞系制备的四价灭活流感疫苗FlucelvaxQuadrivalent®(QIVc)已获得批准用于预防成人和儿童流感。
十、血浆采集中心
作为血制品龙头,CSL的血浆采集网络仍在不断扩展,截至2020财年,公司在全球拥有277个血浆采集中心,仅美国就有261个,德国有8个,还有3个在匈牙利,5个在中国。公司还计划在2021财年新增20-30个采集中心。
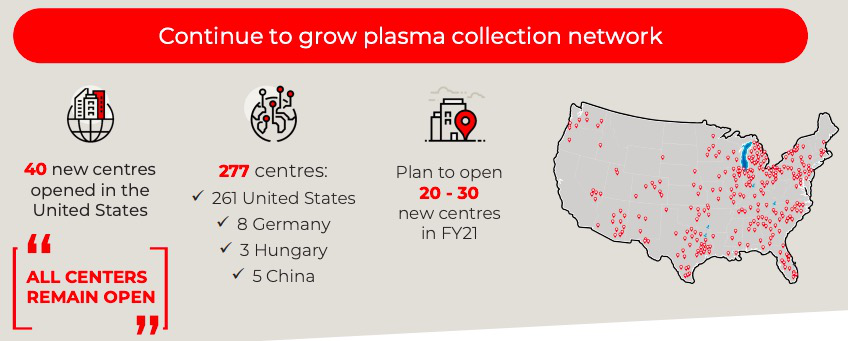
图源:CSL
十一、CSL在中国
1997年起,CSL Behring(杰特贝林)开始在中国销售人血白蛋白,2009年,正式建立中国总部。目前CSL Behring已成为中国市场该产品的主要供应商之一。2017年6月,CSL Behring以3.52亿美元收购人福集团持有的中原瑞德80%股权,再于2018年6月以1.02亿美元收购剩余 20%股权,加强在中国血制品市场进行战略性业务布局。2018年5月,CSL Behring收购广州君信药业有限公司,促进CSL Behring的进口白蛋白和中原瑞德的产品在中国销售。此外,公司还与中国企业百洋医药、广州医药达成合作协议进一步加强在零售药房和医疗机构的销售。2019年4月,CSL Behring与国药控股达成战略合作,启动第四方物流运营模式,从产品进口、物流以及分销到客户服务端到端的服务,进一步加强CSL Behring产品在中国的可及性。
十二、总结
血液制品属于刚性需求药品,在急救、感染以及凝血障碍疾病治疗上有着其他药品不可替代的作用。作为一家“百年老店”,也是澳大利亚血制品“独角兽”,CSL拥有过硬的技术和研发水平,其前身公司在研发和制造血制品中开发出一批里程碑式的产品,包括世界上第一种静脉注射用丙种球蛋白(IVIG)、经巴氏消毒处理的VIII因子、抗-D免疫球蛋白,还在1955年首次发现AIPI。除了保持疫苗+血制品的结构,CSL近年来先后收购基因疗法公司和单克隆抗体公司,开始布局单抗和肿瘤领域,寻求多元化发展。反观国内,我国的血液制品长期处于供不应求的状态,浆站设置门槛高,具有对地域和企业的双重高要求,总体来说,还有较大的提升空间。






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论