
ADC领域历经多年的技术积累和发展,已成为继PD-1之后又一热门赛道。据药融云数据,截至目前已有累计14款ADC药物在全球范围内获批上市,从2000年Mylotarg 的早期概念验证阶段,向定点偶联技术为特点的方向改进,再到近几年来以Enhertu 和Trodelvy 为代表新一代ADC技术以其突破性的临床试验数据站上行业舞台,使得该领域在历经几代技术革新后迎来快速发展的市场机遇。2021年Nature期刊预测目前已上市的ADC药物全球销售额将在2026年超过164亿美元,成为百亿美元级别的重磅市场。
ADC药物是新药研发的热门赛道,国产的ADC 药物,荣昌生物维迪西妥单抗于2021年6月已经获批上市,云顶新耀的国内首款TROP-2 ADC药物戈沙妥组已经申报上市,目前进展到临床3期的有华东制药和东曜药业针对HER2 靶点的ADC药物。
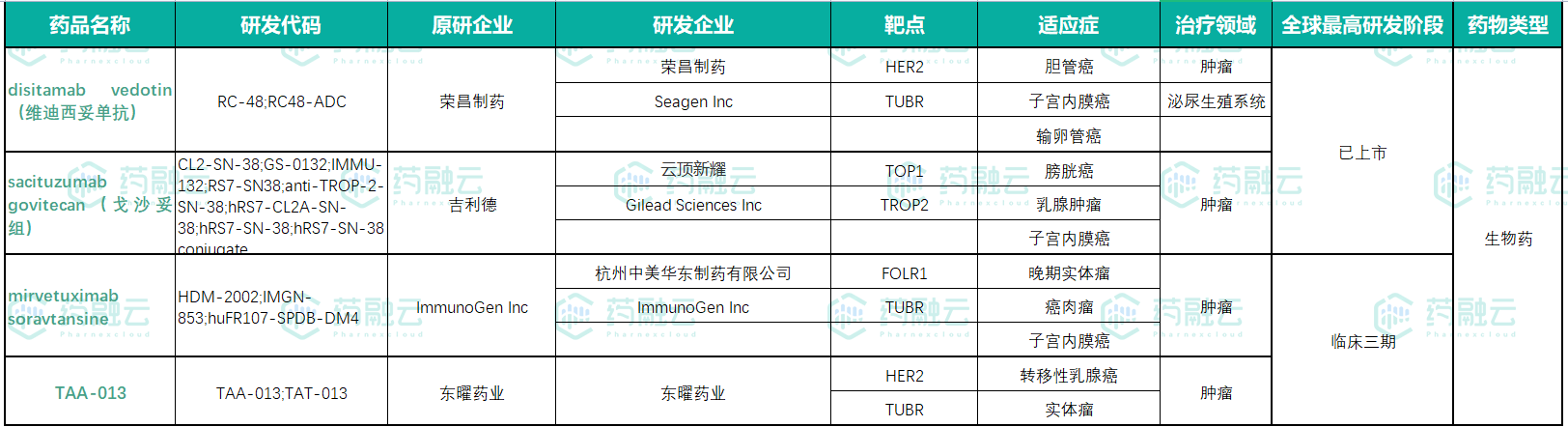
截图来源:药融云全球药物研发数据库
据药融云数据库,截止目前,国内ADC药物研发管线超120个,研发企业近70家,分布如下(欢迎补充更多企业信息):
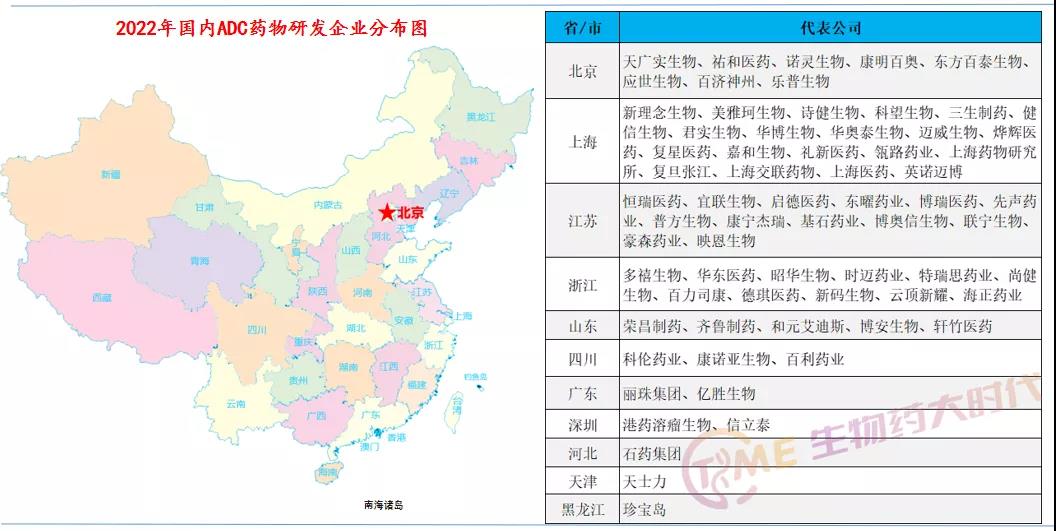
图片来源:生物药大时代
从上图可以看出,国内ADC药物研发企业主要分布在长三角和北京,长三角主要集中在上海、苏州和杭州。
作为超级魔法子弹,ADC药物作用机制如何理解,核心竞争力体现在哪里?ADC药物的过去、现在与未来又是怎样的?我们邀请到苏州宜联生物创始人薛彤彤博士就生物医药、ADC这块内容进行了深入探讨。

薛彤彤,苏州宜联生物创始人、董事长、CEO。此前在四川科伦药业任职,先后担任药物研究院副院长、科伦博泰CEO、Klus Pharma CEO,负责创新药物的研发与生产。曾任职于于齐鲁药业,负责重组蛋白药物的的开发工作,两个品种已经成功上市。近期,宜联生物宣布完成7000万美元B轮融资。
药鼎记:薛博士,您先自我介绍下吧。
薛博士:大家好,我很荣幸参加此次活动。我是宜联生物的董事长、CEO。2009年博士毕业后加入齐鲁制药,在齐鲁的生物研究院工作了4年。后来有幸加入科伦药业,工作了7年多,参与了一系列仿制药的开发,接触到ADC、重组蛋白等项目。这些是我在制药领域重要的经验积累。同时,在科伦工作期间,我还担任科伦博泰的总经理,当时有幸接触到很多小分子药物。后来在2020年时,我和几个志同道合的朋友一起组建了苏州宜联生物医药有限公司,公司专注的方向就是偶联药物。我希望能够站在前辈肩膀上,做出真正有国际化潜力的产品,打造一支具有竞争力的团队。
药鼎记:你在生物医药这块经验丰富,你能简单介绍下不同版本的生物医药公司是如何发展的吗?
薛博士:2000年后的生物医药,解决了药物合规性问题,开始进入创新阶段,很多医药项目有了广阔的市场。同时已经上市产品的疗效和安全性都得到了证明。随着生物医药的成熟,生物医药进入2.0阶段。这个阶段需要独立开发出具有知识产权的分子出来,例如PD-1。刚开始PD-1首家创新的市场空间非常大,但是大家很快掌握了这个技术,然后就出现了很多其它品牌进入临床或上市,由此PD-1竞争进入白热化阶段。不禁引人深思:我们该如何创新?如何获得更大的市场空间?除了中国市场外,如何在海外市场占据竞争力?于是生物医药进入3.0版本。这类公司开始建立创新型产品管线,通过融资进一步夯实管线,然后再建立技术平台,解决创新品种的临床转化问题,最终做出产品。后来又面临了新的问题:药物原创率不够。那怎么办呢?接下来我们应该向更有挑战的创新药物去迈进,并建立自己的独立知识产权,开发出推向国际的新品种,这也是生物医药4.0版本的工作内容。
药鼎记:薛博士,您是从无到有,并且有过千人管理经验,在这能不能给大家传授些宝贵经验?
薛博士:十年来,我迈出的每一步都比较坚实,然后又非常幸运得赶上行业红利期。在齐鲁制药的时候,我从一个小小实验员慢慢到自己独立带组再到后面创业。创业会让人学到很多宝贵的经验,因为你需要有创业型思考,善于学习和观察,了解管理中的问题。后来2013年的时候我去了科伦,在领导的信任下,开始做大分子。当时从零做起,团队规模小,没有大分子相关的平台,也没有项目。于是我们从选题立项,对外合作为切入点,不断向别人学习。然后逐步来提升自主研发与转化能力。2013~2016年,我们主要集中在大分子这块,团队由最初的5人发展到200余人。由于整个过程都是亲力亲为,我学习到很多经验,比如怎么组建团队?怎么管理团队?怎么保证团队的效率?这些经验都很宝贵。后来在科伦博泰时,作为总经理,我有不少机会与其他人交流学习。在科伦博泰我积累了药理毒理、小分子药物的开发、临床团队建设、独立上市等方面的知识和经验。所以在做项目、技术的过程中要不断地建设团队、管理团队,然后上升到建设公司、管理公司,这些都是逐步实践出来的。最后,我想说的是所有的事都不是凭空而来的,遇到了,就抓住机会,不断努力。
药鼎记:对于ADC的历史发展的回顾,ADC核心竞争力体现在哪里?
薛博士:ADC这个概念在1913年被德国科学家保罗·埃尔利希提出,并将ADC称呼为“魔法子弹”。100多年来将其分为四个阶段:
第一阶段:1913-1980年,主要处于临床前一些探索,受限于本身抗体的开发能力,工程化能力有限,ADC相关产品无法在人身上验证;
第二阶段:1980-2000年,抗体技术成熟,ADC产品陆续进入临床,开始有产品进入上市阶段;
第三阶段:2000-2015年,更多产品上市,探索解决前代问题;
第四阶段:2015以后进入快速发展阶段,第四代技术得到验证,有相关产品上市,第四代产品上市标志着ADC能够在更多的靶点、更多事情上成药,把ADC 推向新的高度。
第一代 ADC 的小分子毒性不够强,ADC 不够稳定,大多以失败告终;第二代药物采用毒性更强大的小分子,克服了第一代效力不足的弱点,并对抗体进行了优化,但仍采用传统化学方式偶联,容易在血液中裂解造成严重毒副作用;第三代 ADC的诞生主要得益于定点偶联技术的发展,使得药物在体内分布、代谢和排泄等复杂问题变得简单。
ADC由三部分组成:抗体、毒素、连接物。它们也是打造ADC核心竞争力的三大要素。通过连接物把抗体和小分子偶联到一起,克服缺点,充分发挥抗体和小分子的优势,扩大治疗窗。我们都知道抗体本身具有靶向性,如果说靶点本身的表达特异性很好,然后抗体和小分子结合之后能够很好的内吞。那这就是一个非常优秀的ADC的靶点。然后抗体和靶点结合,把小分子携带到细胞内,发挥对肿瘤的杀伤作用。这样能够扩大小分子在肿瘤治疗当中的效果,减少毒副作用。
药鼎记:如何理解的ADC的作用机制?国内ADC如何平衡抗体、毒素、连接物?
薛博士:对于ADC来言,抗体是导弹,希望它打哪里就打哪里,但是因为其靶点自身的原因,除了在肿瘤部位高表达之外,在其他部分也会表达,因此打过去除了打在肿瘤细胞上也会打在正常组织上,这就属于靶点相关性的毒性,抗体携带高杀伤性毒素就是核弹,来发挥特定杀伤作用。目前,ADC就是为了能够在肿瘤环境特定释放后,结合靶点后释放出来,将肿瘤杀死后再释放出来,本身细胞毒的小分子还能够进入周围肿瘤细胞,将来的ADC进入肿瘤环境不用具体进入某种细胞就可以直接发挥杀伤作用,不借助某个肿瘤细胞。为了能够让更多肿瘤适应症有更好的产品,就需要一步步解决更多靶点成药的问题,还要解决疗效的问题。
药鼎记: 薛博士,你能为国内外ADC的发展情况做个比较吗?
薛博士:整体而言,ADC这块,美国还是领先的。ADC从上个世纪80年代进入到临床之后,一系列优秀的公司基本上都是在美国成立的。美国在ADC第二代技术、第三代技术和第四代技术方面都有涉及。欧洲也有ADC方面的公司。国内有些ADC公司的技术就是来源于欧洲。我认为荣昌生物值得大家去学习,它在ADC方面布局很早,虽然在开发过程中遇到了很多挑战,但是经过长期的努力,终于把合作靶点成功推上市。还有就是科伦,科伦是我原来服务的公司。它在14年就开始部署ADC了,目前有有三个品种处于临床阶段。整体而言,中国ADC第二代技术、第三个技术和第四代技术虽然相对晚些,但我相信随着大家的努力,会出现更多优秀的品种。
药鼎记: 对于ADC来说,未来需要进一步加强的关键点是什么?
薛博士:
a.疗效好的同时强调安全性。
b. 毒素linker偶联方式还需要进一步提升,并不是说抗体不主要,而是因为抗体技术手段越来越丰富,只要评价到合适靶点,充分利用技术就能拿到合适抗体。
c. 生物学的理解很重要。注重药效模型。尤其是灵长类动物,因为它们最接近人。
d.放大生产。整个ADC从早期选题对象到工程转化,是一个完全系统的工程,最后工艺和生产转化是很难的,很多优秀产品早期可以做出来,但是无法成药,目前很多ADC发展流派的生产放大问题也是一个巨大挑战,
e. 商业化。不能泛泛而谈直接说产品上市后可以卖多少钱,需要有更多合作伙伴和合作方去认可技术平台。
药鼎记: 您对ADC的未来有哪些展望?
薛博士:现ADC经过上百年的发展,接下来就是让更多的靶点成药,然后更好的解决实际问题。同时希望ADC能够向非肿瘤适应这方面发展。技术方面来讲的话,ADC在双抗、多种细胞毒、靶向小分子、核酸药物等方面都值得我们去探索。ADC的成功是经历了上百年的积累,但它的成功并不代表其它方向马上就能成功。因为新方向还需要大胆假设,小心求证。
总结
ADC药物作为近年来重要的肿瘤治疗手段之一,具有的独特的治疗价值。全球资本蜂拥进入到ADC领域,据药融云数据显示,最近3年已披露的BD交易总额超过300亿美元。近期,宜联生物完成7000万美元B轮融资,本轮融资由LYFE Capital(洲嶺资本)、启明创投联合领投,君联资本、正心谷资本及弘晖基金(HLC)等跟投。本轮融资所募集资金将主要用于公司新一代抗体偶联药物产品管线的临床试验开发,以及新型偶联药物早期研发。
随着行业的发展,竞争格局也将变得激烈,未来只有真正具备差异化技术特点的ADC研发公司才能脱颖而出,受到行业关注。
“药鼎记”,主要分享生物医药行业全产业链干货包含仿制药、新药BD投资、CXO、改良制剂、抗体、细胞基因治疗等干货,促进上下游建立信任合作。两年内精准服务300+生物医药领域大的企业+创业者建立IP。
参考资料:
药鼎记视频号
想要解锁更多药物信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药物竞争格局、申报情况、最新进展、涉及靶点适应症、市场规模与前景、可否投入研发与仿制!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论