
当下景气的ADC市场正在被更多进入者分食利润。
2022年11月15日,华东医药的美国合作方ImmunoGen,Inc.对外宣布,其用于治疗铂耐药卵巢癌的全球首创(first-in-class)ADC药物ELAHERE™(mirvetuximabsoravtansine-gynx)获得FDA加速批准上市。这也是全球第15款获批上市的ADC药物。
据药融云数据查询,目前全球共有15款ADC药物获批上市,从国内的研发进展来看,已有5款ADC药物获批上市,处于III期阶段的ADC候选药物超过10款,预计国内在未来2-3年内即将迎来ADC药物的爆发期(《全球获批上市的15款ADC药物大盘点!国内在售5款,涉及罗氏、辉瑞》)。
国内企业中,荣昌生物、云顶新耀、华东医药已有ADC药物获批上市;恒瑞医药、东耀药业、科伦药业、信达生物等公司的ADC药物已经处于临床III期阶段。其中科伦药业的两款ADC药物已经与默沙东达成授权许可协议。
截止到11月20日,根据各上市公司2022年Q3财报披露情况,我们统计了全球已经获批上市销售的ADC药物营收情况如下:Kadcyla(15.9亿美元)、Adcetris(6.01亿美元)、Enhertu(7.5亿美元)、Trodelvy(4.85亿美元)、Padcev(3.29亿美元)和Polivy(2.9亿美元)等。
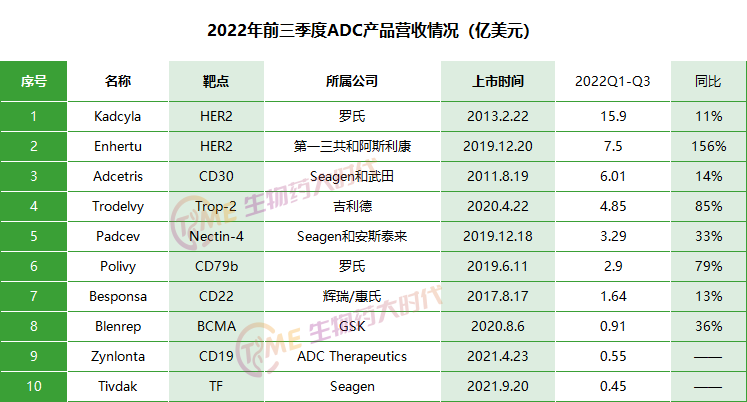
备注:Adcetris在2022年前三季度营收6.01亿美元(Seagen销售额)
Kadcyla在2022年前三季度营收15.9亿美元,同比增长11%。
Kadcyla(Adptrastuzumabemtansine,恩美曲妥珠单抗)由罗氏和ImmunoGen共同研发,于2013年2月22日被FDA批准用于HER2阳性转移性乳腺癌。2020年1月21日,该药成功在中国获批。它是我国首个上市的ADC药物,也是全球首款被批准用于实体瘤的ADC药物。2021年Kadcyla全球销售额为21.8亿美元,位居目前2022年ADC药物营收的榜首。

Adcetris在2022年前三季度营收6.01亿美元(Seagen销售额)。
Adcetris®(brentuximabvedotin,维布妥昔单抗,安适利®),由Seagen(原SeattleGenetics)原研,后来与Takeda联合开发。依照合作协议条款,Seagen拥有美国和加拿大的商业化权益,武田拥有世界其他地方的ADCETRIS商业化权益。Seagen与武田按50:50比例分摊ADCETRIS的开发费用,但在日本例外,武田独家负责在日本的开发费用。

武田的财报披露2个季度(2022年4月1日到9月30日), Adcetris销售额为417.15亿日元(约为3亿美元),同比增长22%。(武田财报周期:2022年4月1日到2023年3月31日)。
2011年8月19日,维布妥昔单抗获得FDA首次批准,用于治疗霍奇金淋巴瘤和系统性间变性大细胞淋巴瘤。2020年5月12日,获得我国NMPA批准,正式进入中国,是第二款国内获批上市的ADC药物。2021年Adcetris®全球销售额13.06亿美元,成为名副其实的重磅炸弹药物。
Enhertu在2022年前三季度营收7.5亿美元。
Enhertu是阿斯利康和第一三共合作开发的靶向HER2的第三代ADC药物,于2021年12月20日被美国FDA批准上市,用于治疗既往已经接受过2种以上HER2靶向疗法的不可手术切除或转移性HER2阳性乳腺癌成人患者。2022年3月21日,Enhertu在中国的上市申请获得NMPA受理。据阿斯利康2022年Q3财务披露,除日本外,第一三共和阿斯利康记录的全球市场今年迄今的销售额达到7.5亿美元(YTD2021:2.93亿美元)。其中在美国市场营收5.32亿美元。
吉利德以210亿美元收购Immunomedics后获得的核心药物Trop2-ADC药物Trodelvy,今年前三季度营收4.85亿美元,超过去年营收的3.8亿美元,同比大增85%。

Zynlonta(loncastuximabtesirine-lpyl)前三季度营收0.55亿美元。
ADC Therapeutics公司2021年4月23日宣布,FDA)已批准Zynlonta(loncastuximabtesirine-lpyl),用于治疗已接受过2种或多种系统疗法的复发或难治性(r/r)大B细胞淋巴瘤(LBCL)成人患者,包括弥漫性大B细胞淋巴瘤(DLBCL)、起源于低级别淋巴瘤和高级别细胞淋巴瘤的DLBCL。

该药目前在国内已经进行到III期临床,临床进展正在平稳推进。值得一提的是,Zynlonta是第一个也是目前唯一一个获批CD19靶向ADC药物。
ADC Therapeutics的研发管线

参考资料:
药融云数据库
各公司财报
<END>




































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论