
据药融云数据库,恒瑞医药目前至少已有4款核药在研,包括两款诊断用药和2款治疗用药。其中,1类新药HRS-4357注射液近日最新启动I/II期临床试验,旨在评价HRS-4357用于PSMA阳性晚期前列腺癌患者治疗的药代动力学及辐射剂量学、安全性及初步有效性。(登记号:CTR20232716)
截图来源:药融云中国临床试验数据库
根据恒瑞医药公告介绍,HRS-4357注射液为该公司研发的化学1类放射性治疗类创新药,适用于既往接受过雄激素受体(AR)通路抑制剂和紫杉烷类化疗的PSMA阳性的转移性去势抵抗性前列腺癌(mCRPC)成人患者。
mCRPC是前列腺癌的一种形式,已扩散至前列腺以外。据预估,有10%~20%的前列腺癌患者会于确诊后5~7年内发展成为mCRPC,临床存在未被满足的临床需求。公开资料显示,PSMA是由前列腺上皮细胞分泌的一种II型谷氨酸缩肽酶。研究显示,PSMA在超过90%的前列腺癌细胞表面都出现了过表达,并且在晚期和去势抵抗性前列腺癌患者癌细胞中表达水平更高。此外多种肿瘤的新生血管内皮细胞也高表达PSMA,这些特点使PSMA成为肿瘤靶向治疗领域的重要研究对象。
此外,前列腺癌是一种对放疗敏感的肿瘤。作为癌症治疗的支柱之一,放疗在杀死癌细胞的同时也会损伤健康细胞,产生严重的副作用。而靶向PSMA的放射性治疗药物有望增加放射性示踪剂在癌细胞内部的聚集,增强治疗效果。
关于前列腺癌,恒瑞另有放射性诊断药物HRS-9815注射液用于成人前列腺癌患者的前列腺特异性膜抗原(PSMA)阳性病灶的正电子发射断层扫描(PET)。
高壁垒核药赛道,市场规模将超百亿
核药(放射性核素偶联药物 ,Radionuclide Drug Conjugates, RDC)是指含有放射性核素,可以用于诊断或治疗的特殊药物。随着2013年拜耳研发的镭233药物Xofigo®获批上市,核药正式走进大众视野。
应用于人体内的核素药物可分为诊断用核药和治疗用核药。2022年,Nat Rev Clin Onco发表关于整个放射性药物市场份额的预测,可以看到目前市场分布还是以诊断药物为主,未来大体量的一定是放射性治疗药物。
2013-2026全球放射性药物市场预测
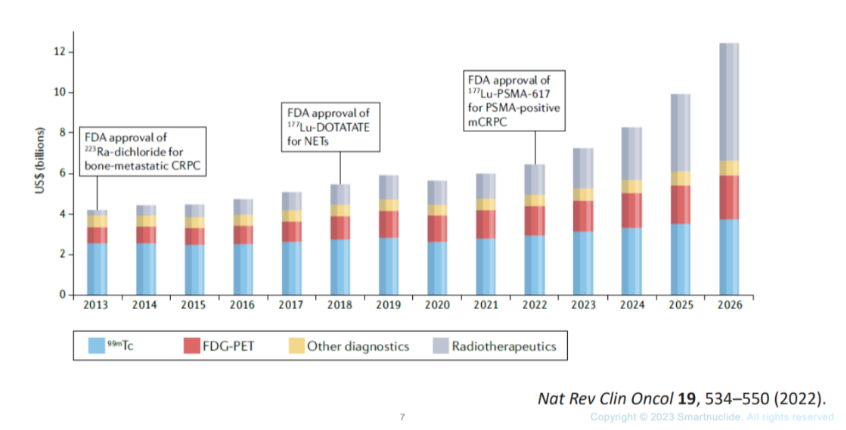
据 Frost & Sullivan,2013 年-2017 年国内放射性药物市场规模 CAGR 为 12.1%,增长态势领先于中成药和化学药,仅次于生物药,并预计 2023 年-2027 年复合增速达到 21.4%,预计到 2026 年市场规模将超过百亿。
从具体企业和药物来看,诺华的2023年中报显示,其创新核药Pluvicto(lu177-psma)二季度销售额为2.4亿美元(23H1销售额为4.5亿美元),环比一季度继续提升,体现了良好的市场前景。
不过,由于核药具有复杂的技术壁垒和政策壁垒,国内外布局者较少。国外有诺华、拜耳、Y-mAbs、TELIX、PRECIRIX、RayzeBio等;国内则主要是中国同辐和东诚药业的双寡头格局,恒瑞、远大医药、药明博锐、云南白药、先通医药等多家企业纷纷下场。
“医药一哥”,4大品种入局
据药融云数据库,在核药领域,恒瑞医药今年以来已有镥[177Lu]氧奥曲肽注射液、镓[68Ga]伊索曲肽注射液、HRS-4357注射液、HRS-9815注射液等四款产品获批临床。其中2款已进入临床。
镥[177Lu]氧奥曲肽注射液是天津恒瑞第一个放射性精准治疗产品,原研来自诺华,2017 年恒瑞以39亿美元收购获得,2022年以3类仿制化药申报临床。目前该药物在国内已进入临床三期阶段,适应症为晚期胃肠胰神经内分泌瘤。(登记号:CTR20230775)
镓[68Ga]伊索曲肽注射液是一款放射肿瘤诊断药物,用于诊断生长抑素受体阳性神经内分泌肿瘤。2023年6月底已获批三期临床,用于已确诊或疑似高分化胃肠胰神经内分泌肿瘤(GEP-NET)成人患者正电子发射断层扫描(PET)成像,以定位生长抑素受体过表达的原发肿瘤及其转移灶。
据悉,镓[68Ga]伊索曲肽注射液与镥[177Lu]氧奥曲肽注射液为一对“诊疗一体化”产品,这两款产品为恒瑞医药在核药领域布局的首对放射性精准诊疗产品,上市后有望为国内胃肠胰神经内分泌肿瘤患者带来新的治疗方案。原研产品于2016年在欧洲药品管理局EMA获批上市。目前国内均无原研及同类产品获批上市。
HRS-4357是一款治疗性核药,适用于既往接受过AR通路抑制剂和紫杉烷类化疗的PSMA阳性的转移性去势抵抗性前列腺癌(mCRPC)成人患者,全球尚未有同类产品获批。目前正在开展I期临床试验。
HRS-9815注射液和HRS-9815注射液制备用药盒为公司自主研发的首个放射性诊断类创新药,已于今年7月获批用于成人前列腺癌患者的前列腺特异性膜抗原(PSMA)阳性病灶的正电子发射断层扫描(PET)。国内外均未有同品种获批上市。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!





























![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://yaorongyun-public.oss-cn-shanghai.aliyuncs.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)










 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论