
GLP-1受体激动剂——Tirzepatide中国递交上市申请

礼来制药研发的GLP-1受体激动剂——tirzepatide最早于2022年5月13日获美国FDA批准上市,商品名为Mounjaro®。每周注射一次,辅助饮食和运动,以改善成人2型糖尿病患者的血糖控制。Tirzepatide也是近10年来首个新糖尿病药物类型。此前,礼来制药同时附上了一张优先审评券,以加快Tirzepatide上市。
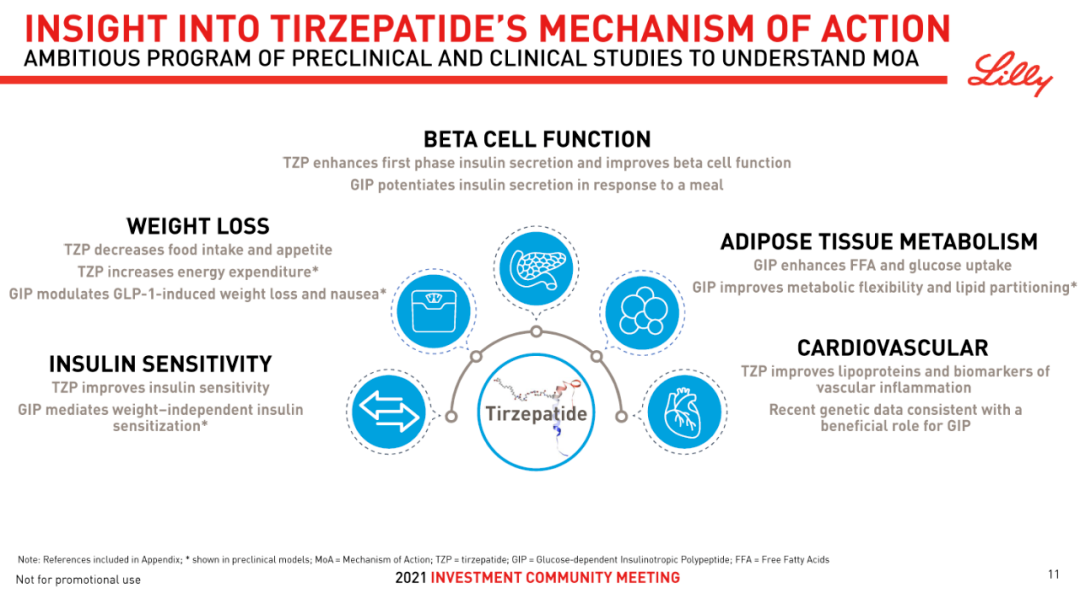
药融云数据,www.pharnexcloud.com显示:该GLP-1受体激动剂也是美国FDA在2022年上半年批准的16个新药中唯一的多肽类药物。据披露,礼来制药的tirzepatide每月治疗标价约为974美元。
近期(2022年9月),礼来制药已正式向中国国家药品监督管理局(NMPA)药品审评中心(CDE)递交Mounjaro® (tirzepatide)注射液(替尔泊肽注射液)用于在饮食控制和运动基础上改善成人2型糖尿病(T2DM)患者血糖控制的注册申请(《重磅降糖药最新申报!盘点礼来将在中国上市的9款药品》)。
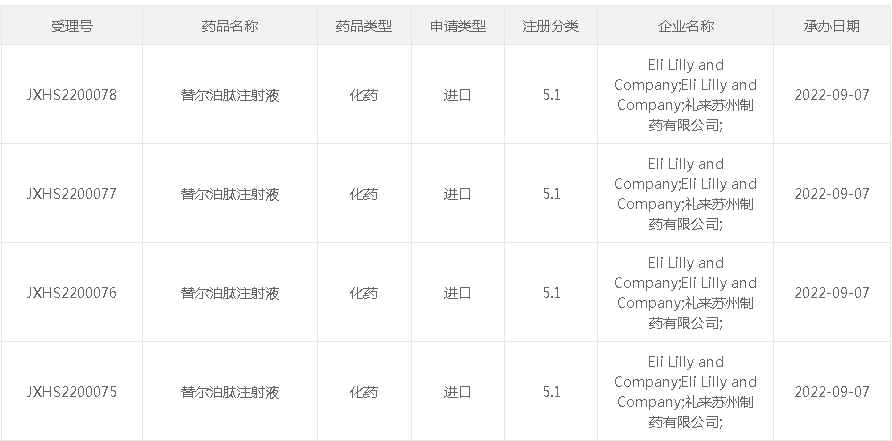
截图来源:CDE官网
礼来制药公司披露:本次向CDE递交的该项申请是基于在健康受试者或T2DM患者中开展的21项已完成的临床研究,其中包括五项全球(关键)III期研究—SURPASS系列临床试验,和一项亚太地区III期研究—SURPASS-AP-Combo临床试验(受试者98.3%为亚裔,83.4%为中国患者)。
SURPASS系列临床试验评估了Mounjaro® (5 mg,10 mg和15 mg) 作为单药治疗或与常用糖尿病处方药物联用的有效性和安全性。结果表明,Mounjaro®对HbA1c和体重产生了稳定且具有临床意义的降低,降幅大于所有评估的所有对照药物——安慰剂、注射司美格鲁肽1 mg、滴定的德谷胰岛素和滴定的甘精胰岛素。在SURPASS系列临床试验的受试者中,Mounjaro®5 mg的HbA1c平均降幅达1.8%至2.1%,Mounjaro® 10 mg和15 mg的平均降幅为1.7%至2.4%。目前礼来制药尚未申请减重适应症,但体重的平均变化是所有SURPASS系列临床试验的关键次要终点。接受Mounjaro®治疗的受试者体重平均降低约5 公斤(5 mg)至11 公斤(15 mg)。
Mounjaro®的总体安全性与已知的GLP-1受体激动剂相似。胃肠道副反应(恶心、腹泻、食欲下降、呕吐、便秘、消化不良和胃痛/腹痛)为最常见的不良反应,通常发生在剂量递增期,并随时间逐渐减少。
除此之外,礼来制药Tirzepatide还在国内布局了心血管系统疾病、NASH、睡眠呼吸暂停等适应症的研发。
Tirzepatide在国内开展登记的临床试验
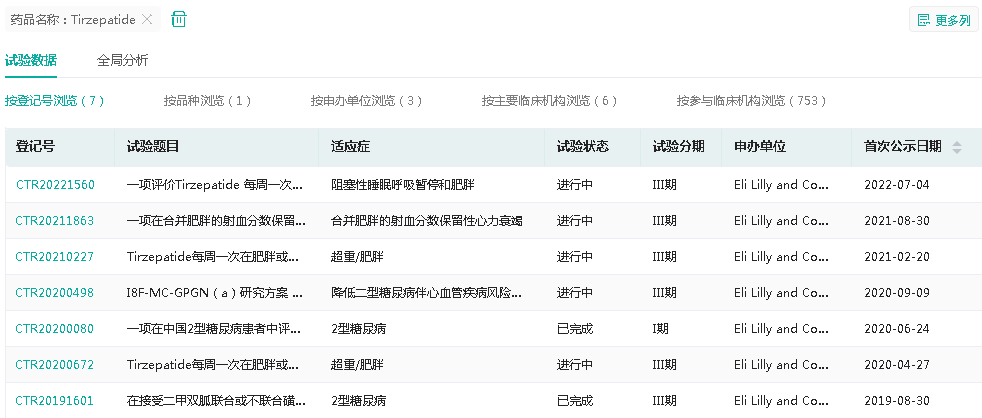
截图来源:药融云中国临床试验数据库
关于糖尿病
国际糖尿病联盟(International Diabetes Federation,IDF)2021年全球糖尿病地图显示,2021年全球成年糖尿病患者数量达到5.37亿例,全球约1/10的成年人受到影响。与2019年相比,糖尿病患者增加了7400万例,增幅达16%。预计到2025年,糖尿病患病率将进一步上升至12.2%,患病人数将增加到7.83亿例。2021年约有670万人死于糖尿病或糖尿病并发症,占到了全因死亡人数的12.2%。糖尿病在全球范围内造成的医疗卫生支出将近1万亿美元,占总医疗卫生支出的9%。
中国是成人糖尿病患者最多的国家,过去的10余年间(2011至2021年),我国的糖尿病患者由9 000万例增加至1.4亿例,增幅达56%,其中约7 283万例患者尚未被确诊,比例高达51.7%。另外,约有1.7亿成人伴有糖耐量受损,约2 700万成人伴有空腹血糖受损,这些人群都是糖尿病人群的“后备军”。预测到2045年,中国糖尿病患者数量将达到1.744亿例。
GLP-1类热门靶点

▲药融云数据全球药物研发数据库
本品亦在开发肥胖、心血管系统疾病(如射血分数保留的心衰(HFpEF))、NASH(代谢疾病)、睡眠呼吸暂停(OSA)等适应症。Tirzepatide作为一种每周一次的葡萄糖依赖性促胰岛素多肽(GIP)和胰高血糖素样肽-1(GLP-1)的双受体激动剂,一个分子实现两种肠促胰素的作用整合,相关专利WO-2016111971。GIP是一种肠促胰素,能够补充GLP-1受体激动剂的作用。在临床前模型中,已证明GIP可减少摄食量并增加能量消耗,从而减轻体重,当联合GLP-1受体激动剂时,可能对代谢紊乱如体重、血糖和血脂产生更大的影响。对于降糖或减重不同的适应症,礼来将实行双品牌策略(类似于诺和诺德的Wegovy和Ozempic)。
药融云数据,www.pharnexcloud.com显示:目前国内布局GLP-1受体激动剂类新药(含多靶点)的企业有:恒瑞医药、豪森药业(翰森制药)、先为达、华东医药及道尔生物、锐格医药、众生睿创、信达生物、奥达生物、硕迪生物、北京质肽生物、甘李药业、安源医药、博瑞生物、石药集团、东阳光、银诺医药、仁会生物、鸿运华宁、闻泰医药、华健未来、诺泰生物、昂博制药、赛诺生物、麦科奥特、北京东方百泰生物、恒诺康、晟斯生物、乐普医疗、诚益生物、领康Leadermed、派格生物、惠升生物、和煦加医药、中晟全肽、常山生化/常山凯捷健生物等。
此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场
参考:
NMPA/CDE;
CDE官网;
药融云数据:vip.pharnexcloud.com/?zmt-mhwz;
FDA/EMA/PMDA;
相关公司公开披露;
https://investor.lilly.com/news-releases;
https://www.fda.gov/news-events/press-announcements/fda-approves-novel-dual-targeted-treatment-type-2-diabetes;
https://www.prnewswire.com/news-releases/fda-approves-lillys-mounjaro-tirzepatide-injection-the-first-and-only-gip-and-glp-1-receptor-agonist-for-the-treatment-of-adults-with-type-2-diabetes-301547339.html;
https://diabetesatlas.org/data/en/;
https://www.rxlist.com/mounjaro-drug.htm;等等。
要解锁更多药企创新药信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、研发阶段、最新进展、申报获批情况、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论