"1类新药"相关的结果
-

2022年获批上市的1类新药盘点:共16款,小分子药物依旧亮眼
2022年完结在即,据药融云数据库,截至2022年12月27日,今年已经有50多款新药在中国获批,其中包括16款1类新药。获批上市的1类新药中有4个进口新药和12个国产新药。经过整理分析,可以发现,2022年获批上市的1类新药有三个特点。 -
11月新药研发大盘点!4款获批上市,103款获临床,还有多款获受理
据《药融云全球在研新药与靶点月报》数据统计,11月有四款新药获批上市,分别为盐酸安舒法辛缓释片(绿叶制药)、林普利塞片(璎黎药业、宣泰药业)、对甲苯磺酰胺注射液(红日药业)和羧基麦芽糖铁注射液(维福制药)。1类新药181402年前 -

最新16款1类新药获批临床!阿斯利康、齐鲁制药、荣昌生物在内
12月6日,据CDE官网,16款(治疗用生物制品10款,化药6款)1类新药获批临床,来自荣昌生物、齐鲁制药、阿斯利康、基石药业、上海海和药物等企业。经梳理,本次获批开展临床的疾病领域主要集中在抗肿瘤领域。本文挑选部分获批临床的1类新药进行简述。 -
恒瑞医药3款1类新药获批临床,均为首次!今年已累计拿下33款
据CDE官网,在刚刚过去的一周时间里(10月31-11月6),恒瑞医药陆续迎来HRS-1358片、HRS-1780片和SHR-7367注射液3款1类新药获批临床(默示许可),均为其首次获批。据药融云粗略统计,今年以来,恒瑞医药已累计有33款1类新药获批临床。 -

杭州地方助资再加码!1类新药最高4000万,2类最高2000万
10月15日,杭州市人民政府办公厅发布《关于加快生物医药产业高质量发展的若干措施》,重点支持药品、高端医疗器械、先进制药装备、新型服务外包、数字化医疗及医美等领域的研发、生产和服务。 -

7月国内新药研发盘点!28款新品首次亮相,恒瑞医药手握3款
据药融云统计,7月共有46款1类新药获得临床默示许可,其中28款为首次获批临床,包括恒瑞的3款新品、甘李药业的超长效胰岛素周抑制剂、君实生物的CD20/CD3双特异性抗体等。 -

恒瑞医药:又一款1类新药报上市!阿片类止痛药SHR8554注射液
2022年7月8日,CDE承办了江苏恒瑞医药股份有限公司的1类化药新药SHR8554注射液的上市申请。该药是恒瑞医药自主研发的靶向μ阿片受体(MOR)的小分子药物,用于治疗手术后疼痛,是阿片类止痛药中作用较强的一类。 -
-

1类新药遭国内药企猛攻!恒瑞医药、贝达药业等6家报产,本周25款获批临床
2月25日,CDE承办了亿帆医药子公司亿一生物制药在研产品艾贝格司亭α注射液的上市申请。这是今年报产的第6款1类新药。据药融云统计,本周已有25款1类新药获批临床,分别来自丽珠医药、和记黄埔、应世生物等药企。1类新药229002年前 -
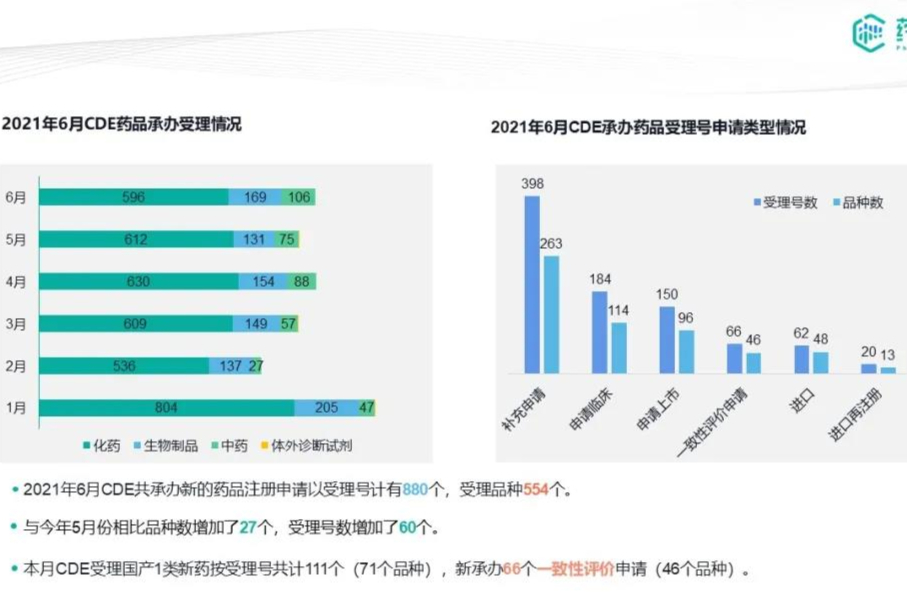
2021年6月|CDE药品审评报告-27个首家过评,扬子江|齐鲁|华润医药大丰收
6月CDE药品审评报告要点 ,27个首家过评,扬子江、齐鲁、华润医药大丰收!6月CDE药品审评报告要点 本月药审中心受理总量为880个 共有111个1类新药申请获CDE受理 本月新承办66个一致性评价申请 13款1类新药获批,泽璟生物1类创新药甲苯磺酸多纳非尼片重磅获批 113个品种通过(含视同通过)一致性评价,扬子江、齐鲁、华润医药大丰收 27个品种首家过评,齐鲁制药斩获2款首家


































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息