
12月6日,据CDE官网,16款(治疗用生物制品10款,化药6款)1类新药获批临床(默示许可),来自荣昌生物、齐鲁制药、阿斯利康、基石药业、上海海和药物等企业。经梳理,本次获批开展临床的疾病领域主要集中在抗肿瘤领域(12款),其他有眼科用药、痛风药等。
本文挑选部分获批临床的1类新药进行简述。
一、生物制品
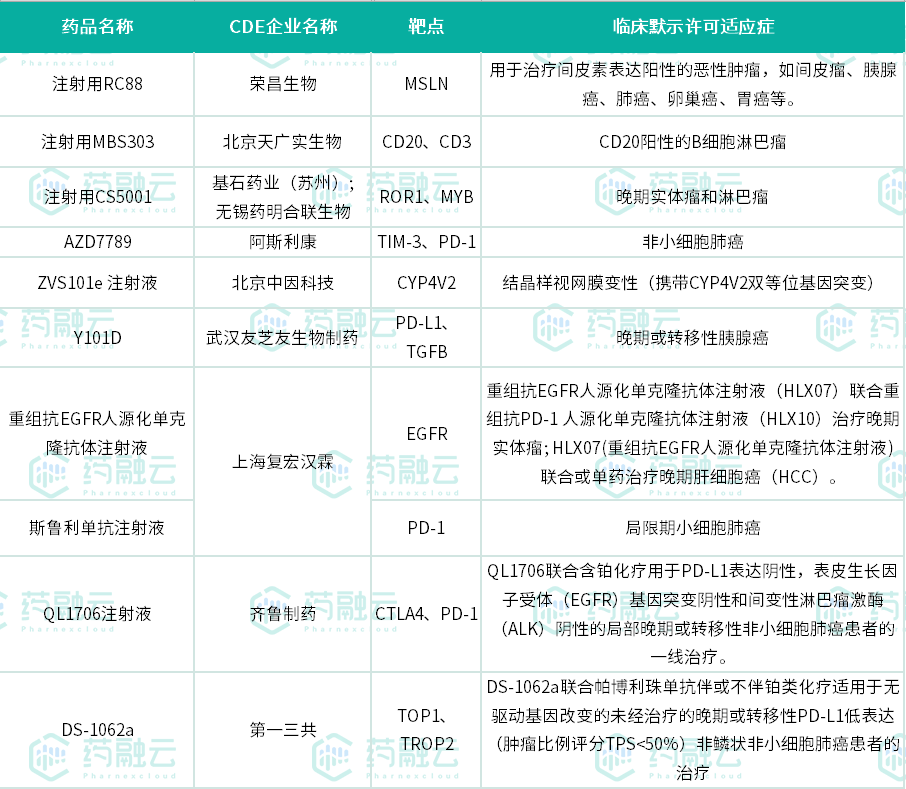
据药融云数据统计,本次共有10款生物制品1类新药获批临床,其中RC88、注射用CS5001、DS-1062a等均为ADC药物。
本次1类新药获批临床的生物制品(微信搜索"药融云小程序"进行相关更多数据查询)
- 01.荣昌生物:注射用RC88
RC88是一款新型抗间皮素ADC药物,结构包括间皮素(MSLN)靶向抗体、可裂解连接子以及微管抑制剂单甲基澳瑞他汀E(MMAE)。MSLN是一种肿瘤相关抗原,在正常组织中较少表达,通常在一些上皮性恶性肿瘤的细胞膜上过表达。
RC88通过靶向结合MSLN阳性的肿瘤细胞,介导抗体的内吞,从而有效地将细胞毒素定向传递给癌细胞,实现较好的肿瘤杀灭效果。目前,该产品在晚期恶性实体肿瘤患者中的I/IIa期临床研究正在进行中。
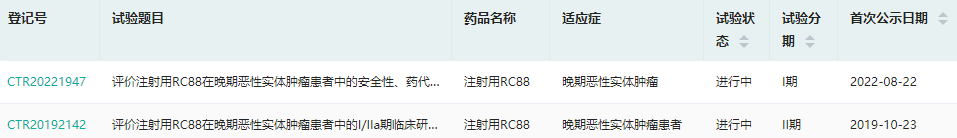
截图来源:药融云中国临床试验数据库
据悉,荣昌生物一共拥有4种ADC候选药物,除了RC88外,另有RC48(维迪西妥单抗,已上市)、RC108和RC118。
- 02.北京天广实生物:注射用MBS303
注射用MBS303是一款基于T细胞重定向的多特异性抗体技术平台研发的2:1结构CD20/CD3双特异性抗体,天广实生物拥有该项目的完全自主专利。基于特殊的抗体结构设计和计算机辅助抗体工程优化,MBS303在临床前研究表现出了更好的疗效,对T细胞的激活相对可控,引起的细胞因子释放水平更低,显示出了同类最优的潜力。
此次为该品种首次以1类新药获批临床(默示许可)。
- 03.基石药业:注射用CS5001
注射用CS5001是一款靶向酪氨酸激酶样孤儿受体1(ROR1)的潜在全球同类最佳抗体偶联药物(ADC),也是国内首款申报临床的ROR1 ADC药物,曾于今年1月获FDA批准临床今年11月,CS5001在国内最新开展并公示了其I期临床试验。

截图来源:药融云中国临床试验数据库
CS5001最早由LegoChem Biosciences(LCB)开发。2020年10月,基石药业引入CS5001的全球(除韩国)开发和商业化权益,交易总额为3.63亿美元(1000万美元预付款+3.53亿美元里程金)。
- 04.复宏汉霖:重组抗EGFR人源化单克隆抗体注射液(HLX07);斯鲁利单抗注射液
HLX07是复宏汉霖自主研发的针对EGFR靶点的创新型生物药。基于公司成熟的抗体工程改造平台,在西妥昔单抗的基础上,通过将HLX07的Fab区人源化,同时使该产品聚糖含量降至最低,以具备更低的免疫原性和良好的靶点亲和力。
据药融云数据库,HLX07已有多个适应症研发至临床II期阶段,包括肝癌、肺癌、鼻咽癌、直肠癌等多个癌种。
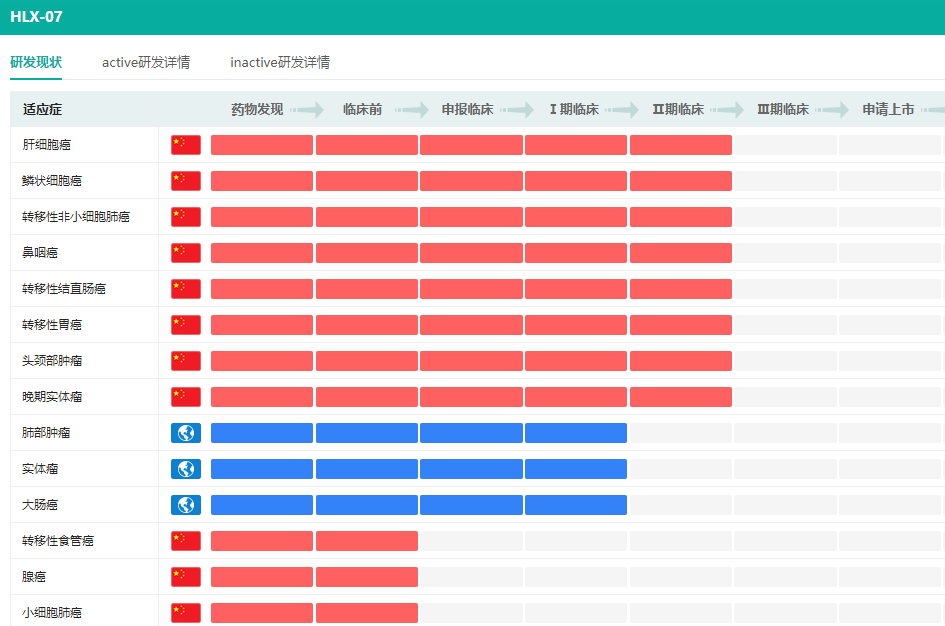
截图来源:药融云全球药物研发数据库
斯鲁利单抗注射液最早于今年3月在国内获批上市,用于单药治疗经标准治疗失败后、不可切除、转移性高度微卫星不稳定型 (MSI-H)实体瘤的上市申请获药监局批准,成为国内首个治疗MSI-H实体瘤的PD-1单抗和第13款PD-1/PD-L1类药物。今年11月,又获批联合卡铂和白蛋白紫杉醇用于一线治疗不可手术切除的局部晚期或转移性鳞状非小细胞肺癌(sqNSCLC)。
此外,斯鲁利单抗联合化疗一线治疗广泛期小细胞肺癌(ES-SCLC)和联合化疗一线治疗局部晚期/转移性食管鳞癌(ESCC)2项适应症的上市注册申请也已获药监局受理,正在审评审批中。
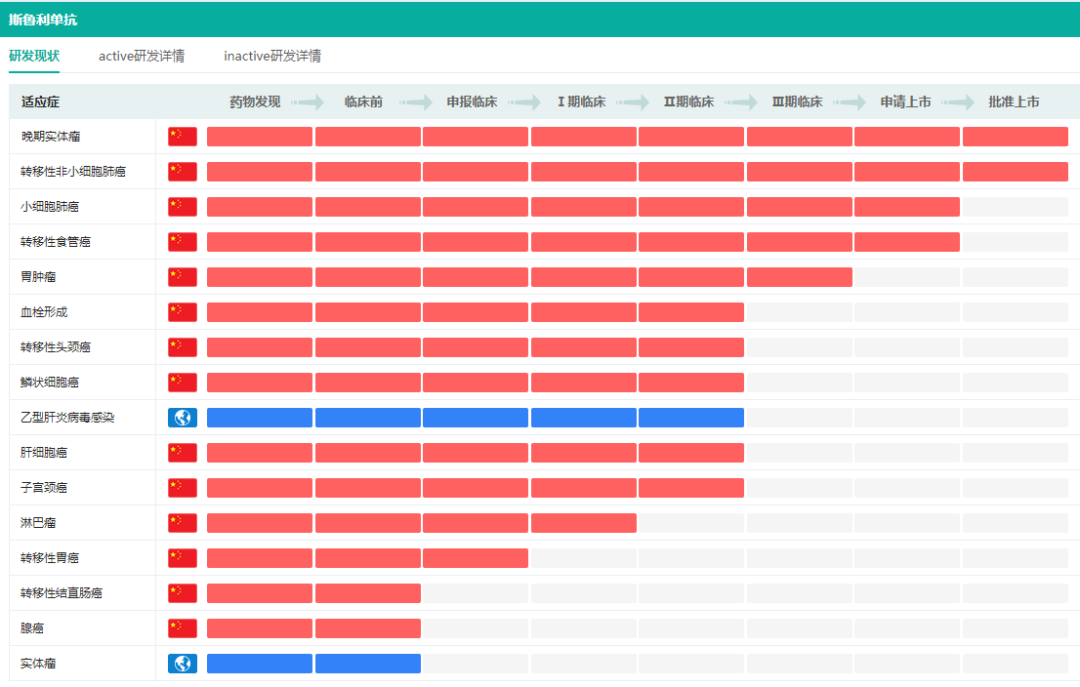
截图来源:药融云全球药物研发数据库
- 05.齐鲁制药:QL1706注射液
QL1706注射液今年1类新药获批临床(默示许可)的项目甚多,适应症覆盖肺癌、直肠癌、肾细胞癌、肝细胞癌、宫颈癌等多个癌种。
这是齐鲁制药基于MabPair组合抗体生物技术研发的,主要靶向PD-1和CTLA-4D的新型治疗用抗肿瘤组合抗体。目前,该药在国内有11项临床试验正在开展中,最高进度为III期临床,多为联合用药,涉及紫杉醇-顺铂/卡铂、吉西他滨、仑伐替尼、贝伐珠单抗等。
QL1706中国临床试验公示
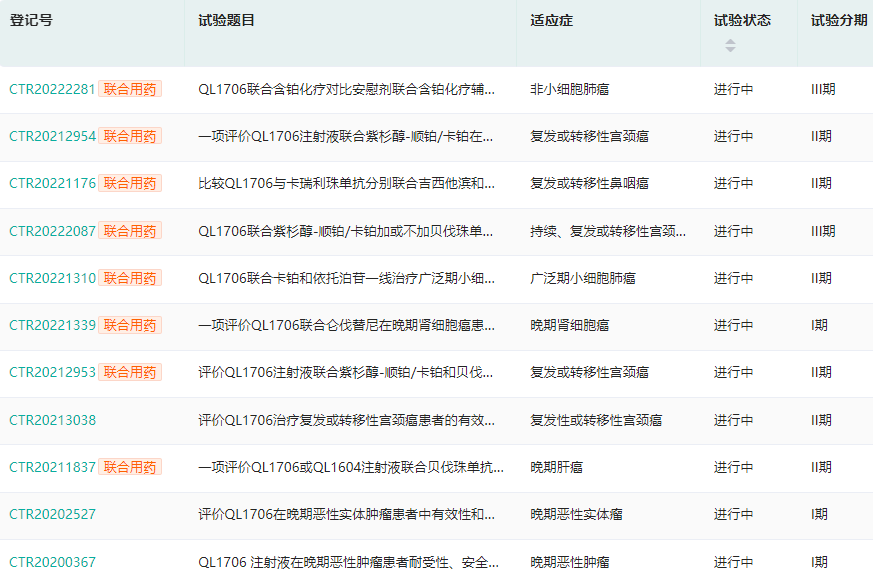
截图来源:药融云中国临床试验数据库
- 06.阿斯利康:AZD7789
AZD7789是阿斯利康在研管线中的一款抗PD-1/TIM-3双特异性抗体,拟开发治疗实体瘤和血液系统恶性肿瘤。此次为该药在中国首次以1类新药获批临床,用于治疗非小细胞肺癌,目前该药正在海外开展1/2期临床研究。
- 07.第一三共:DS-1062a
DS-1062a(德达博妥单抗/Dato-DXd)是研发的一种以滋养细胞表面糖蛋白抗原2 (TROP2)为靶点的抗体-药物偶联药物(ADC),是第一三共重点推进的三大领先ADC项目之一,目前已在国内开展多项III期临床试验,适应症涉及乳腺癌、非小细胞肺癌、实体瘤等。
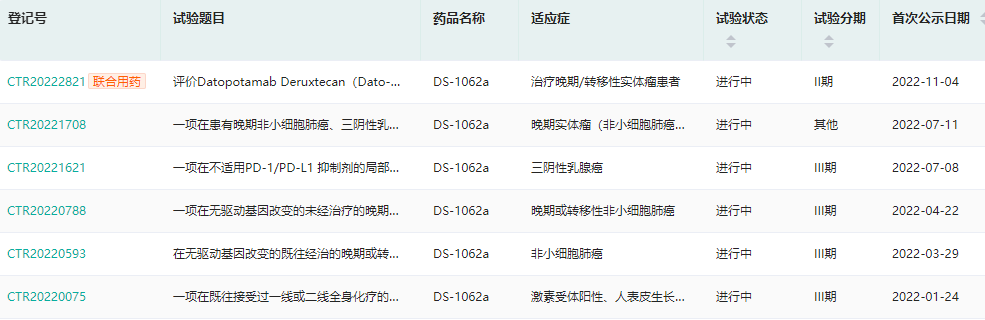
此次作为1类新药获批临床,联合帕博利珠单抗伴或不伴铂类化疗适用于无驱动基因改变的未经治疗的晚期或转移性PD-L1低表达(肿瘤比例评分TPS<50%)非鳞状非小细胞肺癌患者的治疗。
二、化药
本次1类新药获批临床的化药
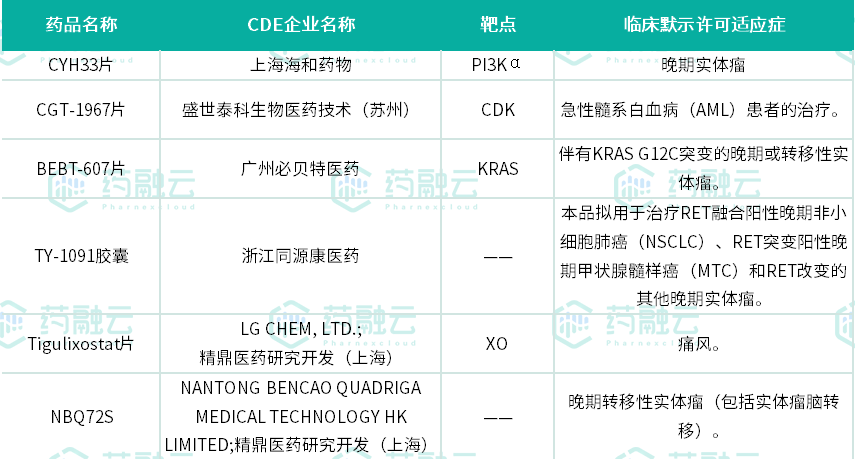
- 01.上海海和药物:CYH33片
CYH33是上海药物所与海和生物共同研究开发的一种新型、高效、特异性的PI3Kα抑制剂,通过抑制PI3K介导的信号通路,阻滞细胞于G1期,从而抑制肿瘤细胞增殖。
据药融云数据库,目前该药已在国内启动多项临床I期试验和1项II期临床试验,其中后者为一项评估CYH33(一种选择性PI3Kα抑制剂)在复发/持续性卵巢、输卵管或原发性腹膜透明细胞癌患者中的有效性和安全性的II期、开放性、多中心研究。
中国临床试验公示
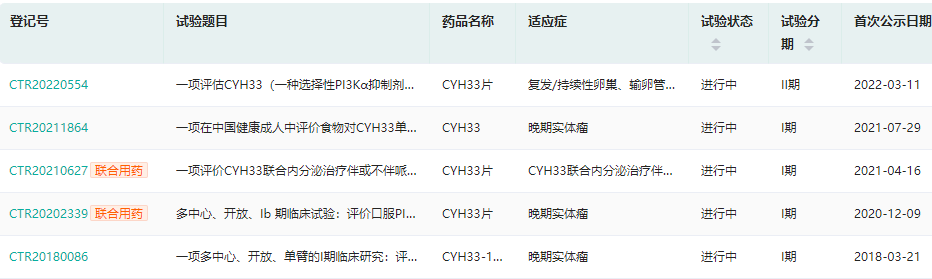
- 02.盛世泰科生物:CGT-1967片
CGT-1967片是CDK4/6抑制剂,拟用于治疗血液癌。盛世泰科指出,这是该公司2022年以来,在研1类新药获批临床的第三款。此外,盛世泰科在研的抗癌药物中,已有CGT-6321(FGFR/VEGFR双靶点抑制剂)、CGT-1881(CXCR4拮抗剂)和CGT-9475(ALK抑制剂)等3款药物进入临床。
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、申报审批情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

—END—


































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)



















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论