
“没有最贵,只有更贵”,这个俗语在医药界同样适用。今年8月,蓝鸟生物(bluebird bio, Inc. ,Nasdaq: BLUE)β-地中海贫血基因疗法Zynteglo(beti-cel)定价为280万,超过诺华的基因疗法Zolgensma(定价210万美元),成为了当时的“史上最贵药”(《FDA批准蓝鸟生物基因疗法!定价$280万,一跃成为“史上最贵药”》)。仅一个月时间,该公司第2款基因疗法SKYSONA®(elivaldogene autotemcel,eli-cel)近日获得美国FDA批准上市,超越了自己的Zynteglo疗法,定价为300万美元,刷新纪录,再次成为“全球史上最贵药物”!
SKYSONA®主要用于减缓4-17岁早期活动性脑肾上腺脑白质营养不良(CALD)男孩神经功能障碍的进展,蓝鸟生物还证实,此前对eli-cel临床开发项目的限制已被解除。该疗法由患者自身的干细胞制成,是美国第一种可用于CALD的药物。据药融云数据显示,蓝鸟生物该基因疗法最早于2021年7月16日首次全球面世,上市国家包括欧盟、挪威、冰岛等国家,获批适应症为肾上腺脑白质营养不良。
SKYSONA®各国研发现状

截图来源:药融云全球药物研发数据库
另外,SKYSONA®还获得了美国的突破性疗法、优先审评、罕见儿科疾病用药以及欧盟的加速批准、孤儿药、EMA优先药物、儿科用药研究计划的特殊审批。这些特殊审批都会获得各国审评审批机构加速审评的待遇,从而加快蓝鸟生物该基因疗法药物研发进程,更早解决病患未满足的临床需求。
SKYSONA®各国特殊审批情况
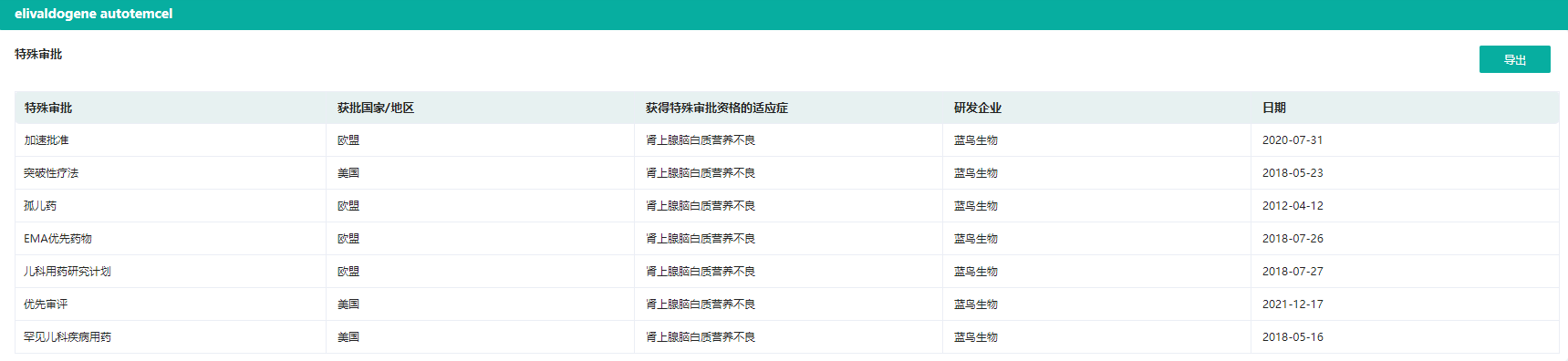
截图来源:药融云全球药物研发数据库
CALD是一种罕见的进行性神经退行性疾病,主要影响儿童早期的男孩(中位年龄为7岁),并导致不可逆转的破坏性神经功能衰退,包括主要功能障碍,例如交流丧失、皮质盲、需要管饲、完全失禁、轮椅依赖或完全丧失自愿运动。近半数未接受治疗的患者在症状出现后5年内死亡。在批准SKYSONA治疗之前,有效的选择仅限于同种异体造血干细胞移植(allo-HSCT),这与包括死亡在内的严重潜在并发症的风险有关,在没有人类白细胞抗原(HLA)匹配供体的患者中可能会急剧增加。
蓝鸟生物预计,该基因疗法的商业产品将在2022年底之前通过美国有限数量的合格治疗中心(QTC)提供,包括波士顿儿童医院和费城儿童医院,预计每年可以治疗10名患者。但该基因疗法也不是完全没有风险。在临床试验期间接受治疗的67名儿童中,有3名患上了血癌,研究人员认为这些血癌与基因治疗有关。波士顿儿童医院基因治疗项目的医学主任,其中一项临床试验的首席研究员Christine Duncan博士表示,这种风险是一个“真正令人担忧的问题”,但癌症是可以治疗的。“我仍然相信这项疗法对一些患者来说是一个不错的选择。”
美国FDA的批准附带了关于血癌风险的警告,以及需要每半年和每年进行一次测试来检测癌症的早期迹象;同时,蓝鸟生物在患者在接受治疗后,必须继续跟踪患者15年,以收集有关其长期安全性和有效性的数据。

蓝鸟生物该基因疗法的批准从患者角度来说,可以惠及罕见病患者,无疑是世界的福音;同时对蓝鸟生物而言,这也是一次关键胜利,在过去几年中,蓝鸟生物一直经历临床挫折、欧洲商业化失败的挫败,以及长期领导者的离职以及重大裁员。蓝鸟生物目前拥有约300名员工,比1月底减少了42%。从6月开始,2款基因疗法的积极消息帮助该公司的股票自6月份的低点以来翻了一番多,但自2018年高点以来仍下跌了94%以上。蓝鸟生物预计其现金和短期收入将在2024年上半年为公司带来收益。
除此之外,蓝鸟生物公司的研发管线其他项目如图所示。目前该公司对镰状细胞疾病的基因治疗处于临床研究阶段,没有得到美国FDA的批准,安全性和疗效尚未确定。
蓝鸟生物研发管线

截图来源:蓝鸟生物官网
注:† lovo-cel临床项目目前处于部分临床搁置状态,该项目涉及一名患有持续性非输血依赖性贫血的青少年患者(18岁以下),蓝鸟生物公司将继续与FDA合作解决部分搁置问题。
信息参考:
[1]蓝鸟生物官网 | https://www.bluebirdbio.com/
[2] 药融云数据库
想要解锁更多药企创新药信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、研发阶段、最新进展、申报获批情况、临床试验信息、销售情况与市场前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论