早在2019年8月2日,吡昔替尼(在美国以Turalio为商品名)已获得美国食品药品监督管理局(FDA)的批准,用于治疗存在严重发病率或功能限制且不适合手术的症状性TGCT成人患者。这一批准是基于一项关键III期临床试验——ENLIVEN研究的积极结果。
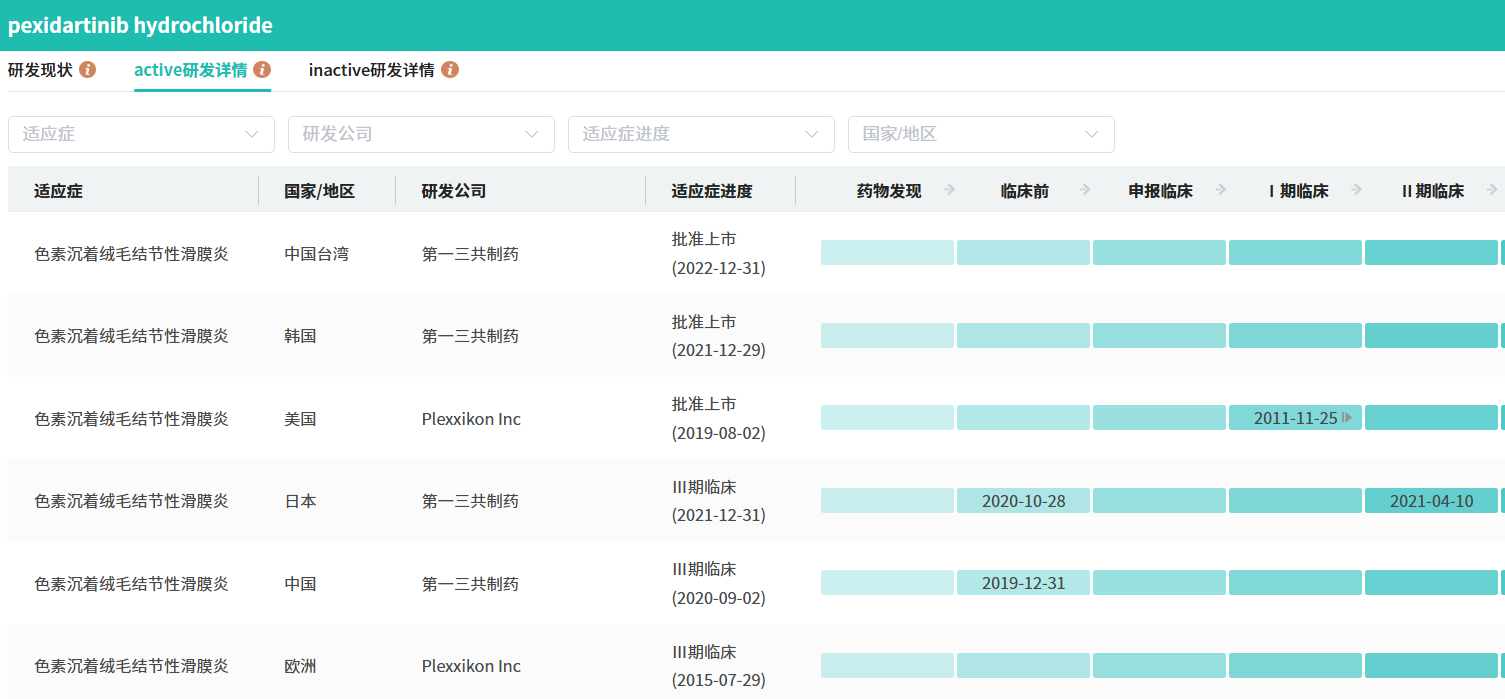
截图来源:摩熵医药全球药物研发数据库
ENLIVEN研究共入组了120例TGCT患者,他们被1:1随机分配至吡昔替尼治疗组(61例)和安慰剂组(59例)。研究的主要疗效终点是治疗25周后的总缓解率(ORR)。结果显示,吡昔替尼治疗组在治疗第25周的ORR高达39%,而安慰剂组则为0%,充分证明了吡昔替尼在TGCT治疗中的显著疗效。
腱鞘巨细胞瘤(TGCT),又称色素沉着绒毛结节性滑膜炎(PVNS)或腱鞘巨细胞瘤(GCT-TS),是一种罕见且通常非恶性的关节或腱鞘肿瘤。虽然多数TGCT呈良性,但它们会导致滑膜和肌腱鞘增厚或过度生长,对周围组织造成损害,严重影响患者的生活质量。手术一直是TGCT的主要治疗手段,但部分患者因病情严重或身体状况不佳而无法接受手术,即使手术后肿瘤也可能复发。
吡昔替尼的获批上市,将为中国TGCT患者提供一种全新的、非手术的治疗选择。这对于那些无法手术或手术后复发的患者来说,无疑是一个重大的福音。我们期待吡昔替尼能够尽快在国内上市,为更多TGCT患者带来希望和康复的可能。
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!











































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论