引言
CDE收审情况一览
12月20日-12月26日CDE共受理国产和进口临床/上市申请173个。其中,上市注册申请93个,临床试验申请80个。并有18个一致性评价受理号。在173个受理号中,1类药品最多占66个,2类药品15个,3类药品45个,4类药品42个,5类药品5个。(文中统计结果不包括补充申请&进口再注册)
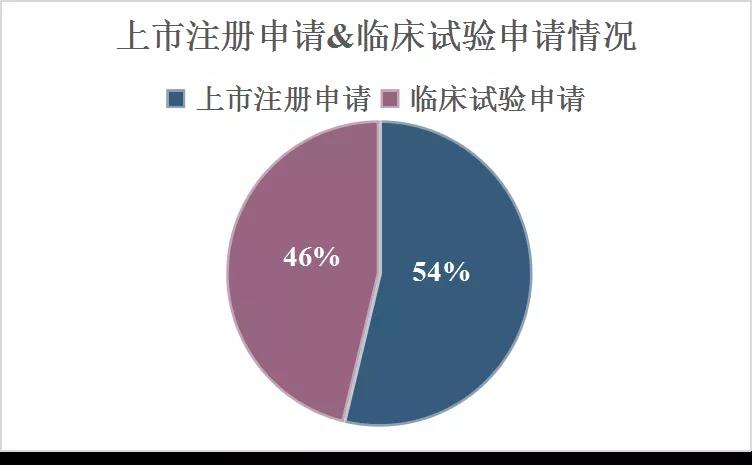
图1.上市注册申请&临床试验申请情况
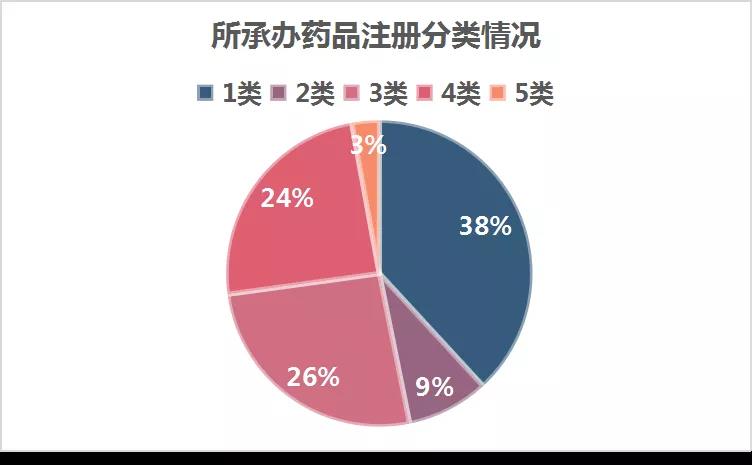
图2.所承办药品注册分类情况
注册分类:1类
创新药
1类新药受理号收审情况:
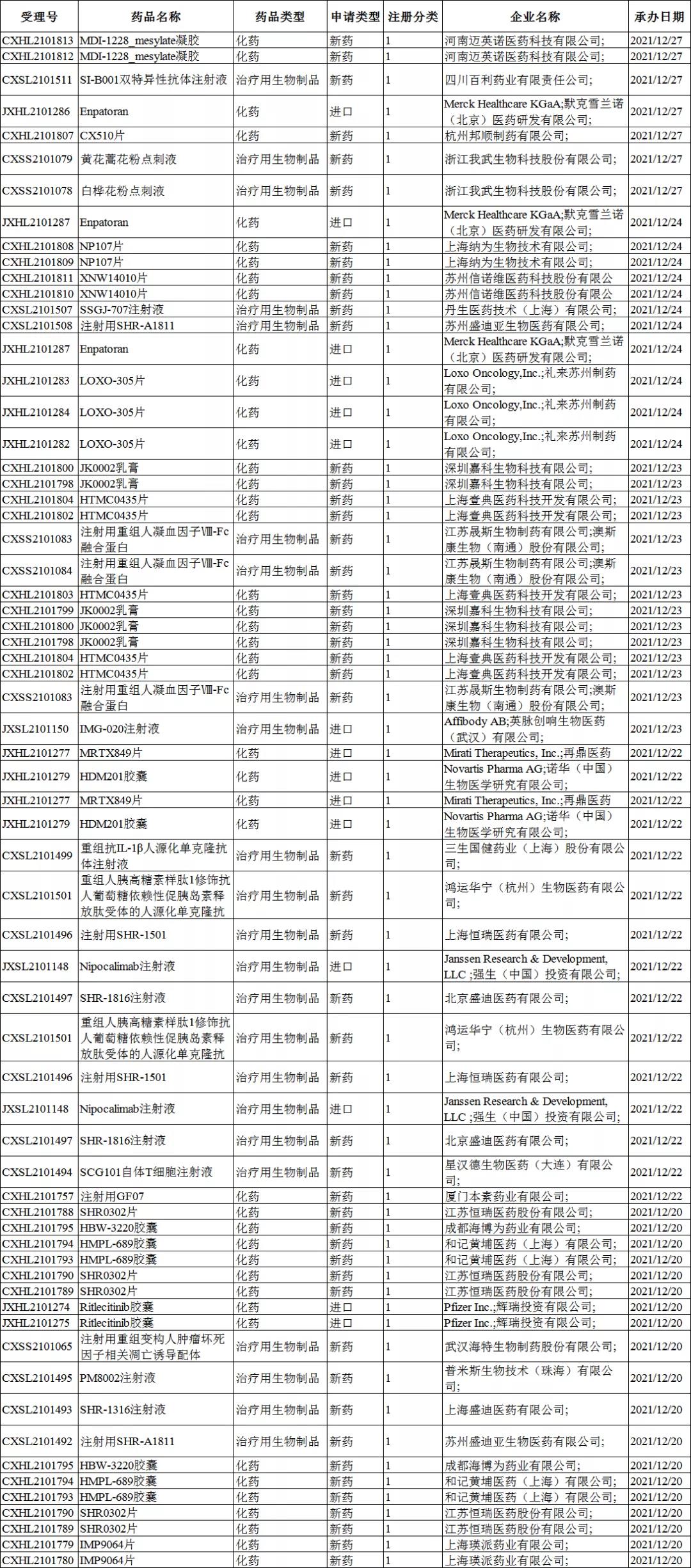
注
66个受理号中,包括化药受理号43个,生物制品受理号23个,无中药受理号。其中,恒瑞及其旗下子公司(苏州盛迪亚、上海恒瑞、上海盛迪、北京盛迪)共占12个受理号,所申报药品分别为:注射用SHR-A1811、注射用SHR-1501、SHR-1816注射液、SHR-1316注射液、SHR0302片。
注册分类:2类
改良型新药
2类新药受理号收审情况:
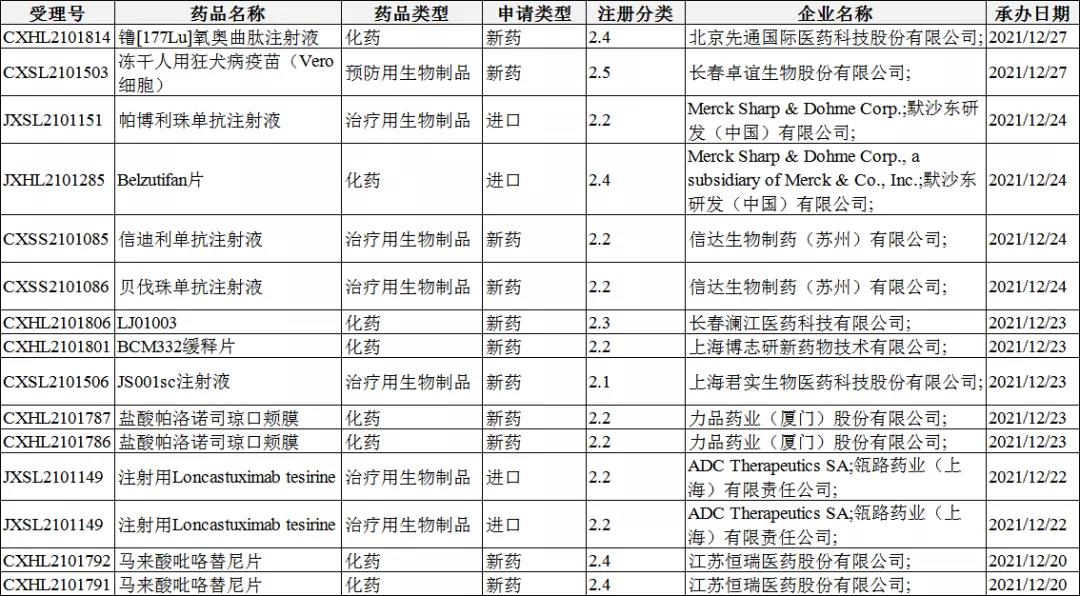
注
15个2类新药受理号包括了化药受理号8个,生物制品受理号7个,无中药受理号。其中包含了信达生物的2款单抗的上市注册申请(信迪利单抗注射液和贝伐珠单抗注射液)。
注册分类:3类
中药:古代经典名方中药复方制剂
生物制品:境内或境外已上市生物制品/疫苗
化药:境内申请人仿制境外上市但境内未上市原研药品的药品
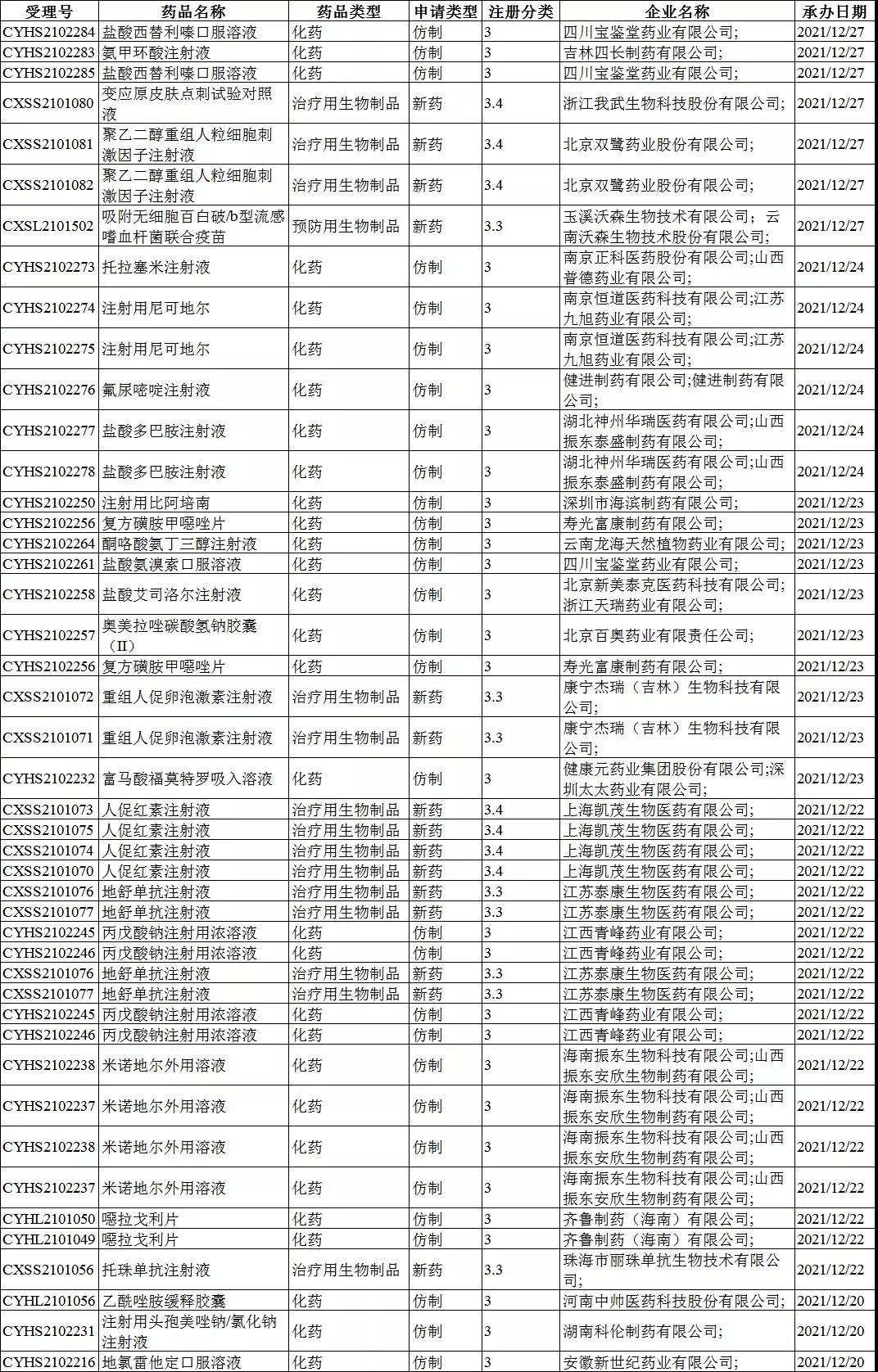
3类药品受理号收审情况:
注册分类:4类
中药:中药同名同方药
化药:境内申请人仿制已在境内上市原研药品的药品
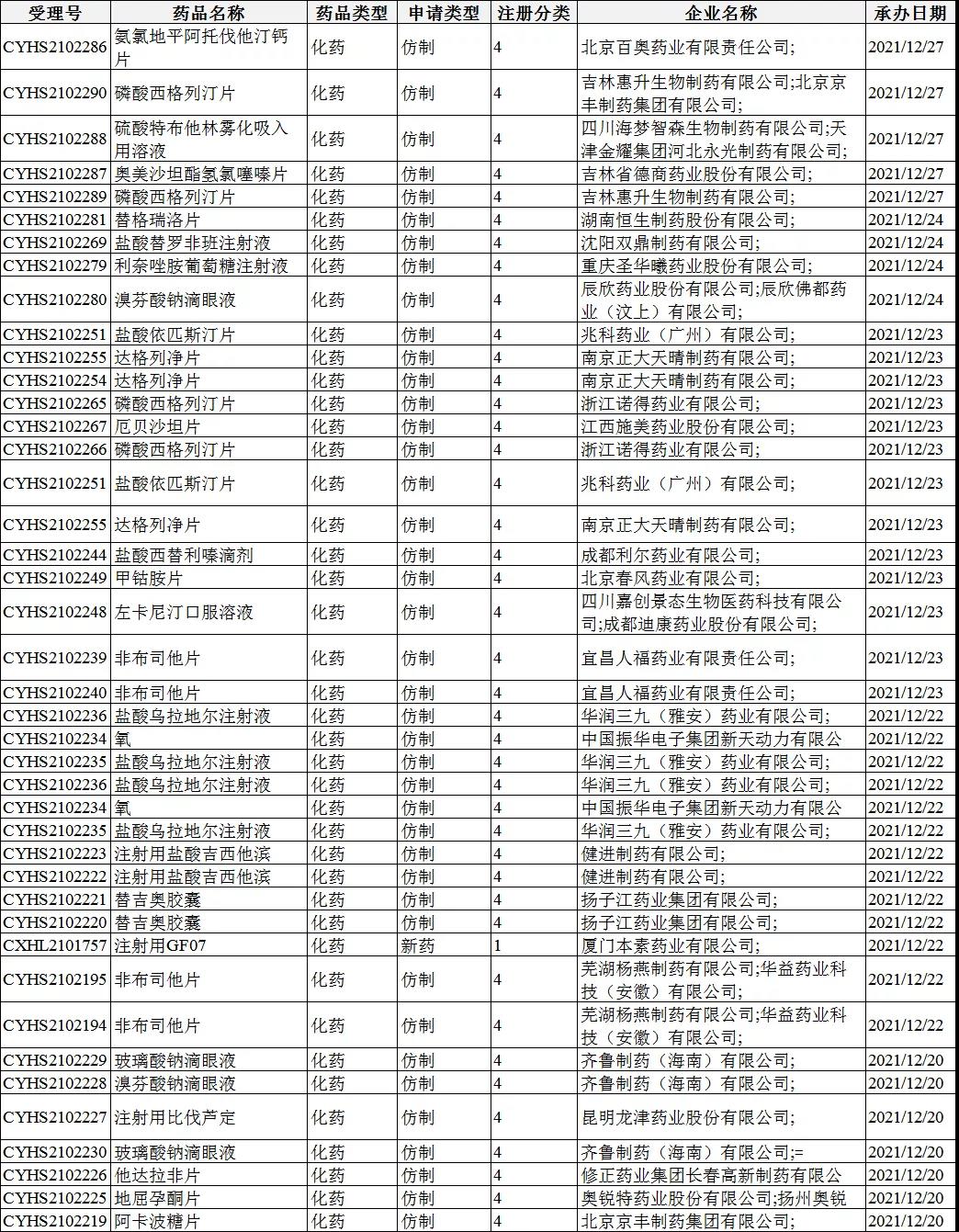
4类药品受理号收审情况:
注册分类:5类
境外已上市境内未上市化学药品
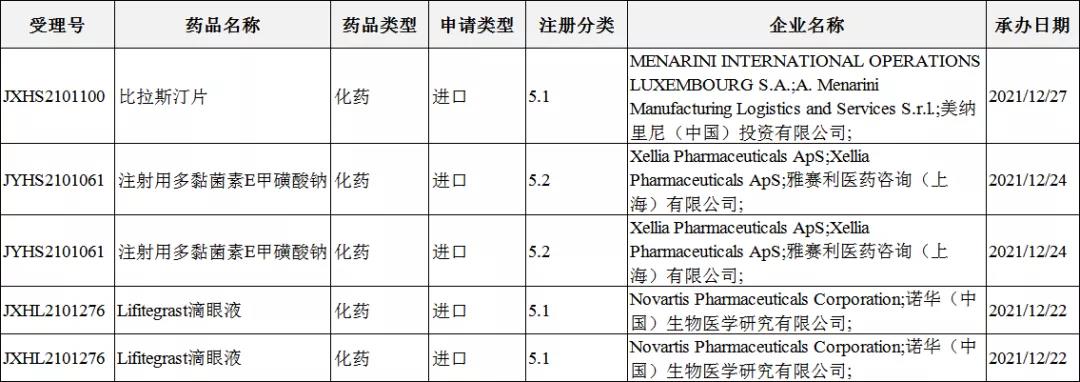
5类药品受理号收审情况:
一致性评价受理情况
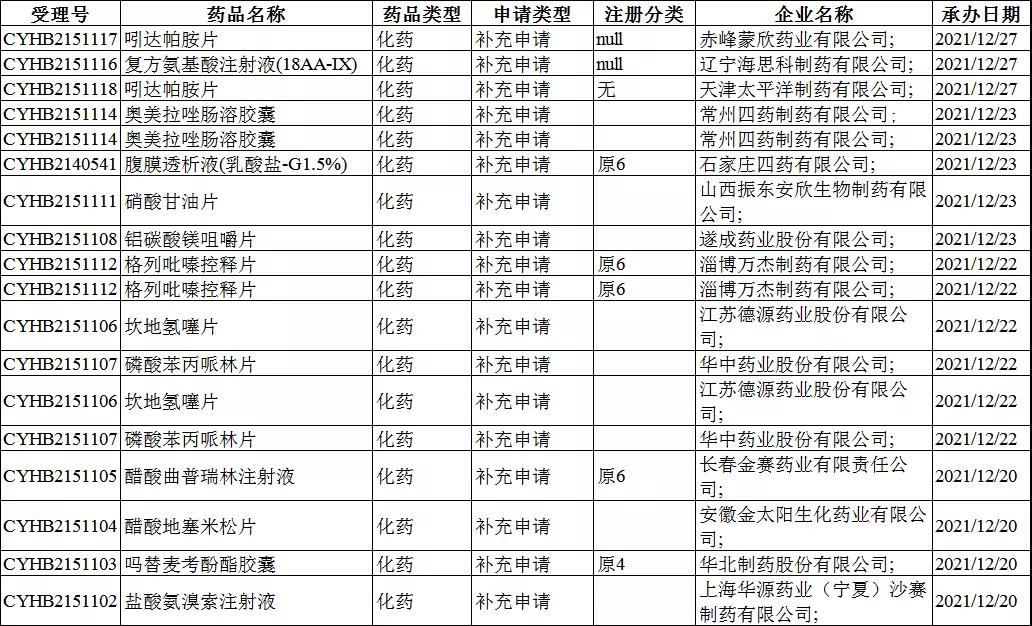
一致性评价受理情况:







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论