
引言:一周一见的CDE药品审评周报来了!本周CDE承办的各类药品数量都有降低,创新药承办25个,改良型创新药承办3个。唯一的上市注册申请为上海复宏汉霖关于PD-1单抗—斯鲁利单抗注射液的申请,该药为国内第七款获批上市的PD-1单抗,有望成为国产首款小细胞肺癌一线免疫治疗药物。详情见下(文中统计结果不包括补充申请&进口再注册)。
创新药承办情况
2022年4月11日-17日CDE共承办25个创新药受理号,其中包括了化药受理号16个,生物制品受理号8个,中药受理号1个 。此次的25个1类新药受理号均为临床试验申请。
化药创新药
此次申报的化学药分别为:MN-08片、HNC664胶囊、GFH018 片、NRT6003注射液、68Ga-HX01注射液、JDQ443片、HRS-7983片、安纳拉唑钠肠溶片、CK-3773274片、TT-01488片、KL340399注射液。
MN-08片:MN-08 为美金刚硝酸酯衍生物,是喜鹊医药旗下的一款阿尔茨海默症(Alzheimer's Disease, AD)1类创新化药。根据喜鹊医药官网披露信息,MN-08 具有独特的双重作用机理,既通过抑制 N-甲基-D-天冬氨酸 (NMDA) 受体进而抑制神经细胞钙离子超载,又能释放一氧化氮 (NO) 舒张脑血管,增加脑血流,对大脑神经细胞具有很好的保护和修复作用。
HNC664胶囊:HNC664胶囊是由恒诺康研发在GLPG1690基础上,通过药化设计改造而来的一个新型ATX抑制剂。根据恒诺康官网披露信息,HNC664已获得中、美临床试验批准,并已在美国完成Ⅰa期临床研究,将扩展其适应症至肿瘤。
GFH018片:根据劲方医药官网披露信息,GFH018为由劲方药业研发的一款TGF-β R1创新药,拟用于治疗晚期实体瘤治疗 。
NRT6003注射液:该药品为首次被承办,暂未查到该药相关信息。
68Ga-HX01注射液:该药品为首次被承办,暂未查到该药相关信息。
JDQ443片:JDQ443 是诺华开发的一款 KRAS G12C 抑制剂,拟开发治疗 KRAS G12C 突变的晚期实体瘤。
HRS-7983片:该药品为首次被承办,暂未查到该药相关信息。
安纳拉唑钠肠溶片:安纳拉唑钠肠溶片作为全新的PPI抑制剂,是一种消化性溃疡治疗药品,用于治疗十二指肠溃疡。
CK-3773274片:CK-3773274片是由Cytokinetics研发的一款心肌肌球蛋白变构抑制剂药品,可通过直接结合心肌肌球蛋白马达结构域和抑制肌球蛋白ATP酶,使马达处于稳定的非产力状态,从而减少每个心动周期中活性肌球蛋白产力横桥的数量,从而治疗在心肌过度收缩的疾病如肥厚性心肌病。
TT-01488片:TT-01488片为药捷安康开发的一款新型非共价的可逆BTK抑制剂,有望应用于多种复发性或难治性血液恶性肿瘤。
KL340399注射液:KL340399注射液是由科伦药业开发的具有自主知识产权、非环二核苷酸(CDN)类新一代小分子STING激动剂。
生物制品创新药
此次申报的生物制品分别为:LBL-007注射液、Relatlimab/Nivolumab固定剂量复方注射液、Tremelimumab、IBI363、注射用DNV3、ZLT-001注射液、TAA06注射液。
LBL-007注射液: LBL-007(抗LAG-3全人抗体注射液)是一种由维立志博自主研发的IgG4亚型全人源单克隆抗体。通过结合人LAG-3蛋白,进一步阻断LAG-3蛋白与其配体的结合,从而解除LAG-3对T细胞的抑制作用,使T细胞恢复免疫功能,起到对肿瘤生长的抑制作用。
Relatlimab/Nivolumab固定剂量复方注射液:Relatlimab是一种人源IgG4淋巴细胞激活基因3 ( LAG-3 ) 阻断抗体,纳武利尤单抗是一种程序性细胞死亡蛋白-1 (PD-1) 阻断抗体。两者均来自百时美施贵宝(BMS),此组合药品拟用于晚期黑色素瘤治疗。
Tremelimumab:Tremelimumab是一个抗CTLA-4单克隆抗体,可通过结合表达于活化的T淋巴细胞表面的CTLA-4蛋白,刺激机体免疫系统对肿瘤细胞发起攻击。
IBI363:IBI363是信达在研的一款免疫细胞因子药物。
注射用DNV3:注射用DNV3是时迈药业通过其具有自主知识产权的超大型全人源IGM抗体文库及抗体药物研发平台而开发的抗LAG-3单抗。
ZLT-001注射液:ZLT-001是一款针对实体肿瘤的免疫细胞药物。
TAA06注射液:TAA06注射液是博生吉自主开发的靶向B7-H3的CAR-T细胞注射液(研发代号:TAA06注射液),在临床前试验中取得了优越的药效学和安全性数据。
中药创新药
本次还有一款中药创新药被承办,为江苏正阳药业旗下的ZY002妇科凝胶。
创新药承办情况

改良型新药承办情况
2022年4月4日-10日CDE共承办3个改良型新药受理号,包括2个临床试验申请和一个上市注册申请。
唯一的上市注册申请为上海复宏汉霖关于斯鲁利单抗注射液的申请。斯鲁利单抗注射液为上海复宏汉霖旗下的一款PD-1抑制剂,在3月24号获批上市,成为国内第七款获批上市的PD-1单抗。获批适应症为:用于MSI-H实体瘤治疗。根据福星医药于4月11日发布的公告,截至 本公告日,以该新药为核心的 9 项联合疗法正在全球多个国家和地区开展临床试验。此次被承办适应症为:联合化疗一线治疗局部晚期或转移性鳞状非小细胞肺癌以及该新药联 合卡铂和依托泊苷一线治疗既往未经治疗的广泛期小细胞肺癌(ES-SCLC)。
改良型新药承办情况

仿制药承办情况
注册分类:3类
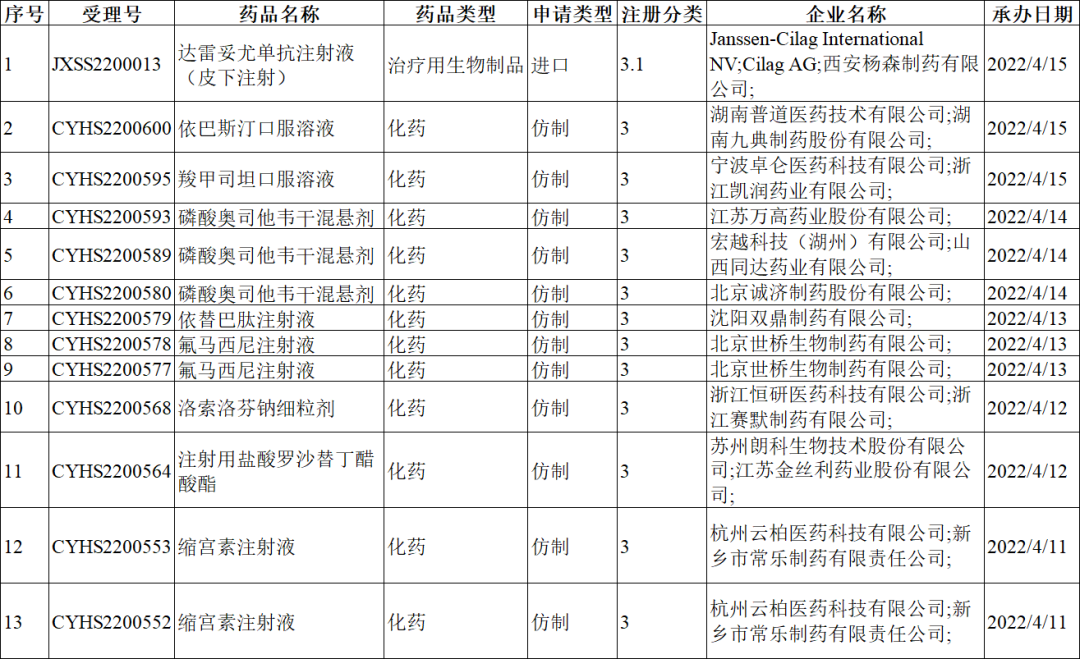
注册分类:4类
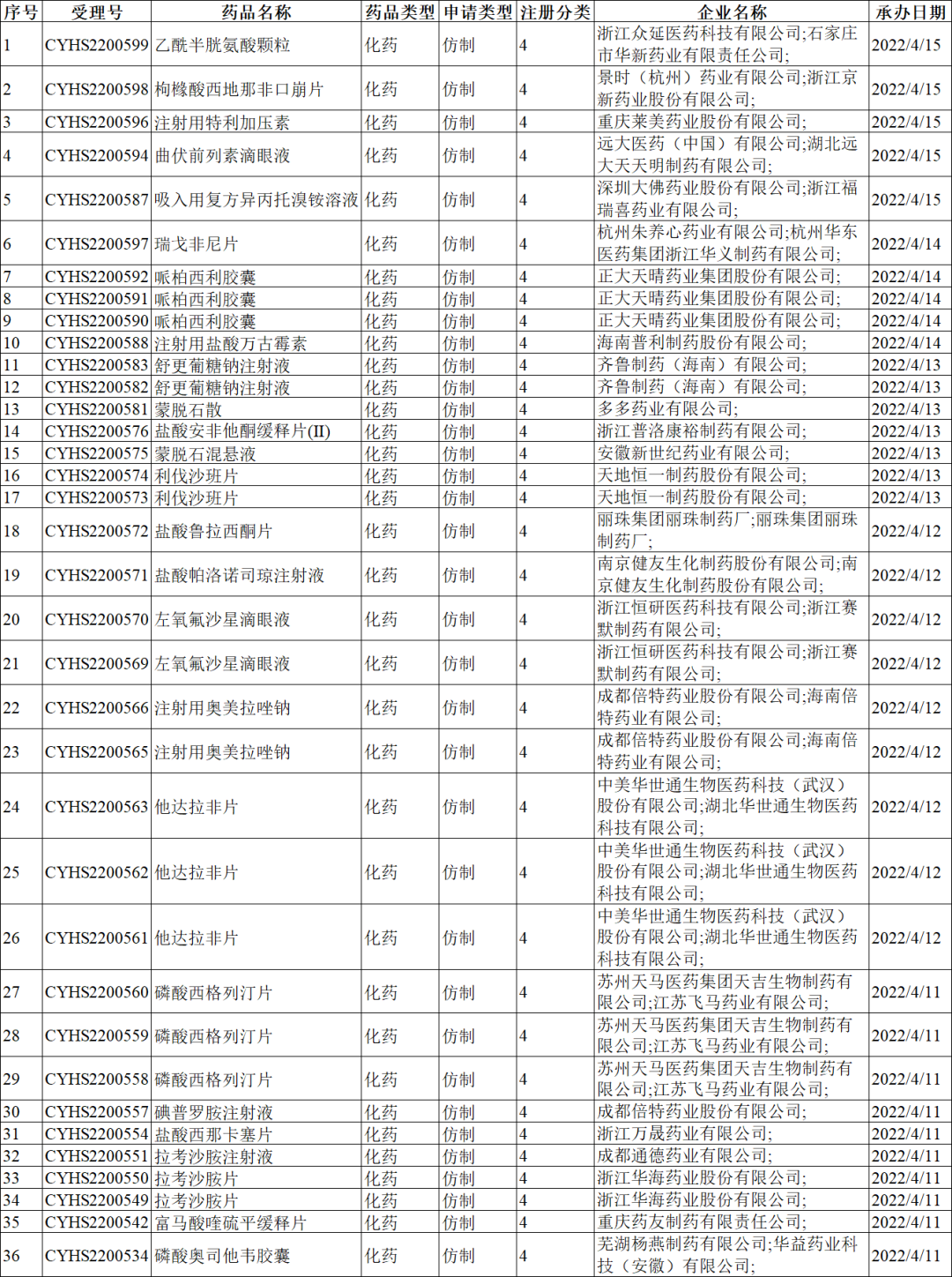
注册分类:5类
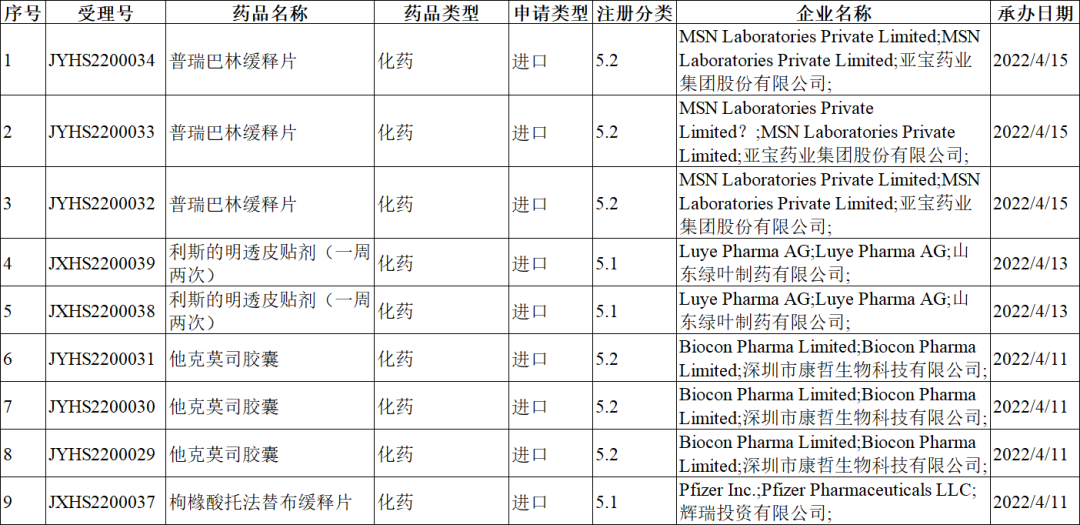
想要解锁更多药品审评最新信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企产品布局、药品申报情况、最新进展、药物涉及靶点适应症等信息,可否投入研发与仿制!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论