一、8月中国临床试验进展要点
- 8月CDE新公示临床试验共计296项,生物制品81项,中药/天然药物5项,化学药物共计210项,化药占71%
- 试验药物品种中,恩格列净片和Efgartigimod注射液成最热登记品种
- 从临床分期来看,临床I期69项,临床II期42项,临床III期40项,临床IV期5项,大多数试验处于临床早期阶段
- 从试验状态来看,293项正在进行中,3项试验已完成,均为BE试验
- 新公示BE试验126项,较上月(135项)下降6%。浙江诺得药业以4项试验占据BE试验申办单位榜首
- 新公示进口及国内新药152项,礼来、阿斯利康、罗氏等多家企业相关药物处于临床后期
- 江苏恒瑞、再鼎医药、正大天晴、ARGENX和PATHEON ITALIA以7项登记试验位居第一。苏州大学第一附属医院以9项登记试验高居榜首
数据统计时间段为2021年8月1日-2021年8月31日,药融云将定期统计新公示的临床试验信息,关注公众号即可定期查看。如有疏漏,欢迎指正!
8月公示296项试验,化药占71%,恩格列净片和Efgartigimod注射液成最热登记品种
2021年8月1日至8月31日,CDE新公示临床试验共计296项。从药品类型来看,生物制品81项,中药/天然药物5项,化学药物共计210项,占试验总数的71%,其中包括BE试验125项。
8月新公示临床试验药品分类
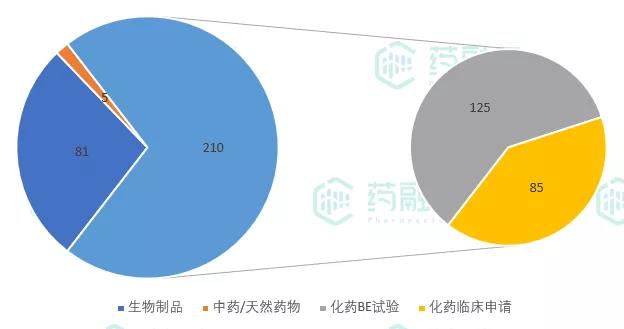
数据来源:药融云中国临床试验数据库
CDE新公示的临床试验药物品种中,共有26个登记试验数≥2的药物品种,其中16项为BE试验品种,恩格列净片和Efgartigimod注射液以4个登记试验位居前列。
登记试验数≥3的药物品种
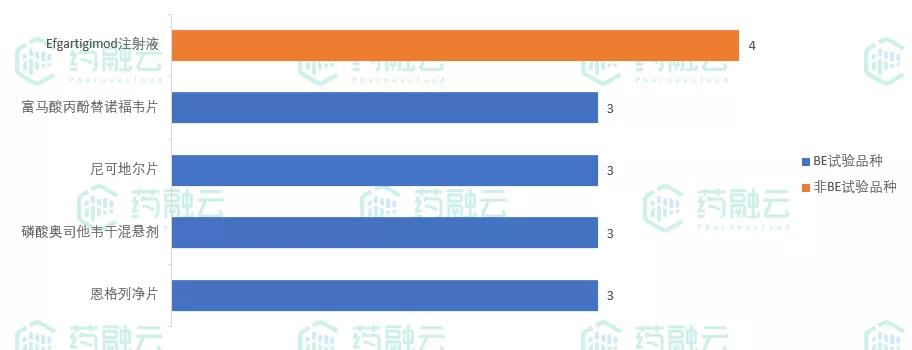
数据来源:药融云中国临床试验数据库
大多数试验处于临床早期,3项BE试验已完成
从临床分期来看,临床I期69项,临床II期42项(含I/II期),临床III期40项(含II/III期、I/II/III期), 临床IV期5项,其他试验140项(主要是BE试验)。
8月新公示临床试验分期
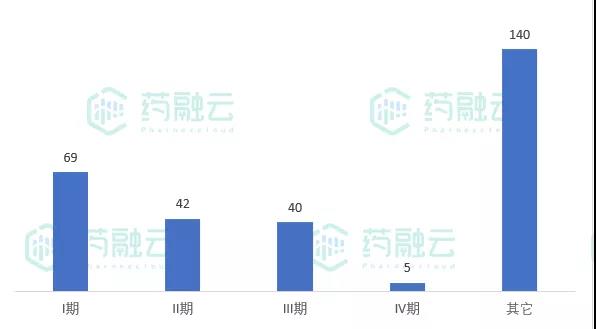
数据来源:药融云中国临床试验数据库
新公示的296项临床试验中,293项正在进行中,3项试验已完成,均为BE试验,涉及浙江华海药业、杭州中美华东制药和河南福森药业。
8月新公示临床试验状态
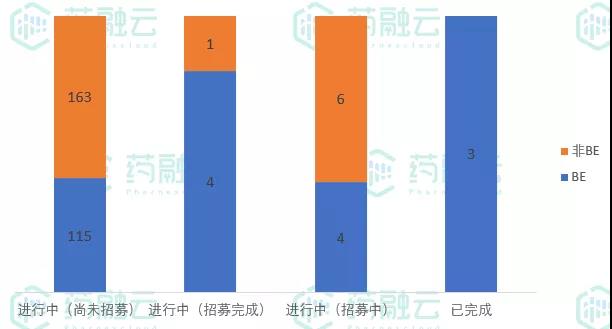
数据来源:药融云中国临床试验数据库
BE试验数较上月下降6%, 多家企业申报3项以上BE试验
8月新公示BE试验126项,较上月(135项)下降6%。浙江诺得药业以4项试验占据BE试验申办单位榜首。
8月新公示BE试验汇总
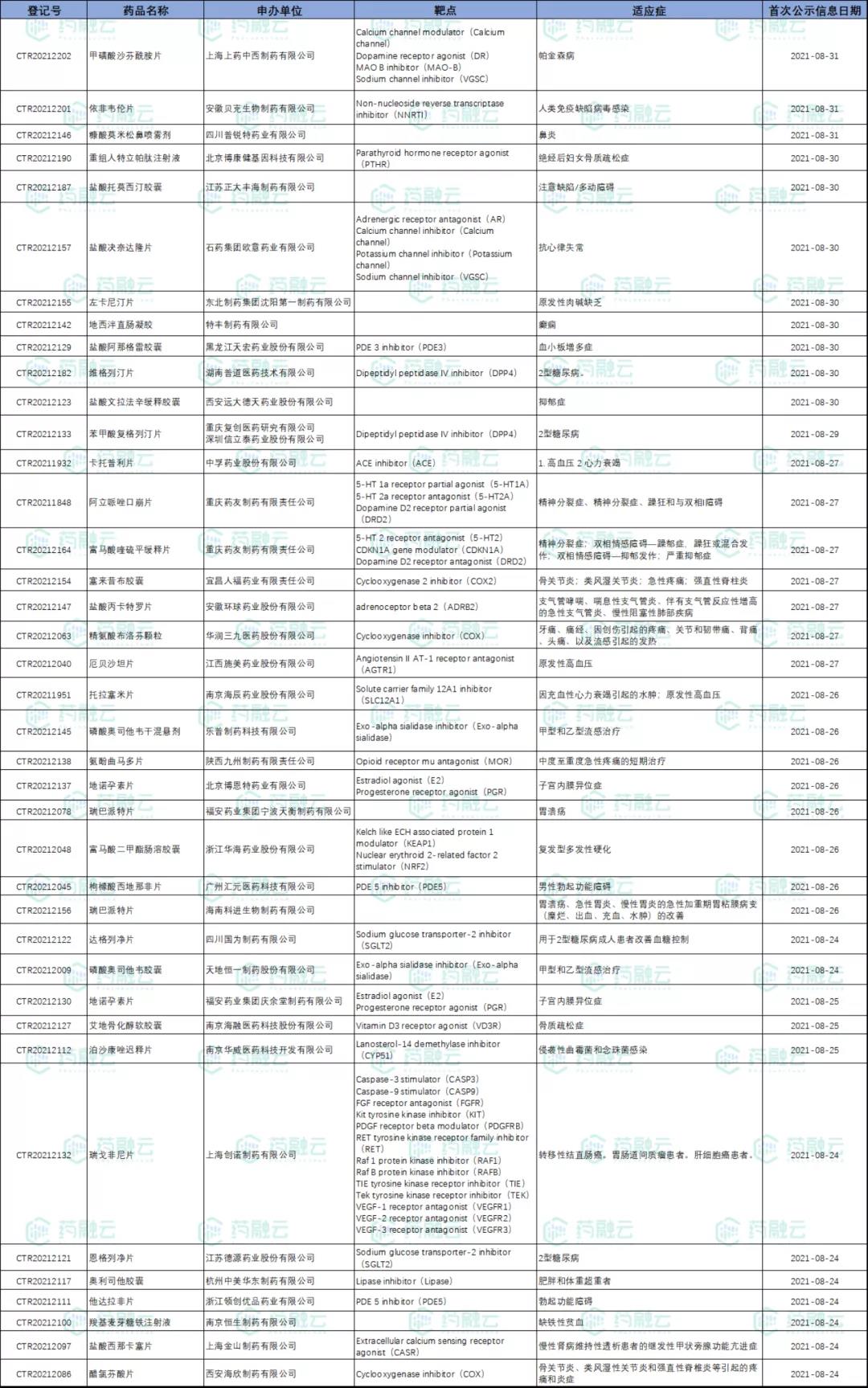
数据来源:药融云中国临床试验数据库
BE试验登记数≥3的申办单位

数据来源:药融云中国临床试验数据库
新公示进口及国内新药152项,诺华、阿斯利康、罗氏等多家企业相关药物处于临床后期
8月新公示进口药试验40项,其中24项试验进入临床III期或IV期,涉及礼来、阿斯利康、罗氏等多个企业;国内新药试验112项,涉及实体瘤、非小细胞肺癌、糖尿病等多个适应症,相比进口药,国内新药仅12.5%的药物进入临床后期。
8月新公示进口药试验
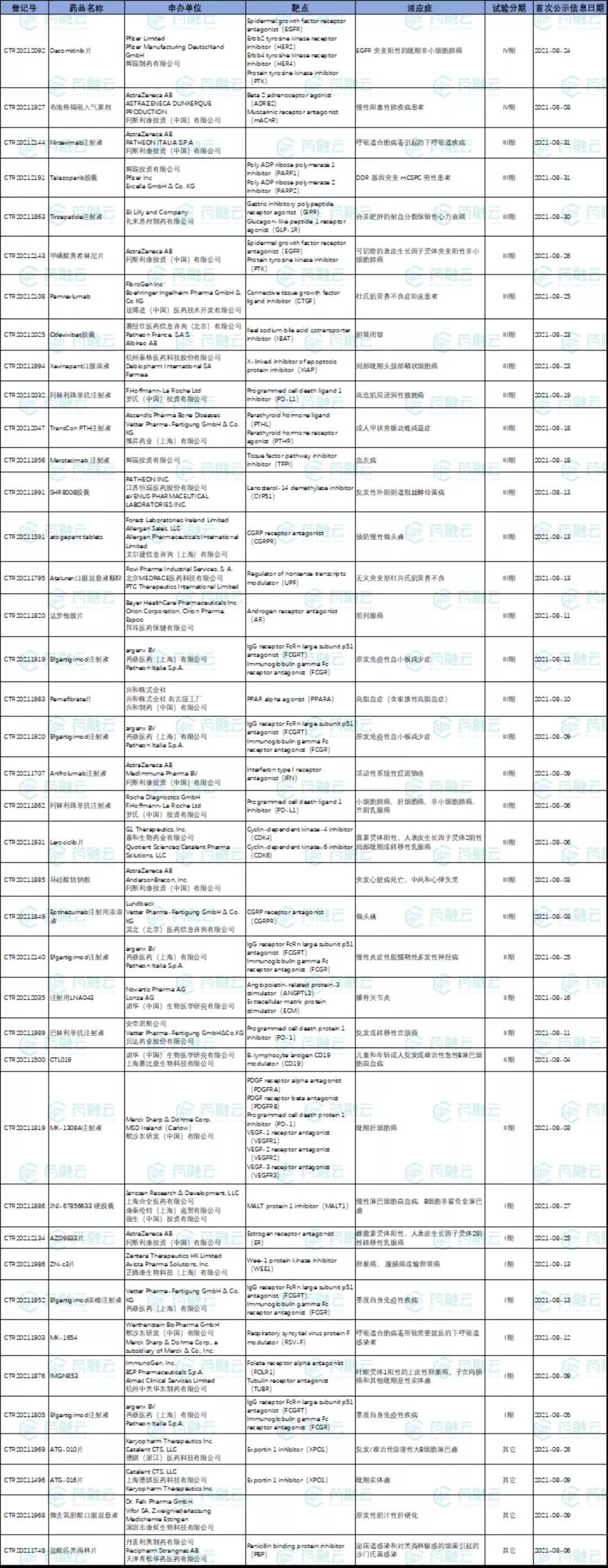
数据来源:药融云中国临床试验数据库
8月新公示国内新药试验
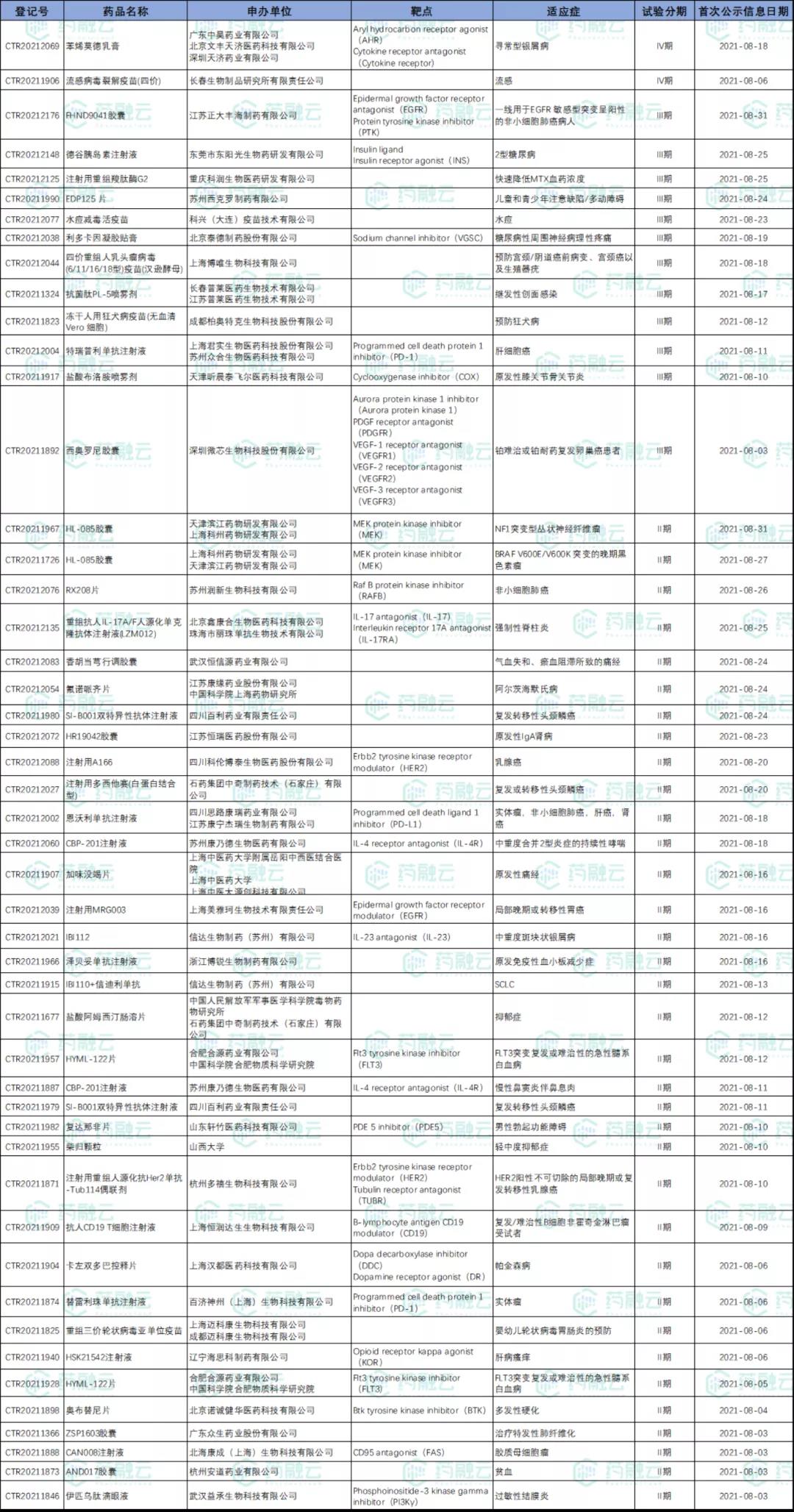
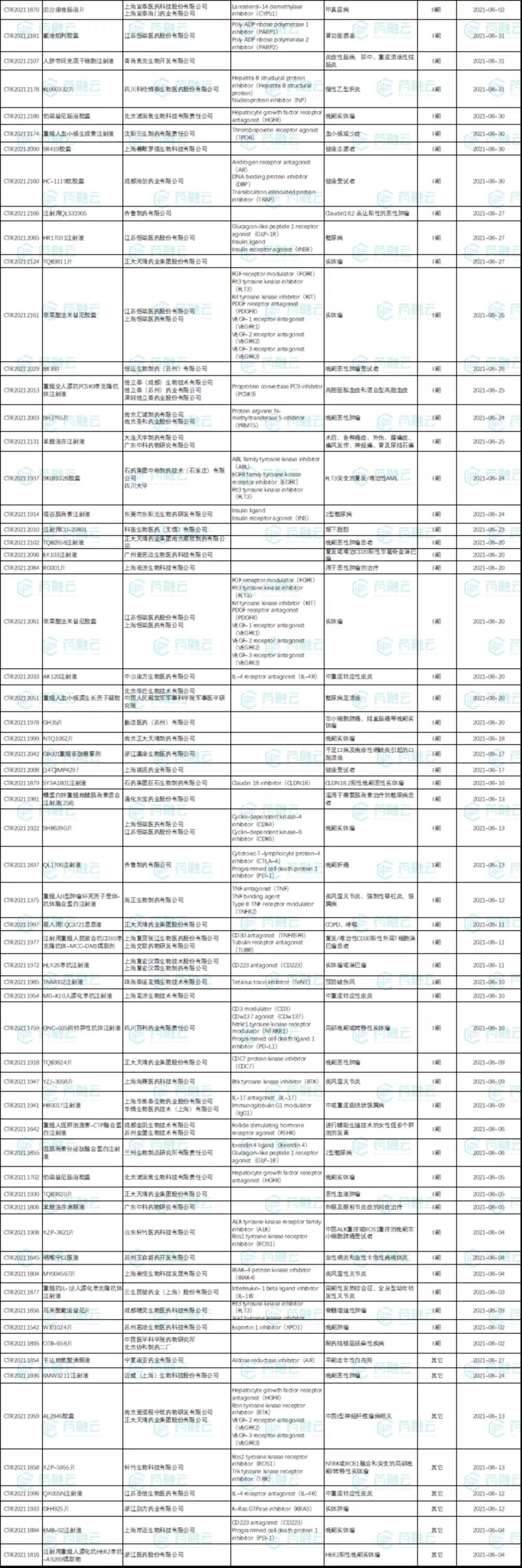
数据来源:药融云中国临床试验数据库
6款重点新药介绍,涉及辉瑞、礼来、泰格医药、恒瑞等多家企业
Talazoparib胶囊
申办药企:辉瑞
BRCA是一种抑癌基因,在调节细胞复制、DNA损伤修复、细胞正常生长有重要作用。由于BRCA基因的突变导致肿瘤细胞的DNA损伤修复机制出现缺陷,一旦肿瘤细胞的其它DNA修复机制受到抑制,会导致它们由于过多DNA损伤无法修复而死亡。基于这一原理开发的PARP抑制剂,可以通过抑制细胞内的另一DNA损伤修复通路,在杀伤携带BRCA基因突变的肿瘤细胞的同时,避免对健康细胞的伤害。BRCA突变类型众多,且与很多癌症的发生都有关系,包括乳腺癌、卵巢癌、前列腺癌等。
talazoparib是由辉瑞研发的,继奥拉帕尼、卢卡帕尼和尼拉帕尼之后,第四款获批上市的PARP抑制剂。临床前研究表明,talazoparib具有高效力且具有双重作用机制,有潜力通过阻断PARP酶活性,并将PARP捕获在DNA损伤部位,来诱导肿瘤细胞死亡。Talazoparib治疗乳腺癌的疗效在临床试验中得到了证实。
Tirzepatide注射液
申报企业:礼来
Tirzepatide是礼来开发的一种胃抑制多肽(GIP)/胰高血糖素样肽-1(GLP-1)受体双重激动剂。目前该药已经在中国获批3项临床试验,分别为:1)2型糖尿病;2)超重或肥胖患者的长期体重管理;3)2型糖尿病合并高危心血管风险。另外,Tirzepatide还对非酒精性脂肪性肝炎显示出一定的治疗潜力。著名投资机构EvaluatePharma在2019年的报告中将其列为了最具投资价值的项目之一。
Xevinapant口服溶液
申报企业:泰格医药
Xevinapant 口服溶液是泰格医药与 Debiopharm International SA 联合开发的一种凋亡抑制蛋白(IAP)抗拮剂。IAP 是细胞凋亡的重要调控因子,与细胞的有丝分裂,恶性肿瘤抑制等有关。可以通过促进细胞凋亡和改善肿瘤免疫反应,让肿瘤细胞对化学放射疗法更为敏感。其与CRT联用的治疗方案,已在多种癌症类型中显示一定效果。
SHR8008胶囊
申报企业:恒瑞
SHR8008是一种新型口服唑类抗真菌药物,最初由Mycovia公司研发,在抑制真菌CYP51酶方面显著优于常用唑类抗真菌药。2019年,恒瑞医药斥资1.1.亿美元引进该产品,并获得了该化合物在中国的临床开发、注册、生产和市场销售的独家权利。临床试验显示,SHR8008在多个研究人群中都显示出良好的安全性和耐受性。
从II期临床研究的结果来看,SHR8008可以有效治疗急性VVC发作。基于以上结果,恒瑞医药拟在国内开展SHR8008治疗急性外阴阴道假丝酵母菌病的III期临床研究,进一步评价SHR8008胶囊治疗急性VVC的有效性和安全性,为急性VVC患者的治疗提供更多的临床选择。
Efgartigimod注射液
申报企业:再鼎医药
efgartigimod是一款靶向FcRn的“first-in-class”疗法。2021年1月,再鼎医药通过一项高达1.75亿美元的合作从argenx公司获得了该候选药在大中华区(包括中国大陆、香港、澳门和台湾地区)的独家权益。据悉,efgartigimod正在全球范围内开展多项临床研究,涉及的适应症包括重症肌无力、寻常性天疱疮、免疫性血小板减少症、慢性炎症性脱髓鞘性多发性神经病等等。其中,efgartigimod在治疗抗乙酰胆碱受体抗体阳性全身性重症肌无力(gMG)患者的关键性3期临床试验ADAPT中,已达到了主要研究终点。
酒石酸阿福特罗雾化吸入溶液
申报企业:正大天晴
酒石酸阿福特罗雾化吸入溶液一种长效β2受体激动剂,原研厂家为Sunovion制药,最早于2006年获得FDA批准,用于治疗慢性阻塞性肺病(COPD),商品名为Brovana 。2017年,Brovana销售额大约为3亿美元。目前,酒石酸阿福特罗雾化吸入用溶液已被国家纳入第2批鼓励仿制药目录,申报企业有正大天晴、北京嘉林药业和江苏长泰药业3家,其中,天晴(新3类)和长泰(新3类)已进入上市申报阶段,北京嘉林仍处于临床阶段。
多家公司以7项试验并列临床试验申办单位榜首,苏州大学第一附属医院成最热试验机构
临床试验申办单位中,江苏恒瑞、再鼎医药、正大天晴、ARGENX和PATHEON ITALIA以7项登记试验位居第一。临床试验机构中,苏州大学第一附属医院以9项登记试验高居榜首。
8月临床试验登记数≥4的申办单位

数据来源:药融云中国临床试验数据库
8月临床试验登记数≥5的试验机构








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论