本周中国药品审评审批进展要点
1、2021.07.01-202107.08期间药审中心受理总量为307个,涉及品种202个
2、22个1类新药申请临床获CDE受理
3、新增25个按仿制药质量和疗效一致性评价品种申报的受理号
4、26个品种通过(含视同通过)一致性评价
5、3款国产新药获批上市:中国首款注射用左亚叶酸获批
数据统计时间段为2021年7月1日-2021年7月8日,药融云将定期公示中国药品审评审批信息,关注我们即可定期查看。如有疏漏,欢迎指正!
2021年7月1日至7月8日期间,共有3款国产新药、5款进口药获批上市;另有26个品种通过(含视同通过)一致性评价。有秦皇岛爱晖药业「盐酸美金刚口服溶液」等2款首仿获批上市,中国首款汇伦医药「注射用左亚叶酸钠」重磅获批,具体信息如下:
3款国产新药获批
汇伦医药旗下「注射用左亚叶酸钠」获批上市,用于叶酸拮抗剂(例如甲氨蝶呤)化疗、过量时使用,以减轻其毒性、抵消其作用;以及用于化疗中,与氟尿嘧啶类药物联用治疗胃癌和结直肠癌患者。
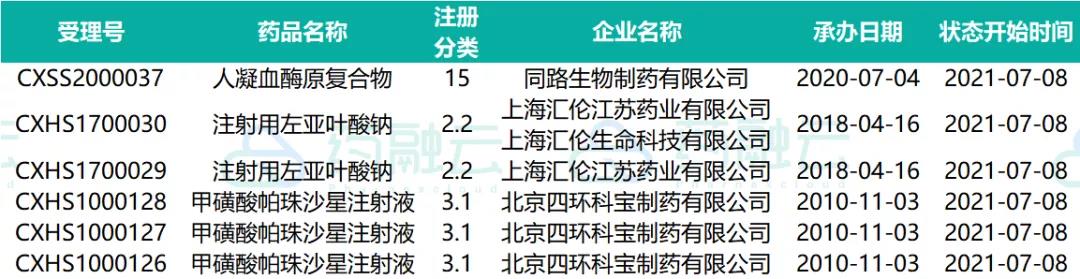
亚叶酸是叶酸还原型的甲酰化衍生物,系叶酸在体内的活化形式。目前中国已有多家公司的注射用左亚叶酸钙获批上市,但尚未有注射用左亚叶酸钠产品获批。此次上海汇伦江苏药业为中国首家获批注射用左亚叶酸钠的公司。
5个品种批准进口

过评品种信息
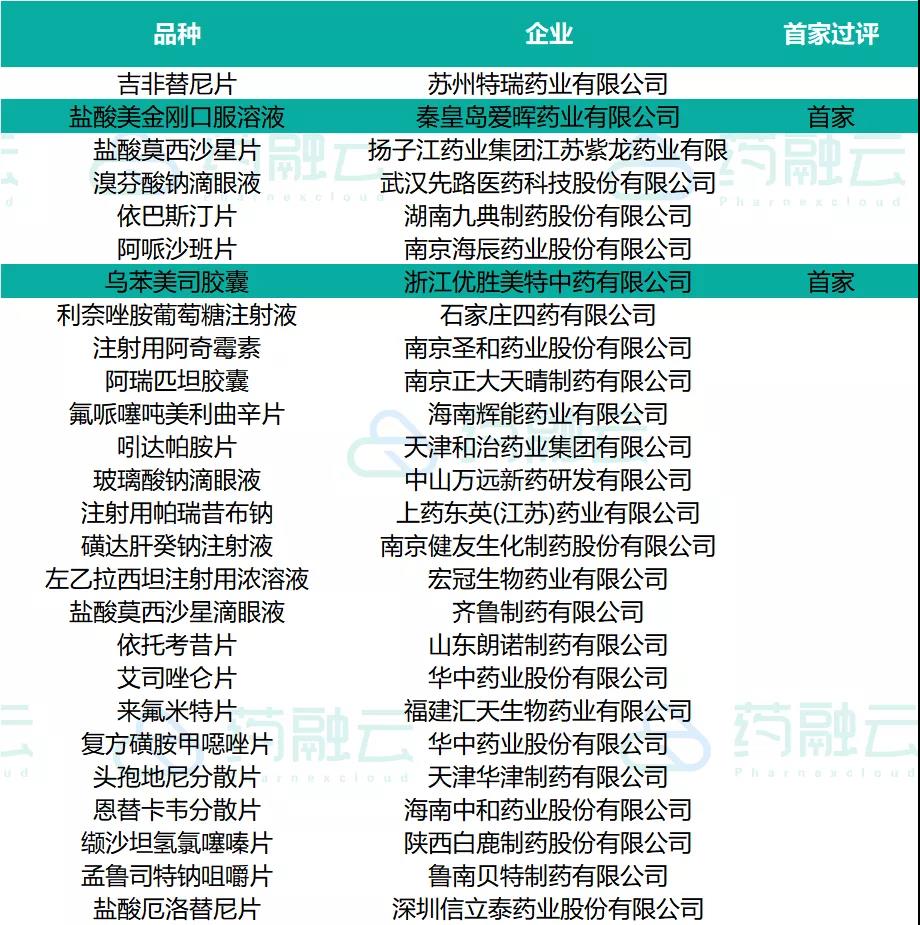
在审评审批阶段
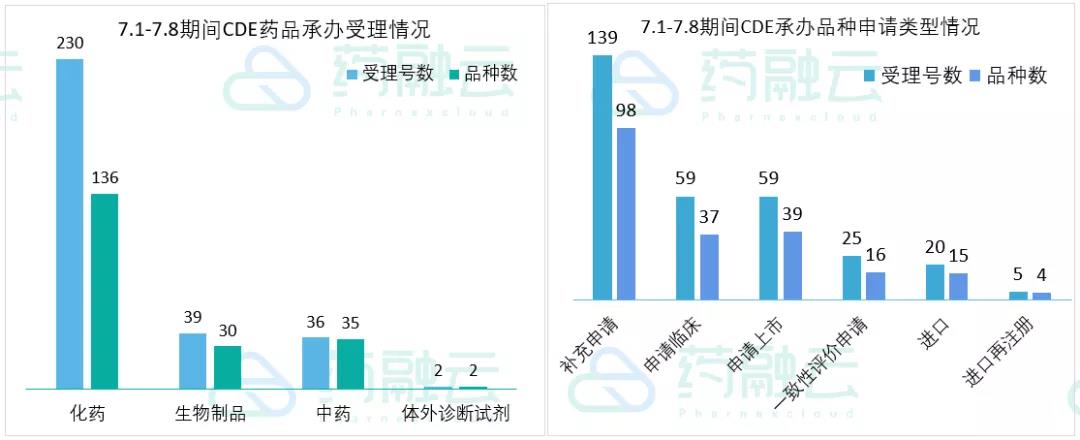
根据药融云中国药品审评数据,7月1号-7月8号期间共202个(按品种计,下同)药品获CDE承办,包括化药136个,生物制品30个,中药35个,以及体外诊断试剂2个。
近期CDE承办的共有37个品种申报临床,其中包括29款国产新药,另有16个品种提交一致性评价。
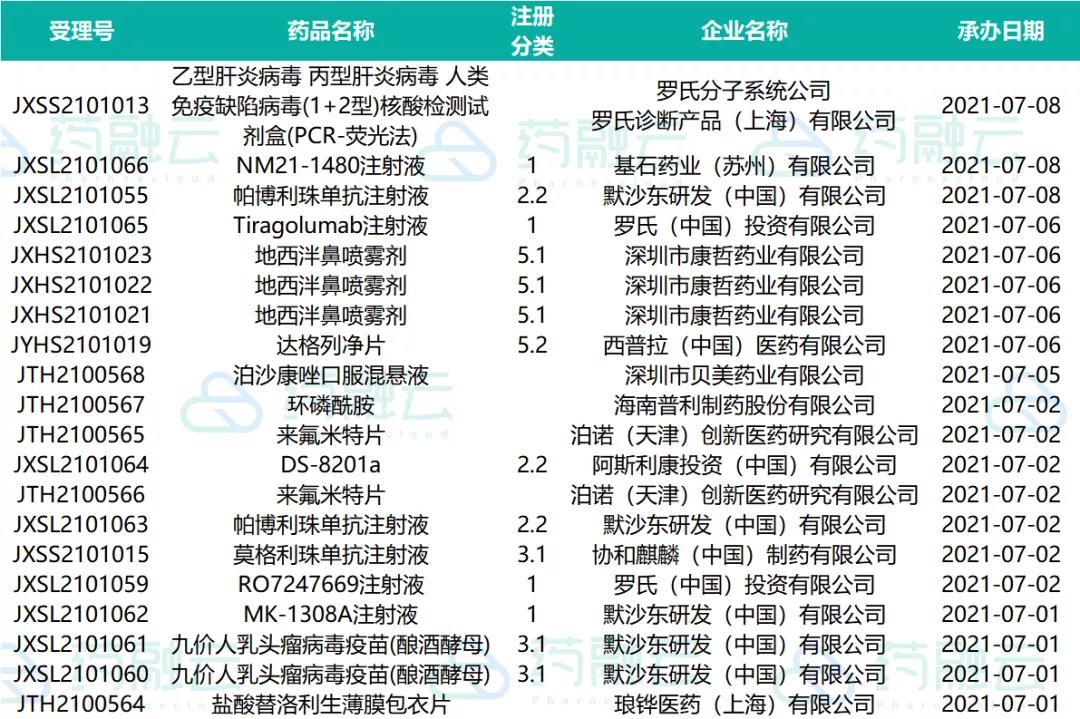
近期受理国产新药共计48个受理号,涉及36个品种38家企业,其中人福医药的注射用苯磺酸瑞马唑仑和博雅生物制药的人凝血因子Ⅷ等7款药品提交上市申请,其余均为申请临床,这其中包括25款1类新药。
07.01-07.08申请上市的药物情况

注射用苯磺酸瑞马唑仑为宜昌人福研发的1类新药,2020年7月首次上市,用于常规胃镜检查的镇静。此次申报为新增适应症,目前本品已完成麻醉诱导与维持的三期临床,用于治疗或诊断性操作时的镇静的三期临床正在进行中。
07.01-07.08申请临床的新药药物情况
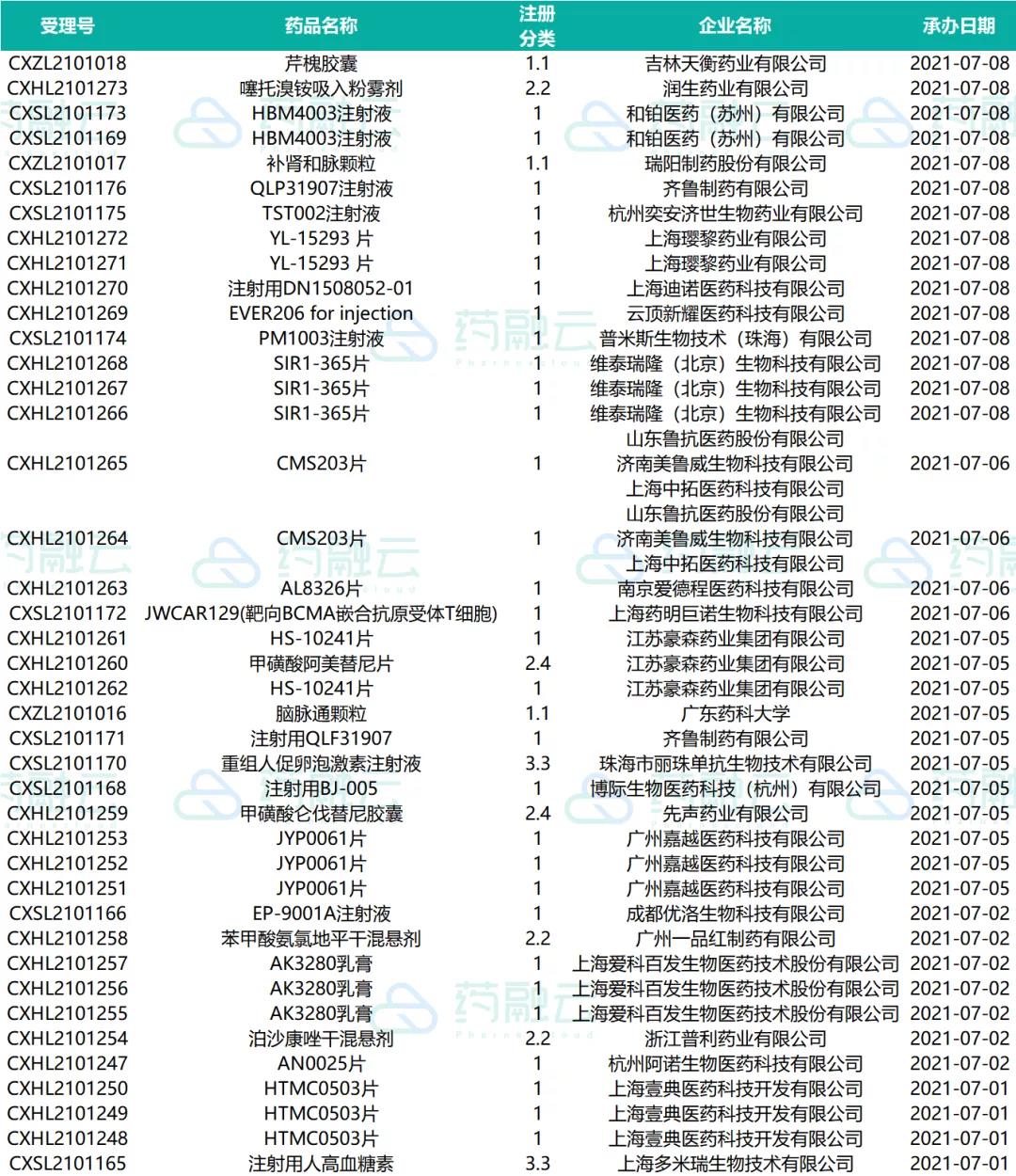
07.01-07.08申请临床的进口药物情况

07.01-07.08申请进口的进口药药物情况
在审批阶段
近期共有12个品种(22个受理号)进入审批阶段。
07.01-07.08在审批阶段药物情况

制证完毕-待发批件
近期共计38个品种(涉及受理号59个)制证完毕-待发批件。其中有7个品种通过一致性评价。下表是处于制证完毕-待发批件的过评药物情况。
07.01-07.08制证完毕-待发批件过评药物情况

已发件药物情况
近期共计127个品种(涉及受理号193个)已发件,其中有9个品种通过一致性评价,17个品种视同通过一致性评价。下表是已发件过评药物情况。
07.01-07.08已发件过评药物情况 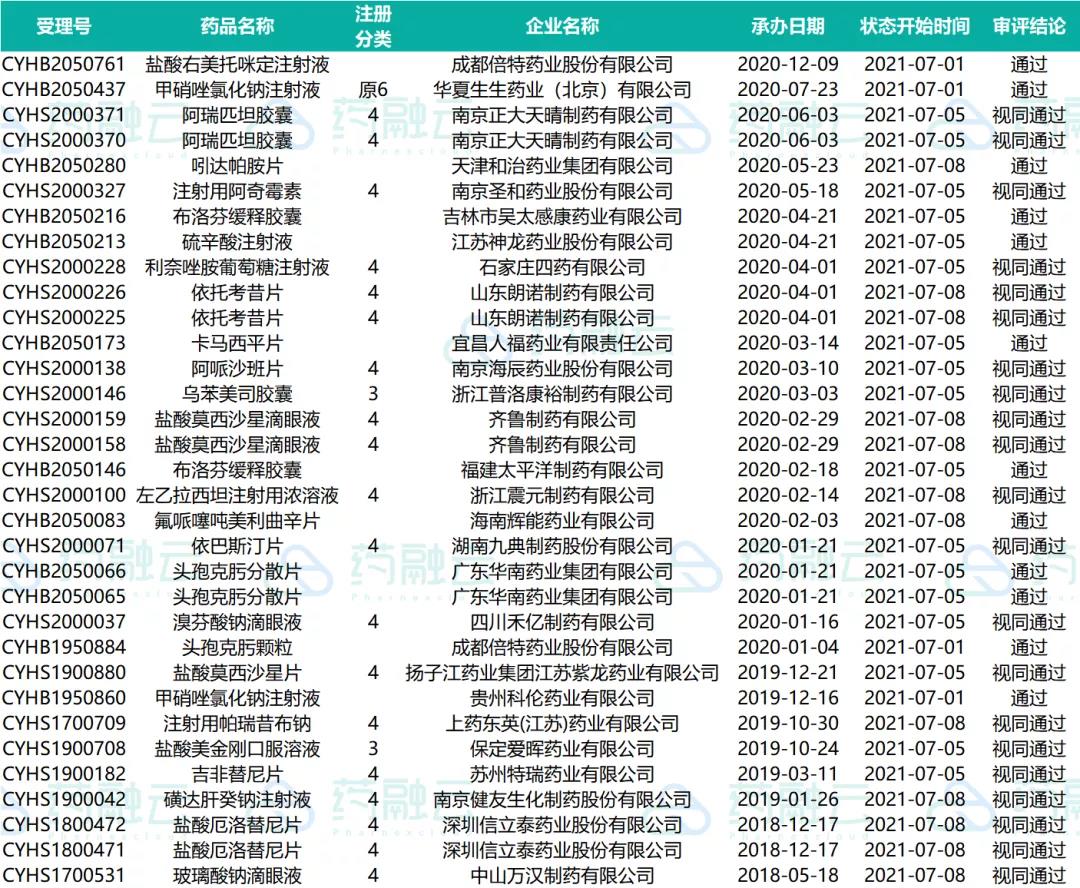

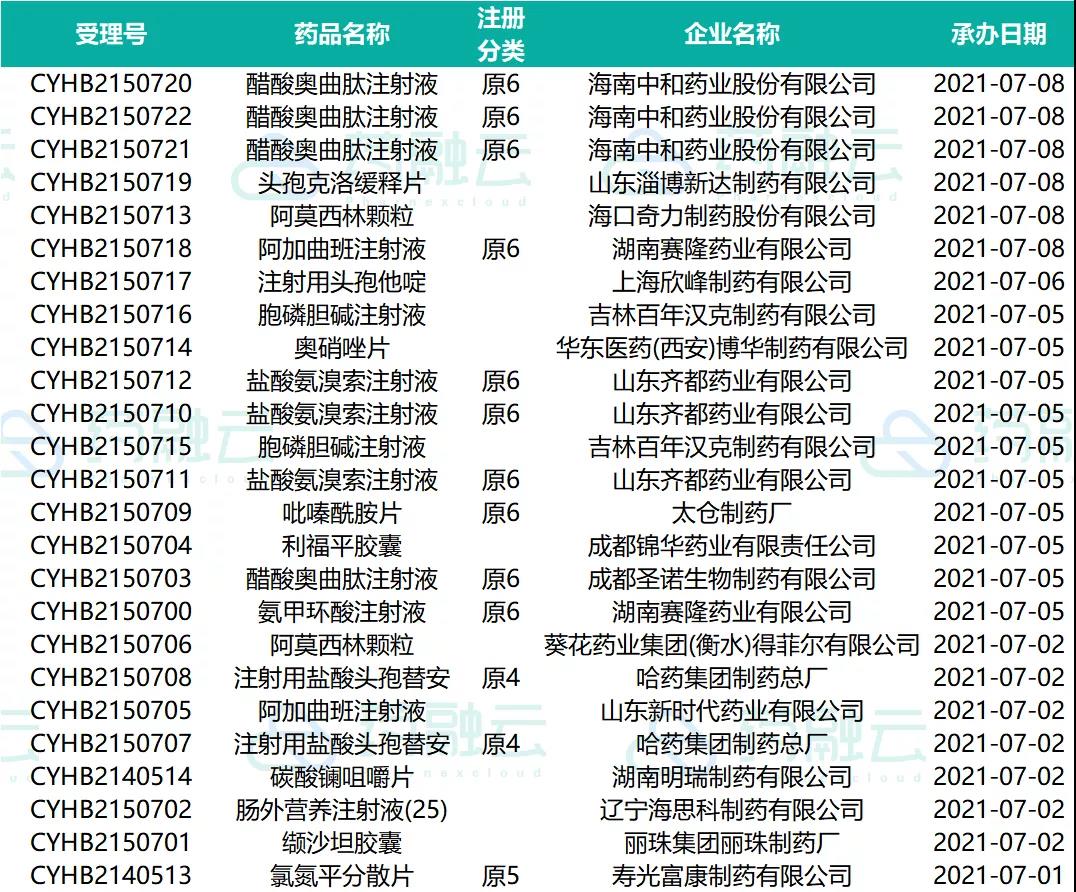
一致性评价申请
近期有16个品种提交一致性评价申请。详见下表:

















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论