"PD-1"相关的结果
-

齐鲁制药:抗肿瘤药物研发又迎新进展!PD-1单抗临床研究结果公布
创新时代的车轮滚滚向前,齐鲁制药持续加大研发投入,积极创新弯道超车。据药融云统计,齐鲁制药今年在千亿肿瘤免疫市场持续布局,目前已有1款1类新药申报上市、9款1类新药获批临床,其中主要瞄准的是抗肿瘤药物研发,近日又迎来研发新动态。 -

再生元11亿美元回购PD-1,只为成为肿瘤免疫领导者!
2022年6月2日,再生元回购Cemiplimab全球权益。赛诺菲将获得首付款9亿美元,监管注册和销售里程碑付款2亿美元以及约定范围内的11%的特许使用权费用。 -
康方生物的新型PD-1单抗上市|正大天晴_齐鲁_安科..生物类似药来袭!
2021年8月5日,NMPA批准康方生物与正大天晴共同申报的抗PD-1单抗派安普利单抗上市,医药市场迎来了第5款国产PD-1单抗,是目前全球唯一采用IgG1亚型且经Fc段改造的新型PD-1单抗。派安普利单抗此次获批的适应症为:用于治疗至少经过二线系统化疗复发或难治性经典型霍奇金淋巴瘤。 -
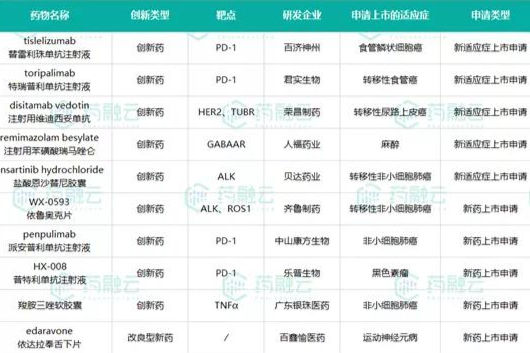
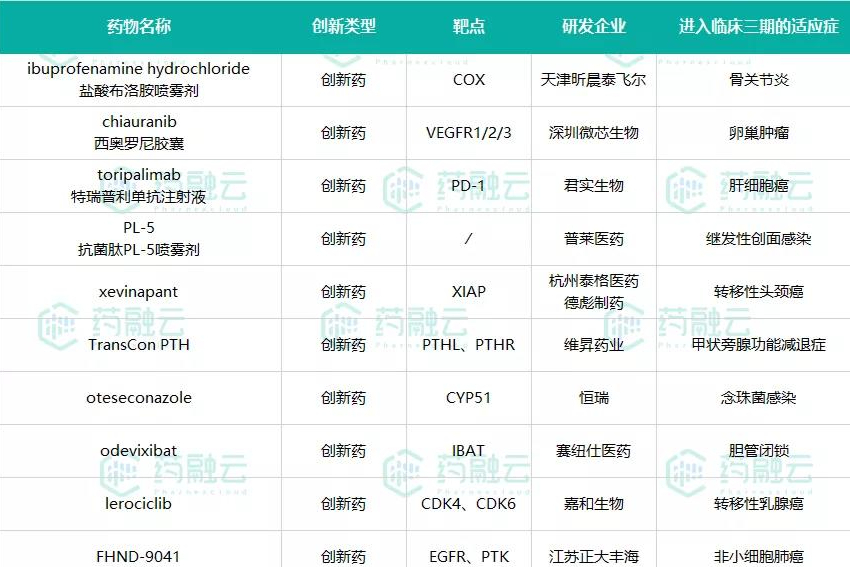
5款新药上市在即|4款PD-1单抗提交NDA申请|康方生物的PD-1能否逆袭?
据药融云全球药物研发、中国审评、中国临床、全球临床、中国药品批文等数据库统计: 2021年7月,我国仅有一款新药上市为同路生物的生物类似药人凝血酶原复合物。 10款新药提交NDA申请,其中5款提交新的适应症上市申请,5款新药即将面世。 97款新药申请临床。 百余款药物进入新的临床阶段:2款新药开展上市后Ⅳ期临床试验,17款新药开展Ⅲ期临床试验,18款新药开展Ⅱ期临床试验,72款新药开展Ⅰ期临床试验。 -

创造历史!FDA首次受理国产自研创新PD-1药物并进入审评阶段!
药融云数据库查询显示:中国自主研发的创新生物药的完整上市申请首次被美国FDA受理并进入正式审评阶段 -

四大国产PD-1全部出海 恒瑞、君实、百济、信达谁海外实力最强?
随着君实的特瑞普利单抗开启出海之旅,四大国产PD-1下一“战场”逐渐扩大至海外,相继挺进医保目录的四款PD-1在海外实力到底如何?谁会有更大的发展? -

-

治疗有效率59% 新抗原疫苗+PD-1迈出坚实一步
PD1在临床上的用法灵活多变,单药疗效不够时,可以联合化疗、靶向、CTLA4、放疗等来增效,近日更是惊现PD1联合疫苗的搭配方式! -

替尼爆炸 PD-1泛滥 新药研发何去何从?
若论2019年最炙手可热的靶点,PD-(L)1当之无愧。在O药、K药先后于国内上市后,国内君实、信达、恒瑞、百济你追我赶,好不热闹。但是随着企业如潮水般涌入,这一赛道的研发趋于拥挤,有分析师形容当下研发呈现出“替尼爆炸,PD-1泛滥”的态势。 -

信达PD-1联合贝伐单抗治疗晚期肝癌达主要研究终点,拟提交上市申请
这是全球首个达到主要研究终点的PD-1抑制剂联合治疗用于晚期肝癌一线治疗的III期研究。






































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息