据药融云全球药物研发、中国审评、中国临床、全球临床、中国药品批文等数据库统计:
- 2021年8月,我国仅有一款新药上市,为康方生物/正大天晴申报的派安普利单抗
- 6款新药提交NDA申请,其中2款提交的为新适应症上市申请。
- 105款新药申请临床。
- 4款新药开展上市后Ⅳ期临床试验,21款新药开展Ⅲ期临床试验,35款新药开展Ⅱ期临床试验,62款新药开展Ⅰ期临床试验。
一、第5款国产PD-1单抗面世
2021年8月5日,NMPA批准康方生物与正大天晴共同申报的抗PD-1单抗派安普利单抗上市,医药市场迎来了第5款国产PD-1单抗,是目前全球唯一采用IgG1亚型且经Fc段改造的新型PD-1单抗。派安普利单抗此次获批的适应症为:用于治疗至少经过二线系统化疗复发或难治性经典型霍奇金淋巴瘤。
派安普利单抗是一款康方生物自主研发的具有创新性、潜在同类最佳的人源化抗PD-1单克隆抗体,差异化地选择了结构稳定的免疫球蛋白G1亚型,并通过结晶(Fc)段改造,去除了ADCC/ADCP/CDC效应,避免了免疫细胞被吞噬或杀伤,持久阻断了PD-1通路的活性,能够维持更强的T细胞抗肿瘤活性。
表1 上市的新药

数据来源:药融云全球药物研发数据库
二、6款新药提交NDA申请
2021年8月,我国共有6款新药提交NDA申请,其中2款提交新的适应症上市申请,3款生物类似药和1款改良型新药即将面世。这6款新药共有5款单克隆抗体,另有2款创新药此次申请上市的适应症为“鼻咽癌”。
表2 提交NDA申请的新药
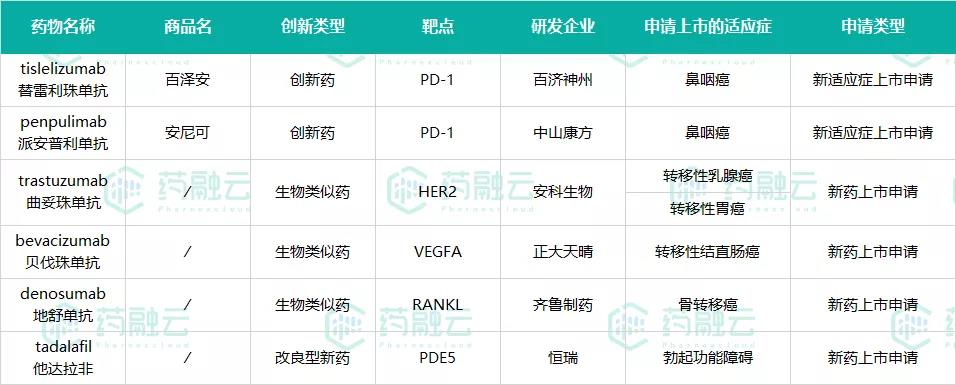
数据来源:药融云全球药物研发数据库
(1)替雷利珠单抗注射液
8月20日,百济神州提交替雷利珠单抗的新适应症上市申请,用于 “复发或转移性鼻咽癌患者的一线治疗”,这是替雷利珠单抗在我国提交的第9项新适应症上市申请。
(2)派安普利单抗
8月5日,中山康方生物提交派安普利单抗的上市申请,用于“三线治疗转移性鼻咽癌”,这是派安普利单抗在中国和美国成功提交的第四个适应症上市申请。
(3)曲妥珠单抗
8月5日,安科生物研发的曲妥珠单抗申报上市,用于治疗“转移性胃癌”和“转移性乳腺癌”。这是国内第二个曲妥珠单抗类似药申报上市。
(4)贝伐珠单抗
8月3日,正大天晴研发的贝伐珠单抗申报上市,用于治疗“转移性结直肠癌”。目前国内已有4款贝伐珠单抗类似药获批上市。
(5)地舒单抗
8月30日,齐鲁制药研发的地舒单抗申报上市,用于治疗“骨转移癌”,这是国内首家申报的地舒单抗类似药。
(6)他达拉非
8月3日,恒瑞医药研发的2.2类改良型新药他达拉非口溶膜申报上市,用于治疗“勃起功能障碍”。目前他达拉非在国内有4种剂型(普通片剂、咀嚼片、混悬剂及口溶膜剂),除普通片剂外,尚未有其他剂型获批,不过齐鲁制药已经首家申报上市了口溶膜剂。
三、17款新药进入临床三期
2021年8月,21款开展Ⅲ期临床试验的新药中,有15款是创新药,5款是生物类似药。8月,深圳微芯、正大天晴、恒瑞等大型药企都有新药纷纷开展临床三期试验。
表3 进入临床三期的新药
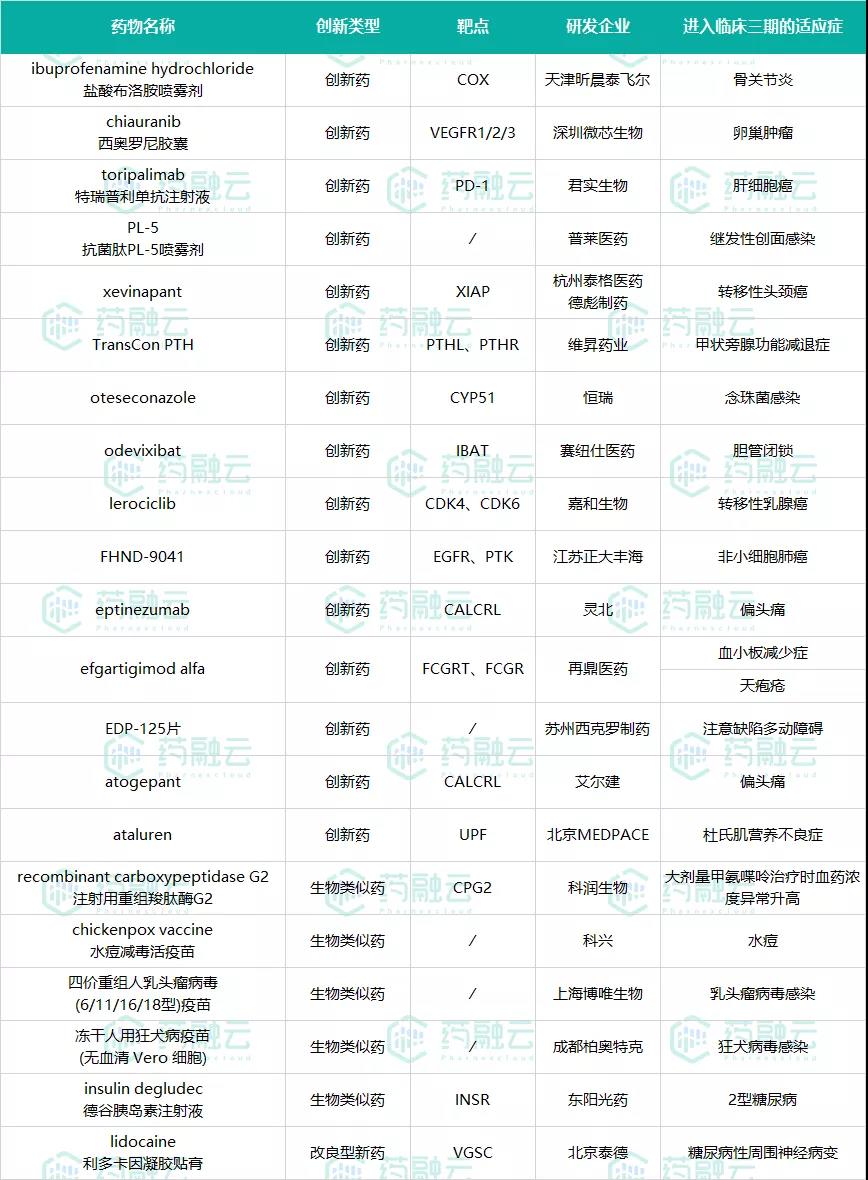
数据来源:药融云全球药物研发数据库






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论