Karuna Therapeutics
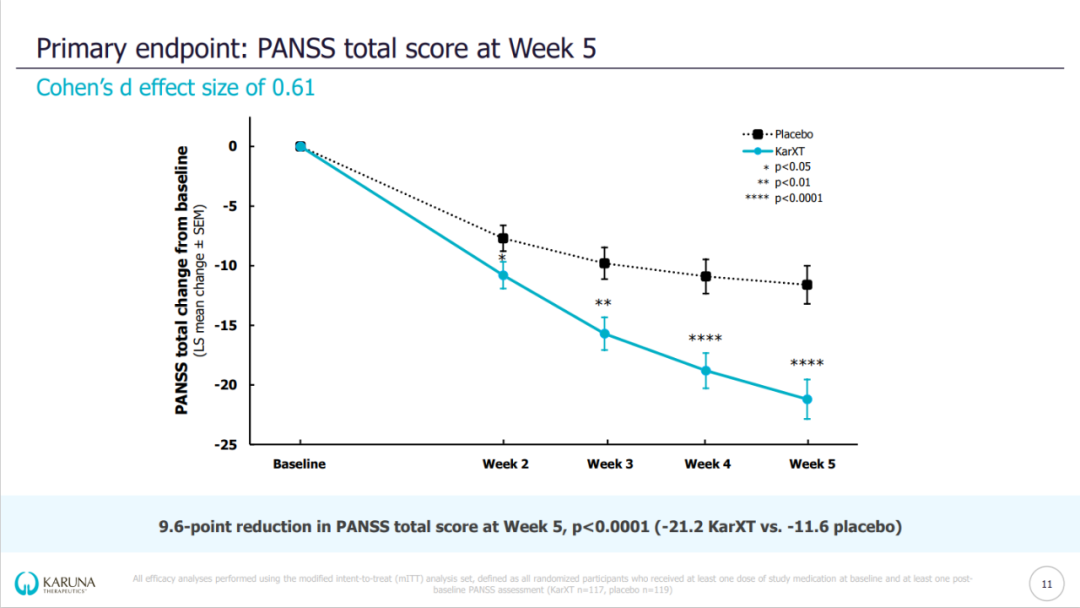
2022年8月8日,Karuna Therapeutics, Inc.(纳斯达克股票代码:KRTX) 宣布其3期临床研究EMERGENT-2的阳性初步结果,该研究评估了其主要在研疗法KarXT(xanomeline-trospium)在成人精神分裂症患者中的疗效、安全性及耐受性。该研究达到了其主要终点,在第五周时,与安慰剂相比,KarXT在阳性和阴性综合征量表(PANSS)总分降低了具有统计学意义和临床意义的9.6分(-21.2 KarXT与-11.6 安慰剂,p<0.0001)(Cohen’s d效应量为0.61)。从第2周开始,根据PANSS总分评估,KarXT还表现出早期且持续的有统计学意义的显著症状减少,并持续至研究结束。(推荐阅读:KarXT最新消息丨BMS创新机制精神分裂症药物,或将打破半世纪僵局)
KarXT在3期临床研究EMERGENT-2中也达到了关键的次要终点,精神分裂症的阳性症状(如,幻觉或妄想)和阴性症状(如,难以享受生活或远离他人)均实现统计学上显著减少,评估方式为PANSS阳性症状、PANSS阴性症状和PANSS Marder阴性症状分量表。
▲https://investors.karunatx.com/news-releases/news-release-details/karuna-therapeutics-announces-positive-results-phase-3-emergent
第 5 周时的结果包括:
与安慰剂相比,KarXT的PANSS阳性症状分量表降低2.9分(-6.8 KarXT对比-3.9 安慰剂,p<0.0001)。与安慰剂相比,KarXT的PANSS阴性症状分量表降低1.8分(-3.4 KarXT对比-1.6 安慰剂,p=0.0055)。与安慰剂相比,KarXT的PANSS Marder阴性症状分量表降低2.2分(-4.2 KarXT与-2.0 安慰剂,p=0.0022)。KarXT总体耐受性良好。KarXT组和安慰剂组的总体停药率相似(25%对比21%)。KarXT和安慰剂的总体治疗出现不良事件(TEAE)率分别为75%和58%。
3期临床研究EMERGENT-3的初步数据预计将在2023年第一季度发布。预计在2023年年中,向美国FDA提交KarXT用于精神分裂症的NDA(新药上市申请)。针对3期临床研究EMERGENT-2数据的额外分析正在进行中。
Karuna Therapeutics由CNS领域老兵Steve Paul先生创立,现任董事会主席兼首席执行官。曾任职于美国国家精神卫生研究院(NIMH)和NIH科学部门以及礼来制药等等。同时也是Sage Therapeutics、Voyager Therapeutic联合创始人。
关于精神分裂症(Schizophrenia)

精神分裂症是一种慢性且经常使人衰弱的精神疾病,它会影响人们的思考、感受和行为方式。它的特点是阳性症状(幻觉和妄想)、阴性症状(难以享受生活和远离他人)和认知障碍。全球影响超过2100万人。
据数据预计,目前中国有超过800万精神分裂症患者,但接受治疗的患者不足一半,从目前的抗精神病药物治疗中获得足够症状改善的人更少。与全球患者类似,大中华区精神分裂症患者迫切需要更有效的、安全性更高的治疗方法。
关于KarXT
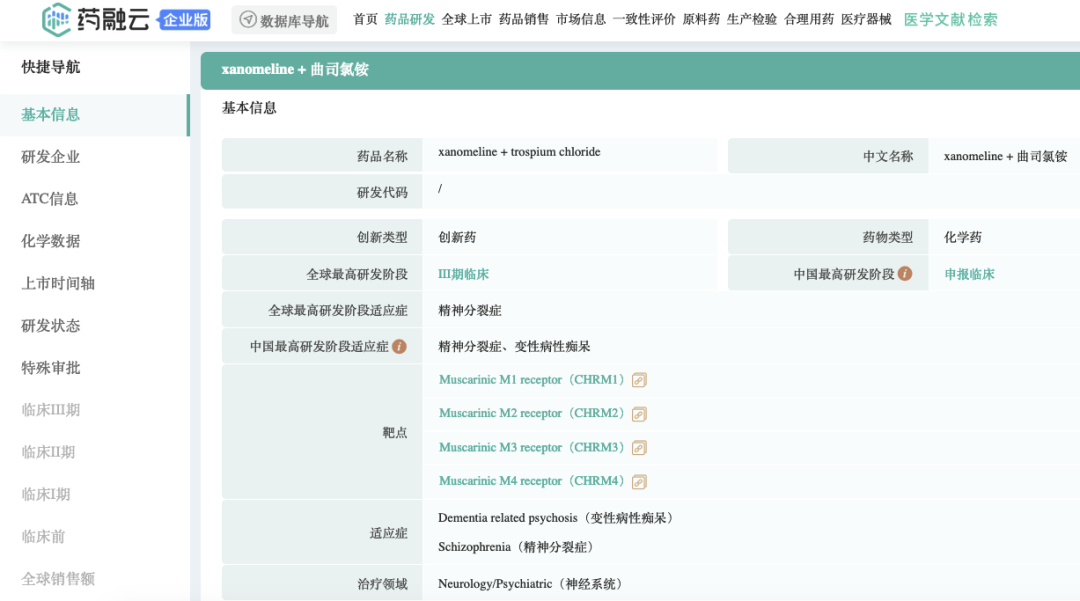
药融云数据,www.pharnexcloud.com
KarXT (xanomeline-trospium) 是一种口服的、在研的M1/M4首选毒蕈碱激动剂,用于治疗精神和神经系统疾病,包括精神分裂症和阿尔茨海默症中的精神症状。KarXT由毒蕈碱激动剂xanomeline和毒蕈碱拮抗剂trospium(曲司氯铵)组成,旨在优先刺激中枢神经系统中的毒蕈碱受体。
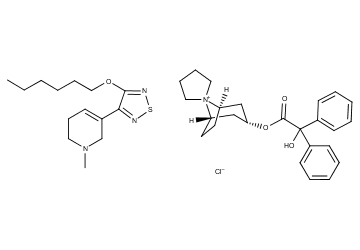
▲KarXT (xanomeline-trospium) ,相关专利WO-2020069301
据药融云数据库显示,截至目前,KarXT针对精神分裂症的适应症临床试验已推进到3期,变性病性痴呆适应症推进到临床2期。KarXT是目前潜在首个具有这种真正新颖且独特的双重机制,不依赖多巴胺能或血清素能途径来治疗严重精神疾病的症状的药物。
KarXT适应症研发现状
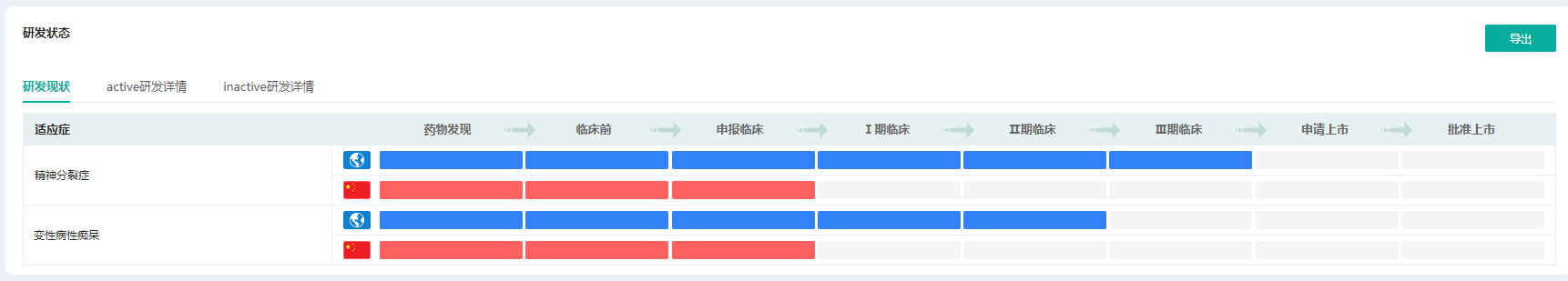
截图来源:药融云全球药物研发数据库
2021年11月,再鼎医药与Karuna Therapeutics签订了独家许可协议,拥有在大中华区(包括中国内地、中国香港、中国澳门和中国台湾地区)开发、生产和商业化KarXT的权益。交易细节:Karuna获得3500万美元的现金首付款(upfront),及潜在里程碑付款(最高达8000万美元的注册里程碑付款和最高达7200万美元的销售里程碑付款milestone)和特许权使用费(百分之十几至二十之间的royalty)。
此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场
参考:
NMPA/CDE;
药融云数据,www.pharnexcloud.com;
FDA/EMA/PMDA;
相关公司公开披露;
www.karunax.com;
https://investors.karunatx.com/news-releases/news-release-details/karuna-therapeutics-announces-positive-results-phase-3-emergent;
https://investors.karunatx.com/events-presentations;
www.zailaboratory.com;
再鼎医药和Karuna Therapeutics宣布在大中华区就KarXT开发和商业化达成战略合作;
《中国精神分裂症防治指南(第二版)》;
《精神病学》;
Charlson FJ, et al. Global Epidemiology and Burden of Schizophrenia: Findings From the Global Burden of Disease Study 2016. Schizophr Bull. 2018 May 12. doi: 10.1093/schbul/sby058.;等等。
想要解锁更多药企创新药信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、研发阶段、最新进展、申报获批情况、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论