
近日,恒瑞医药子公司山东盛迪医药有限公司收到国家药品监督管理局核准签发的《药品临床试验批准通知书》,同意公司自主研发的1类创新口服小分子GLP-1受体激动剂HRS-7535片开展用于减重适应症的Ⅱ期临床研究。

HRS-7535片是一种新型口服小分子胰高血糖素样肽-1(GLP-1)受体激动剂,既可以通过激活人的GLP-1受体,促进胰腺的胰岛素分泌和降低胰高血糖素分泌并抑制胃排空,还可以通过影响中枢增强饱腹感和抑制食欲,直接减少能量的摄入等机制用于治疗2型糖尿病(T2DM)和减重。全球范围内尚无口服小分子GLP-1受体激动剂上市。

来源:药融云全球药物研发数据库
恒瑞医药自主研发的小分子口服GLP-1受体激动剂HRS-7535片已完成一项中国单次给药和多次给药的Ⅰ期健康人试验(HRS-7535-101)。作为国内首个见刊的口服小分子GLP-1受体激动剂I期临床研究,HRS-7535-101数据显示,HRS-7535具有良好的安全性、耐受性及药代动力学特征,支持每日一次的给药方式。值得一提的是,即使基体重较低(67.6kg),HRS-7535片连续给药4周后依旧可以观察到体重下降4.38kg的明显减重效果。该研究全文已于2023年11月刊登于代谢领域权威杂志《糖尿病肥胖与代谢》(Diabetes Obes Metab,影响因子:5.8)。此外,HRS-7535目前已完成成人2型糖尿病(T2DM)II期临床研究的入组。
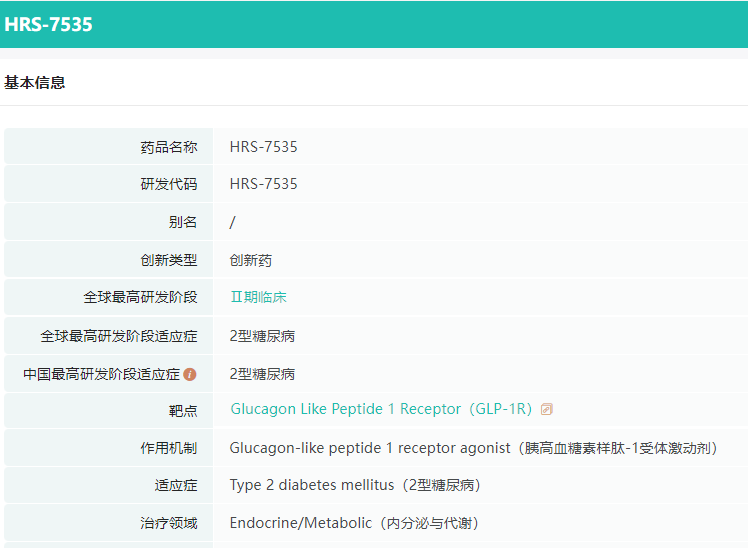
来源:药融云全球药物研发数据库
基于较好的安全性、耐受性,HRS-7535片有望为中国肥胖及超重的广大人群提供新的治疗选择。
推荐阅读:GLP-1产业现状与未来发展
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






























![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://yaorongyun-public.oss-cn-shanghai.aliyuncs.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)









 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论