
8月22日,三生国健宣布,其研发的抗IL-4Rα人源化单克隆抗体药物(研发代号:611)在中国中重度特应性皮炎成人受试者中进行的多中心、随机、双盲、安慰剂对照、2期临床研究达到主要终点。结果显示,611可显著改善中国中重度特应性皮炎成人患者的临床症状,且应答迅速。

特应性皮炎(AD)是一种慢性、复发性、炎症性皮肤病。中重度特应性皮炎患者通常全身大部位皮肤红疹,引发强烈持续的瘙痒、皮肤干燥、结痴、渗液等症状。该病属于自身免疫性疾病,由异常免疫反应引起,致病原因涉及免疫的多个环节,如朗格汉斯细胞和皮肤树突细胞对变应原的提呈、Th2为主的异常免疫反应、调节性T细胞功能障碍、IgE过度产生和嗜酸性粒细胞升高等。目前,皮质类固醇类药物是治疗此类疾病最常用的药物,但该类药物较强的副作用,限制了其临床应用,目前临床上仍具有广泛的未被满足的治疗需求。
公开资料显示,611产品是一款人源化抗IL-4Rα单克隆抗体,具有全新的氨基酸序列。611能够通过特异性的结合IL-4Rα,阻断IL-4和IL-13的信号传导,实现对免疫功能的调节,达到缓解特应性皮炎等疾病的作用。
611基本信息
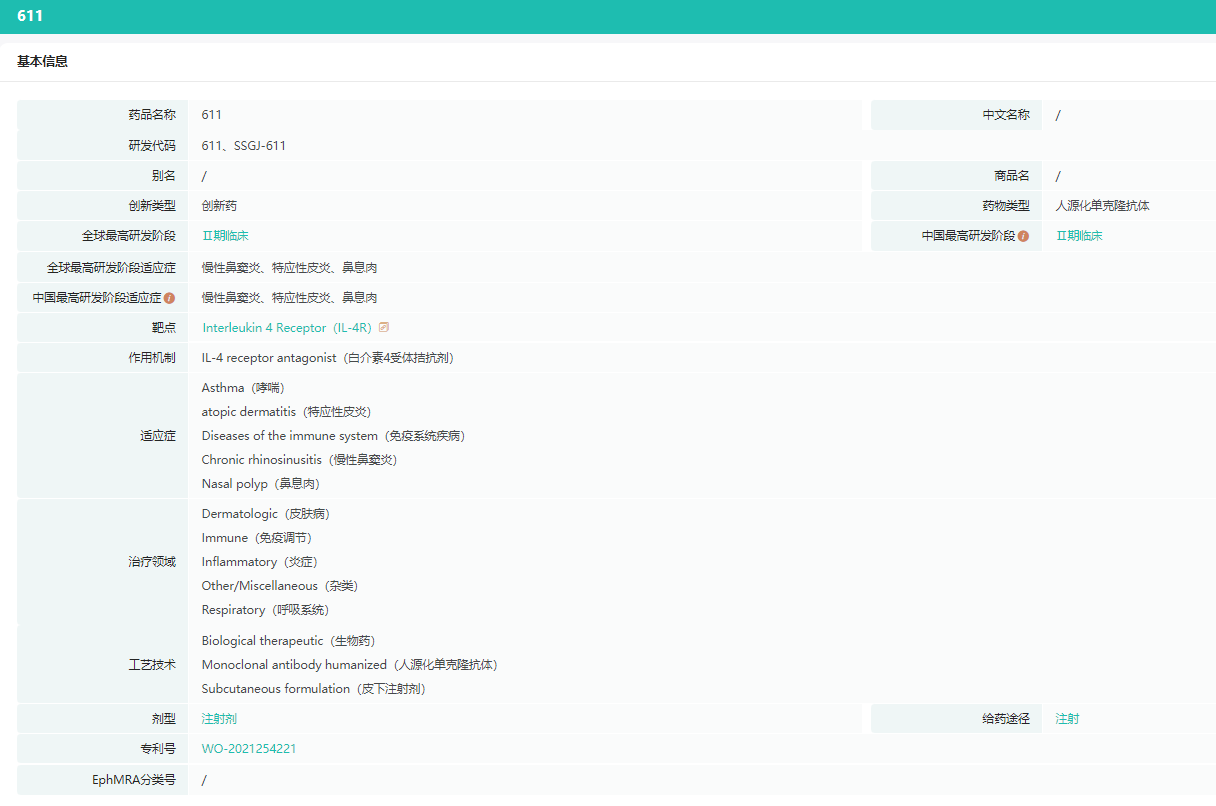
截图来源:药融云全球药物研发数据库
此次达到主要终点的研究共纳入93例中重度特应性皮炎成人受试者,以1:1:1的比例被随机分配至试验药物A组(611首剂600mg + 300mg每两周一次[Q2W])、试验药物B组(611首剂600mg + 300mg每四周一次[Q4W])和安慰剂组,每个剂量组别各分别纳入30例、31例和32例受试者,并接受相应的试验药物或安慰剂治疗,主要疗效终点为“第16周时,EASI评分较基线降低≥75%(EASI-75)的受试者百分比”。截止目前,全部受试者完成16周访视并获得主要终点结果。
有效性方面,第16周时,各试验药物组达到EASI 75、IGA 0/1(定义为研究者整体评分法[IGA]评分达到0或1分且较基线降低≥2分)、EASI 90、EASI 50和瘙痒NRS周平均值较基线降低≥4分的受试者百分比均显著高于安慰剂组,且具有显著的统计学意义。
安全性方面,611整体安全性和耐受性良好,药物相关的不良事件严重程度均为1~2级(CTCAE级别),无≥3级的药物相关不良事件、无药物相关SAE,无导致停药、退出和死亡的TEAE。与前期临床研究数据及同靶点药物相比,未发现新的安全性信号。
根据三生国健新闻稿介绍,通过瘙痒NRS评分可以看到,611在给药后第2周即显示出明显的缓解瘙痒的临床作用,且持续维持至第16周。尤其值得关注的是,2期研究中每4周一次的给药方案同样显示出明确的疗效应答,临床上有望实现探索较长周期(如Q4W)的给药频率,在保证临床疗效的基础上,提高特应性皮炎患者的治疗依从性。目前,该研究的随访仍在进行中,研究相关完整数据将随研究进展进行披露。
三生国健董事长娄竞博士表示,“我们很高兴看到611完成了2期临床研究,并获得积极结果。未来,我们将加速推进该产品的临床试验进程,期待在大样本人群中进一步确证611的积极疗效。三生国健将继续致力于探寻及开发更安全有效的治疗性生物制剂,以应对迫切的医疗需求,为自身免疫性疾病患者提供重要的治疗选择。”
参考资料:
1.公司官网
2.药融云数据库
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论