
8月25日,中国国家药品监督管理局药品审评中心(CDE)官网显示,阿斯利康提交1类新药AZD5335的临床试验获得受理。

来源:CDE官网
关于AZD5335
据了解,AZD5335是阿斯利康第 3 款自研 ADC 新药,由靶向FRα抗体与TOP1i有效载荷(AZ14170132)偶联而成,DAR值为8。
研发进度查询
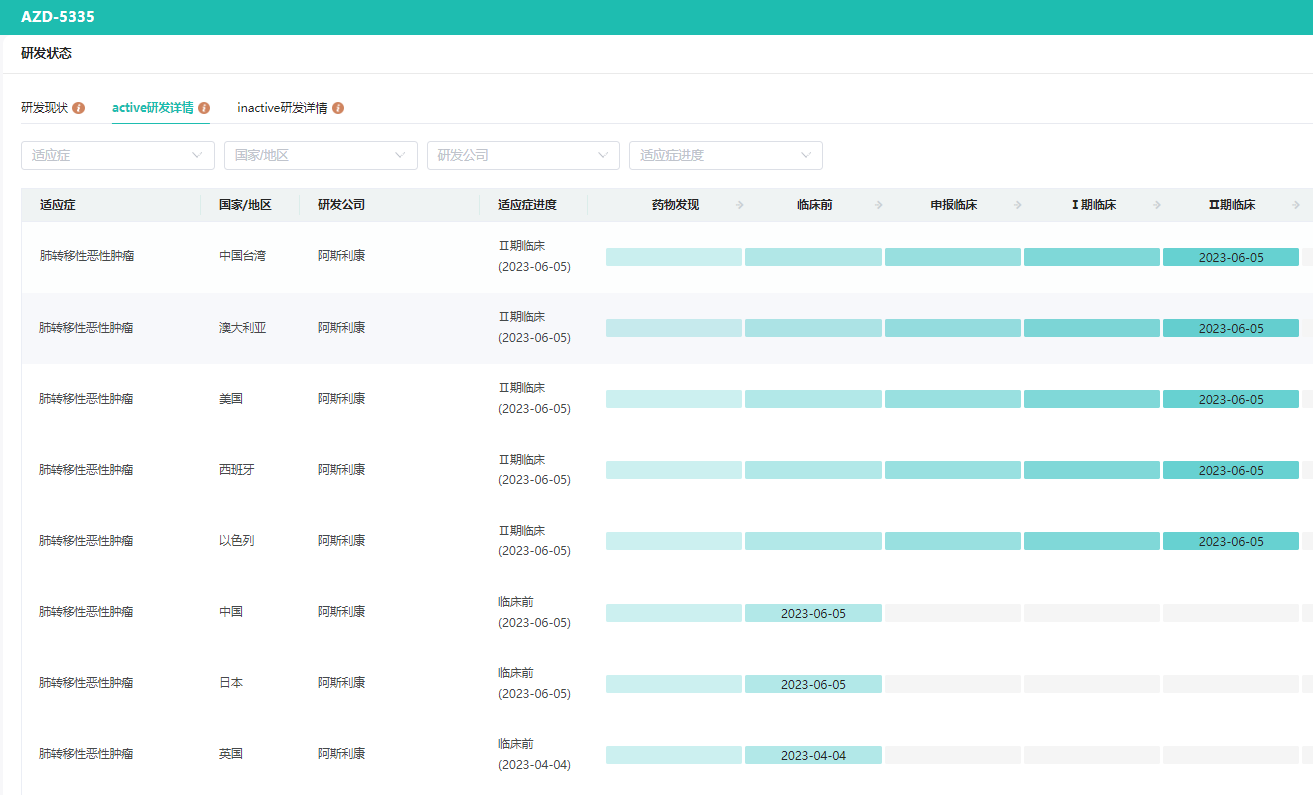
截图来源:药融云全球药物研发数据库
阿斯利康在2023年美国癌症研究协会年会(AACR)上首次披露其自主研发的FRα 靶向ADC AZD5335在FRα阳性卵巢癌中的临床前疗效。
阿斯利康2023半年报显示,其重磅HER2 ADC药物Enhertu(DS-8201)销售额达11.69亿美元,同比增长两倍。同时,阿斯利康还在积极推进其管线上其它ADC产品。阿斯利康与第一三共合作 DS-8201a 和 DS-1062;还与国内康诺亚牵手成功,以总额近 12 亿美元引进 CLDN18.2 ADC 项目 CMG901。
今年 2 月,AZD5335已经在 ClinicalTrials.gov 登记了 I/IIa 期临床,探究 AZD5335 单药或联用 PARP1 抑制剂 AZD5305 在实体瘤中的安全性、耐受性和初步抗肿瘤活性。
2023上半年,阿斯利康的中国区收入达到 30.43 亿美元,同比增长 9%。阿斯利康还预计这款ADC新药将在中国取得新进展。
参考资料:
1.CDE官网
2.药融云数据库
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论