
10月19日,华润双鹤全资子公司双鹤药业(海南)有限公司递交了利那洛肽胶囊的上市申请,并获得CDE受理。目前该药国内仅原研获批上市,仿制药方面除此次报产的双鹤药业外,另有四川国为制药于2021年11月递交了上市申请,目前尚在审评审批中。总体来说,该药的国内首仿药竞争程度较弱。
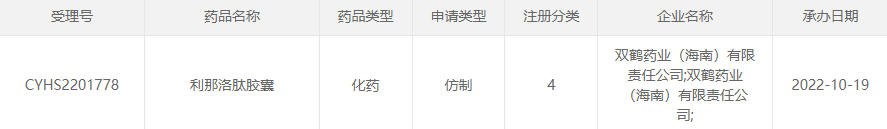
截图来源:CDE官网
利那洛肽是一款由Ironwood自主研发的鸟苷酸环化酶-C(GC-C)激动剂,于2012年8月在首次获批上市,用于便秘、便秘型肠易激综合征。目前Ironwood对该药还在持续开发,旨在增加新适应症,造福更多患者群体。据药融云统计,2021年利那洛肽全球销售额突破10亿美元大关。
在国内,利那洛肽胶囊于2019年初获批上市,次年年底被纳入医保乙类品种(限制用于成人便秘型肠易激综合征(IBS-C)),该版本目录于2021年3月1日正式实施。由此,利那洛肽胶囊实现快速放量。据药融云统计,2022年上半年,院内销售额超4千万,同比增长246%。目前该药国内市场由阿斯利康一家独占,期待国内首仿药早日获批上市。
利那洛肽胶囊院内销售情况(微信搜索"药融云小程序"查看更多维度数据分析)

截图来源:药融云全国医院销售数据库
2009年11月,安斯泰来与Ironwood达成合作,获得利那洛肽在日本、印度尼西亚、菲律宾、中国台湾和泰国的独家开发和商业化权益。后来,阿斯利康和艾伯维相继与Ironwood达成合作,阿斯利康获得利那洛肽在中国(除了台湾)的独家开发、生产和商业化权益,艾伯维则获得利那洛肽在上述国家和地区以外的独家权益。
原研为增加新适应症,对利那洛肽的开发还在持续进行中。今年9月,Ironwood公告宣布,其鸟苷酸环化酶C激动剂利那洛肽一项III期研究成功,治疗儿童功能性便秘(FC)患者。这是首款在III期研究中证明对儿童FC患者有效的药物。Ironwood表示,将与艾伯维共同推进该适应症的上市申请。
参考来源:
[1]CDE官网
[2] 药融云数据库
想要解锁更多仿制药信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握仿制药国内市场格局、上市情况、一致性评价、销售情况与各维度分析、企业申报情况、国家审批最新进展、集采情况、价格信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

—END—
















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论