
引言

2022年8月10日,Cure Rare Disease (CRD),一家总部位于波士顿的非营利性生物技术公司宣布,其首个CRISPR疗法CRD-TMH-001获得了FDA批准的临床申请,用于治疗杜氏肌营养不良(DMD)蛋白基因上的肌肉启动子和外显子1突变,预计第一位患者将在马萨诸塞大学医学院接受给药。
CRD-TMH-001
CRD-TMH-001为一次性给药。患者将接受静脉注射药物,并将在医院接受数日监测,以确保没有不受控制的不良反应。出院后,将根据FDA指南对患者进行为期15年的随访,以跟踪患者的进展。
“看到Cure Rare Disease获得FDA批准使用CRISPR反式激活剂技术治疗导致杜氏肌营养不良症的罕见突变的IND是令人鼓舞的。从这一重大成就中吸取的教训无疑将使其他罕见病患者受益。”马萨诸塞大学校长Terence Flotte在一份声明中说。
目前,杜氏肌营养不良有多种基因疗法进入临床,包括腺相关病毒(AAV)基因治疗,代表药物辉瑞的PF-06939926,已进入3期临床,反义寡核苷酸疗法(例如ExonDys-51,效果一般),CRD-TMH-001是第一个进入临床的CRISPR疗法。
除了CRD-TMH-001,针对DMD的不同突变,CRD还布局了多个杜氏肌营养不良管线,具体如下:
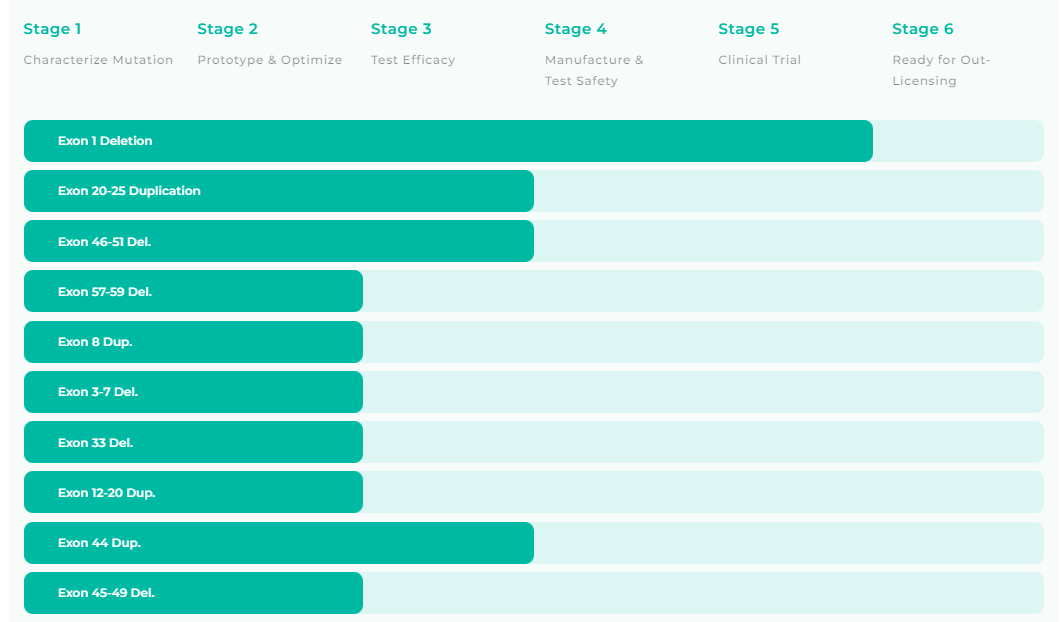

参考来源:
[1] https://www.cureraredisease.org/
<END>







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论