
引言
蛋白水解靶向嵌合体 (PROTAC)是用于一种靶向蛋白质降解的工程技术。具有两个共价连接配体的PROTAC分子将靶蛋白和E3泛素连接酶一起募集,以触发泛素-蛋白酶体的路径对靶蛋白进行降解。目前,PROTAC已成为一种有很有前景的靶向疗法,特别在癌症领域。
Molecular Cancer上发表了一篇名为Proteolysis-targeting chimeras (PROTACs) in cancer therapy的综述。在这篇综述中,作者汇总了 PROTAC 在靶向关键癌蛋白中的应用。
癌症的发生和发展是一个复杂的过程,其特点是维持增殖信号、逃避生长抑制因子、抵抗细胞死亡、诱导血管生成、激活侵袭和转移,下文将按这5类肿瘤活动和相关的异常蛋白质进行PROTAC的汇总,每个PROTAC分子的结构与靶点将在表格中列明:
靶向肿瘤中与增殖相关的蛋白
RAS-RAF-MEK-ERK通路在内的促生长信号在肿瘤中经常被过度激活,刺激细胞周期进程以诱导不受控制的细胞增殖。PROTAC技术已应用于靶向癌症中参与细胞周期调控的过表达、过激活或突变的蛋白质:
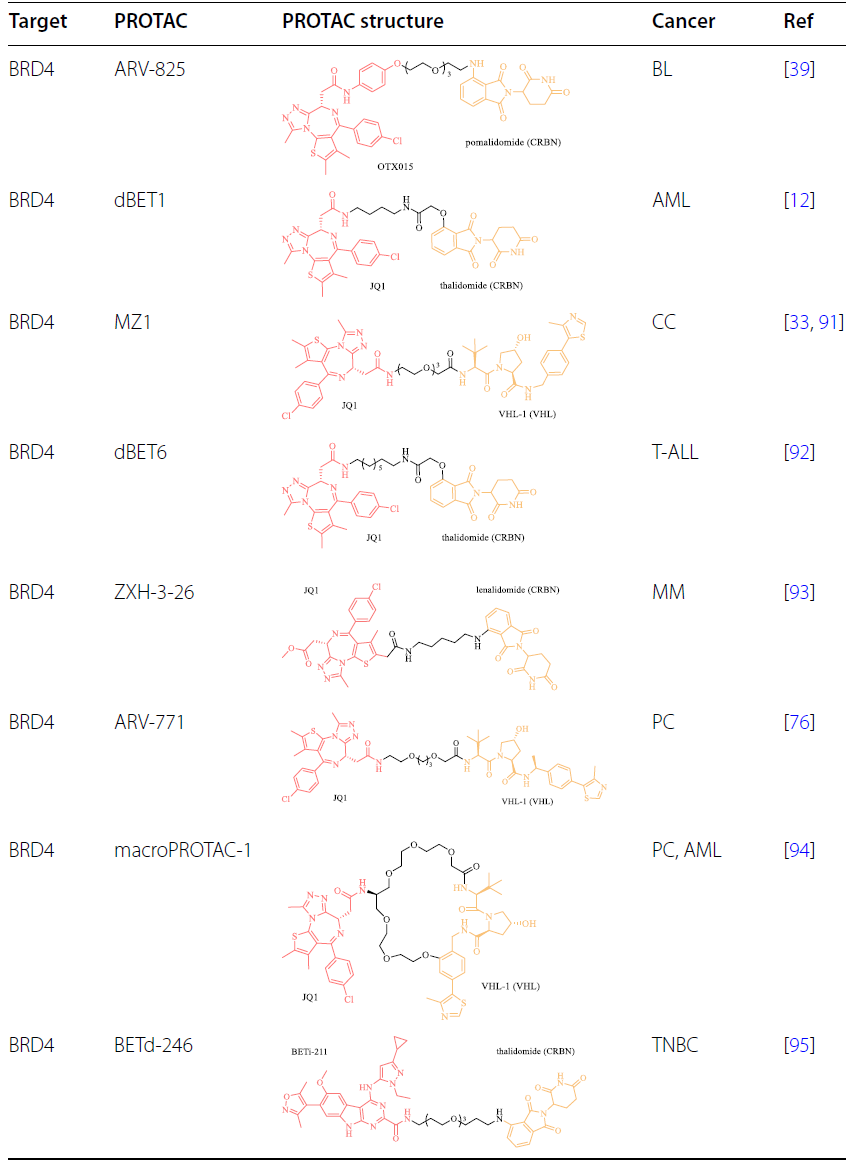
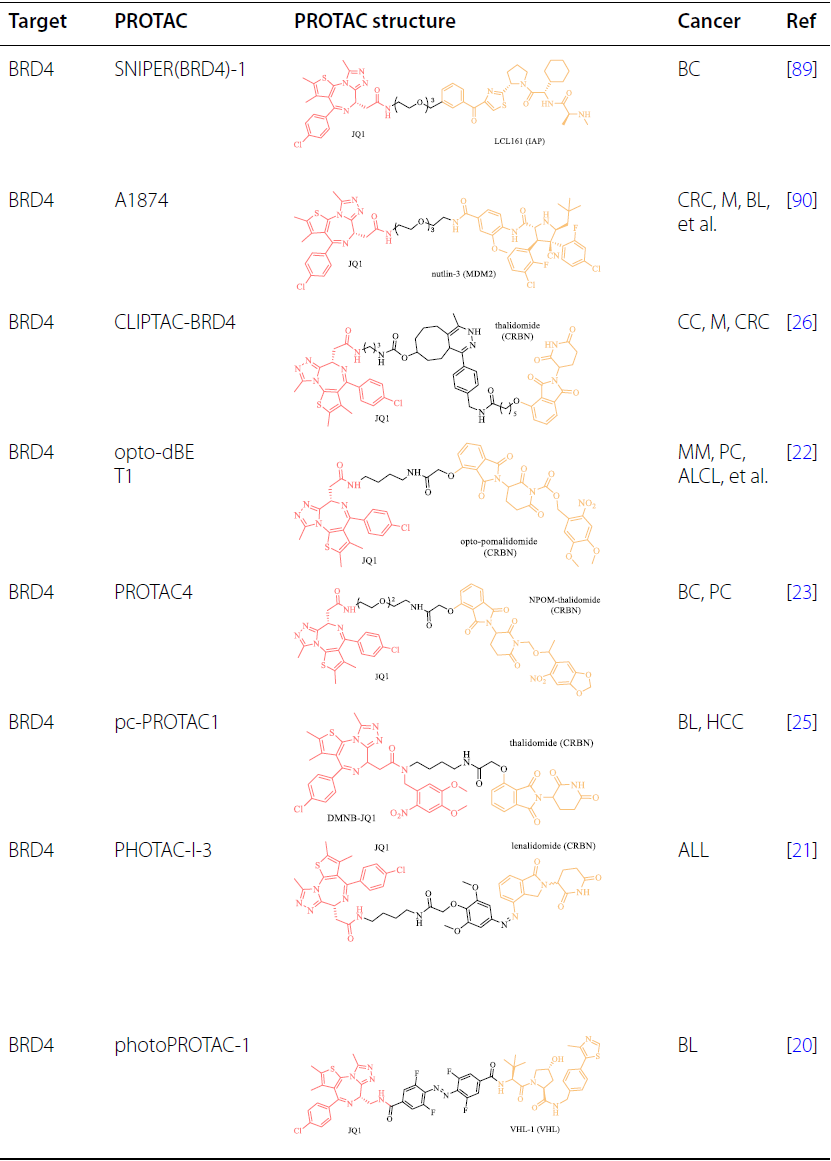
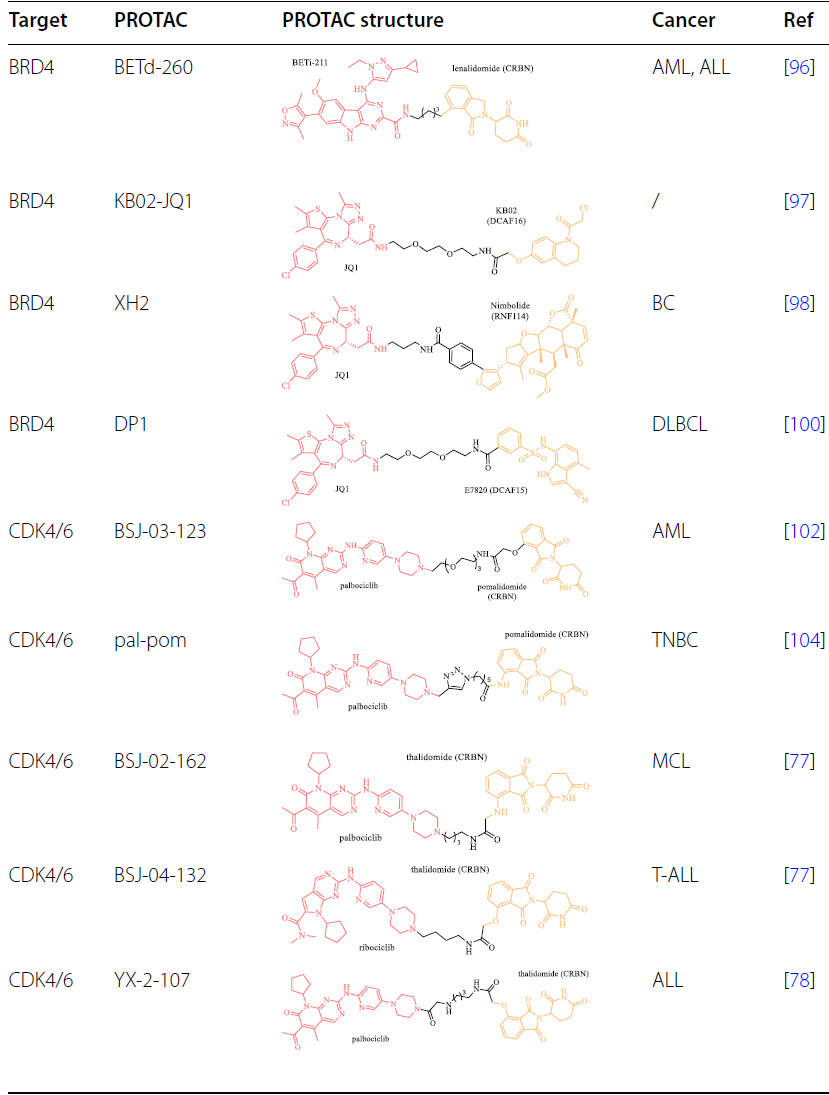

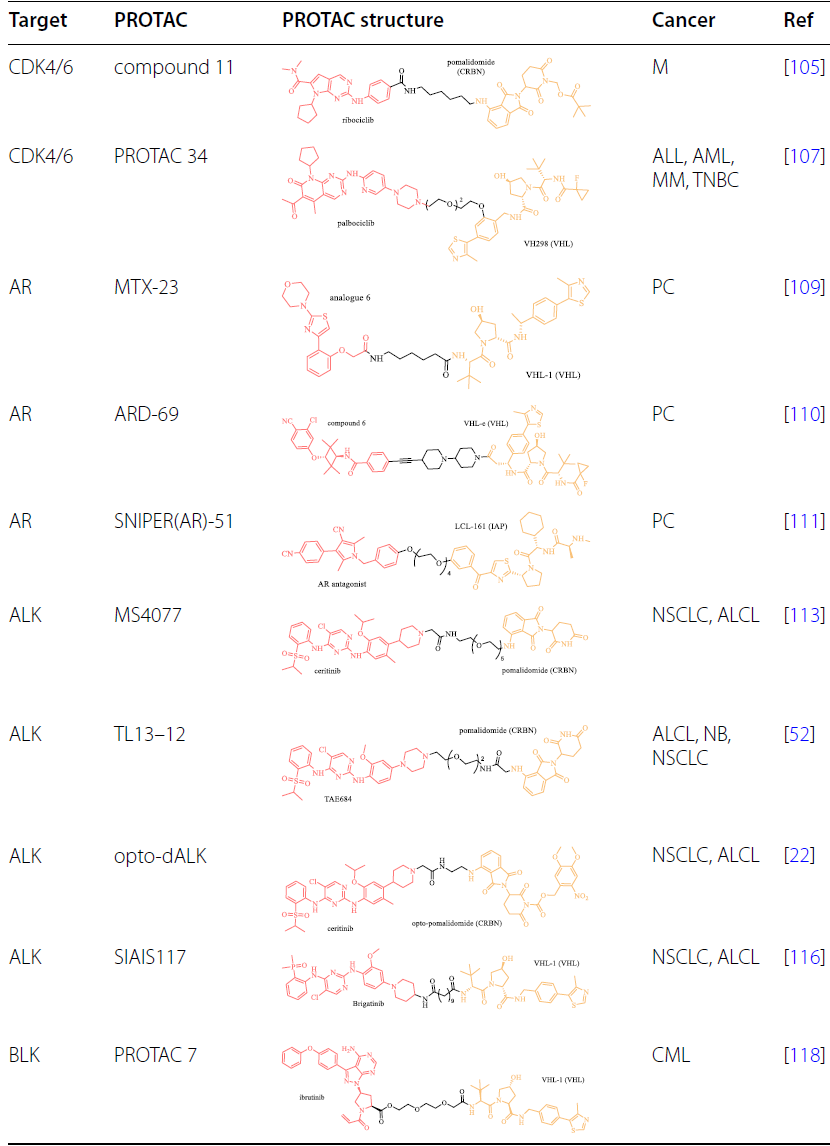
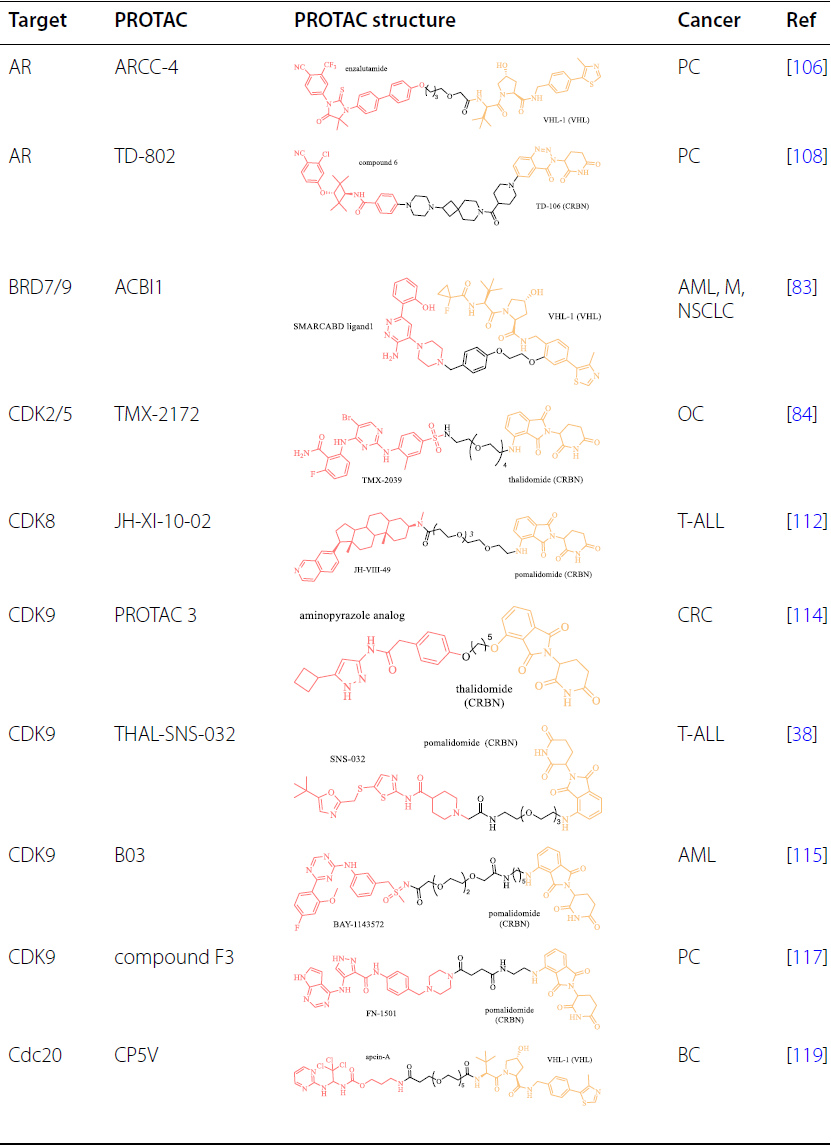
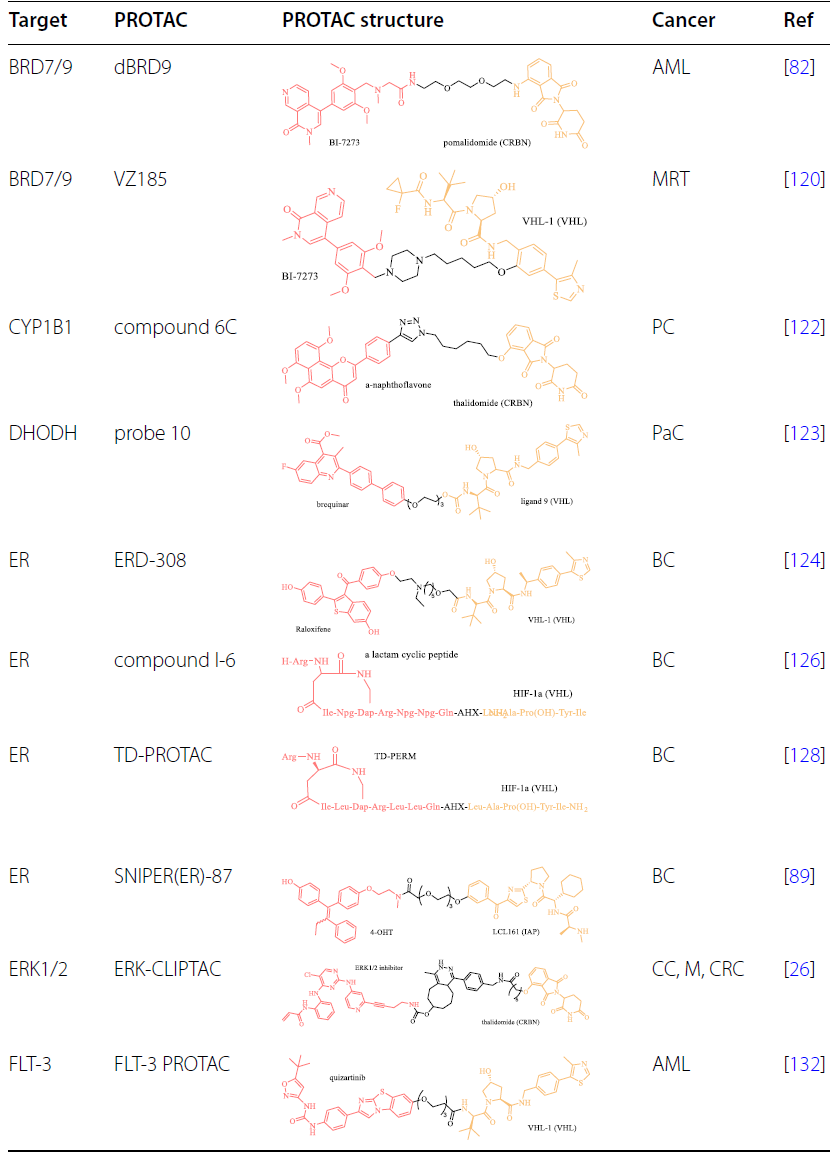
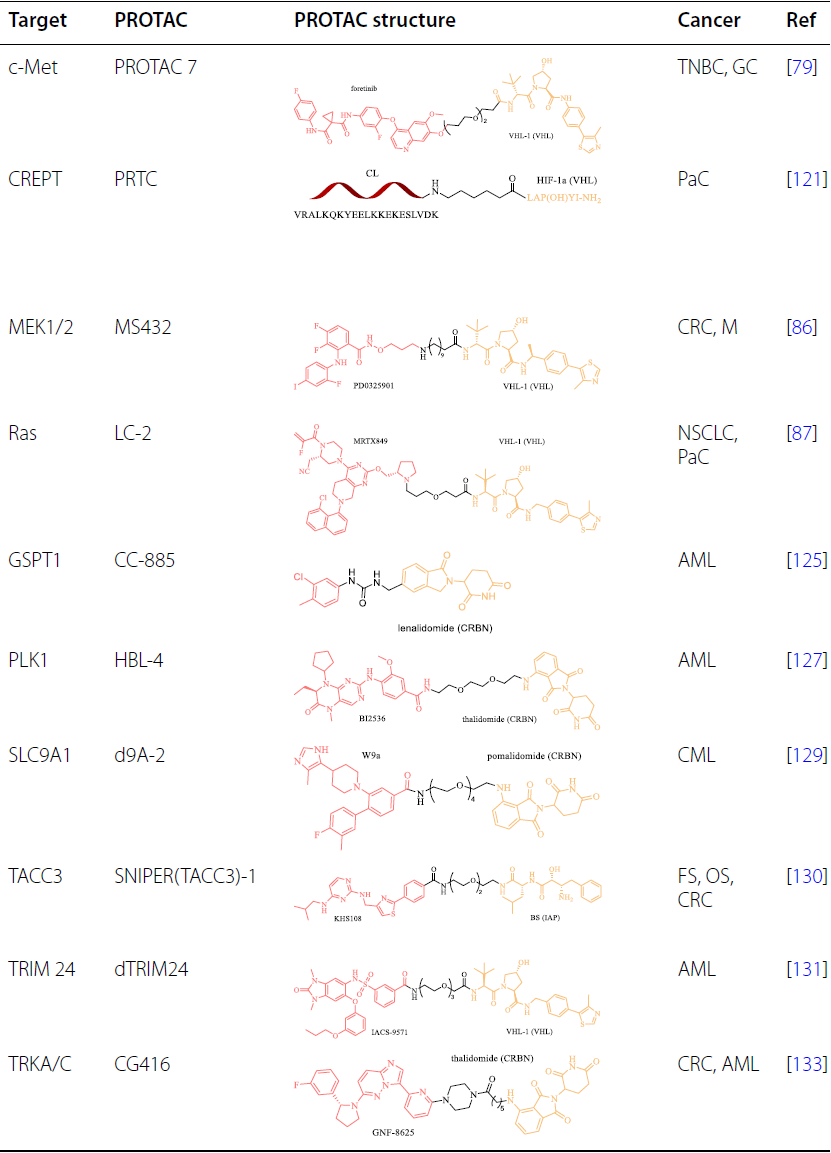
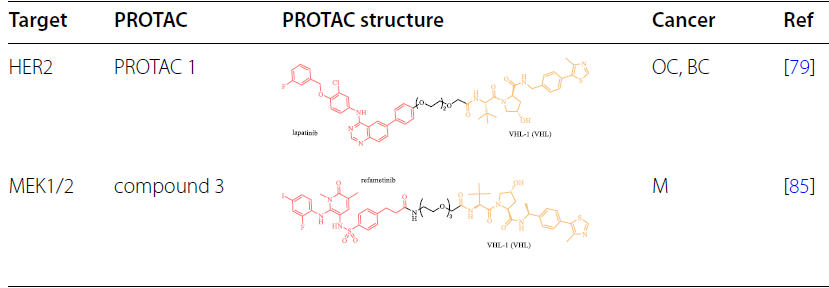
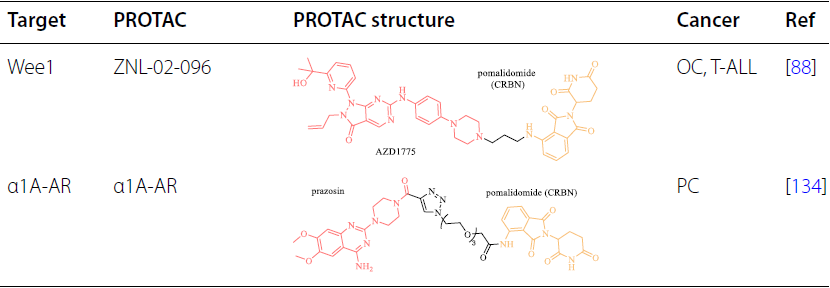
靶向细胞凋亡相关蛋白
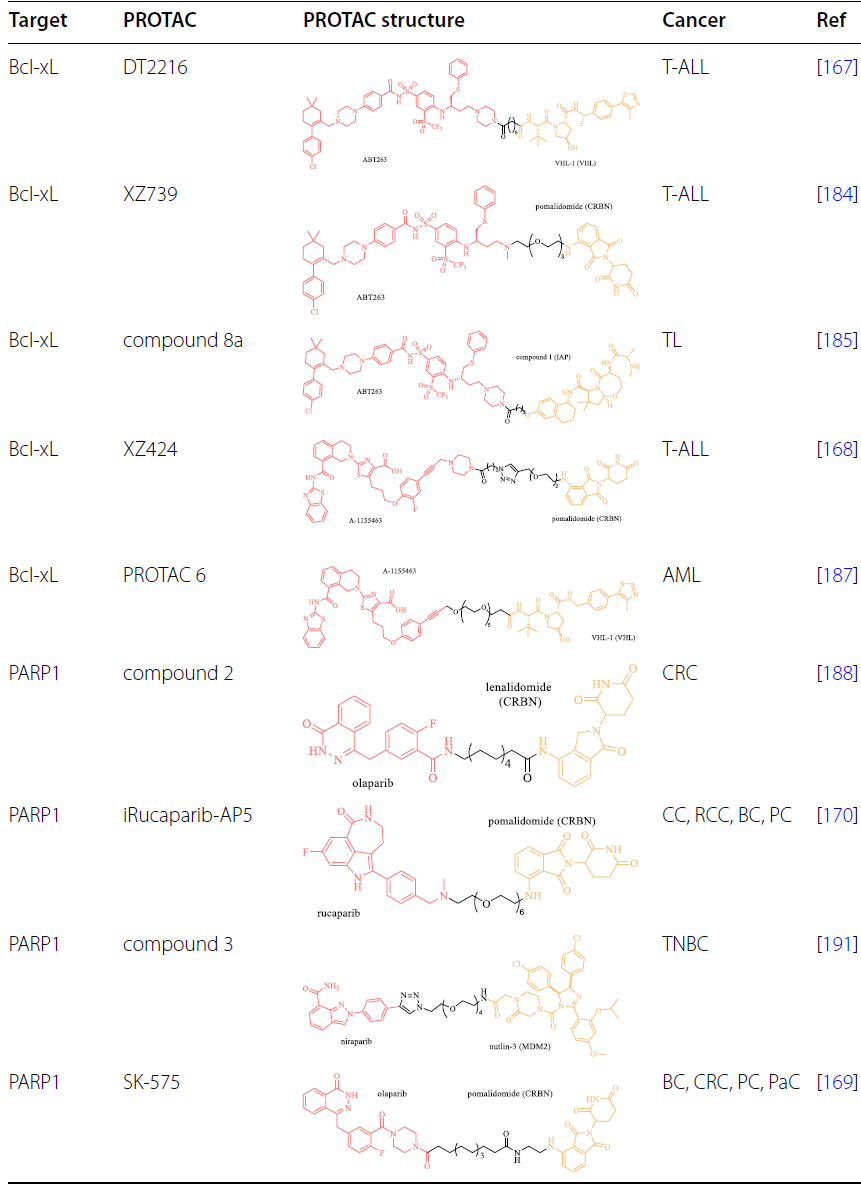
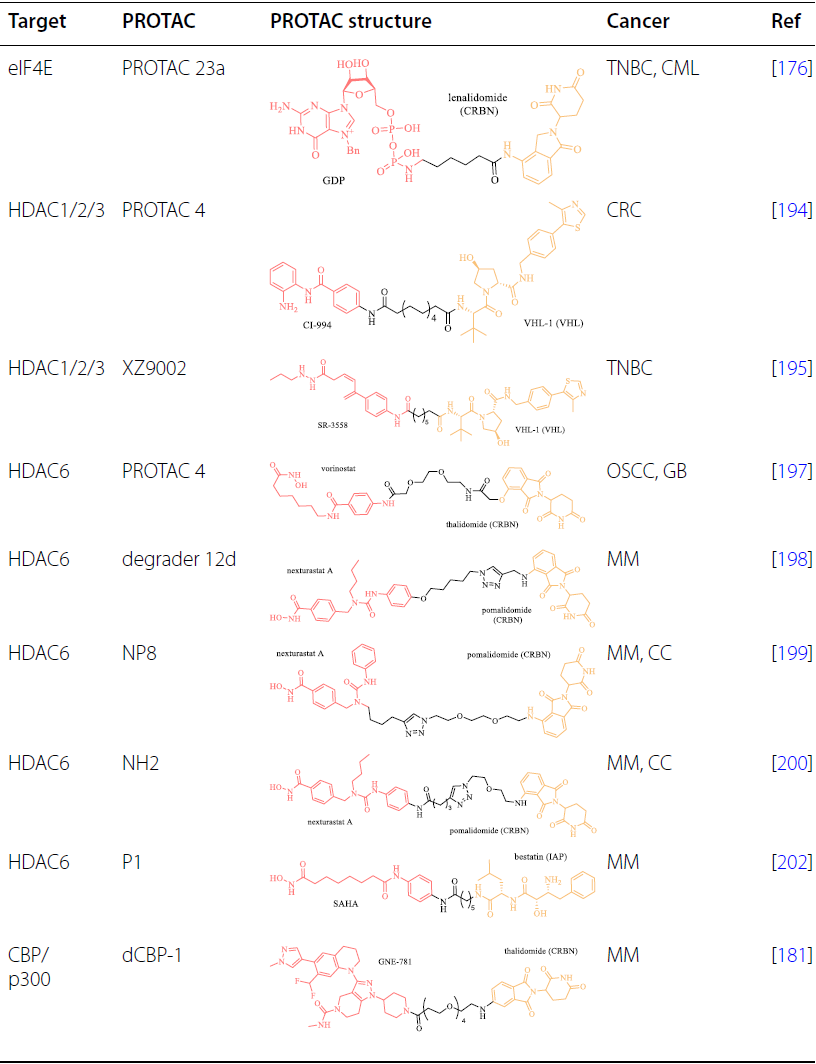
癌细胞可以通过上调抗凋亡蛋白(如 Bcl-2 和 Bcl-xL)或下调促凋亡因子(如 Puma、Bax)来逃避凋亡,从而支持它们的异常存活、治疗抗性和癌症复发。因此,通过利用PROTAC分子靶向调节凋亡相关蛋白,可以启动癌细胞的程序性细胞死亡。



靶向肿瘤血管生成相关蛋白
肿瘤需要产生新的血管系统来获得营养和氧气,以及排出代谢产物。血管生成是由激活多种生长因子表达的缺氧触发的,比较典型的是血管内皮生长因子(VEGF),这是一种关键的生长因子,可特异性识别血管内皮生长因子受体(VEGFR)以诱导新血管系统的形成。目前已经开发出阻断VEGF/VEGFR信号以抑制血管生成的PROTAC:

靶向免疫和炎症相关蛋白
为了存活,癌细胞通过重新编程涉及调节细胞(例如调节性T细胞)、B细胞受体 (BCR) 信号传导和T细胞受体 (TCR) 信号传导的肿瘤微环境来诱导炎症和免疫逃避。
免疫检查点抑制剂是一种治疗癌症的新兴疗法,可解除免疫抑制并实现免疫介导的肿瘤清除。然而,一些患者对免疫疗法具有先天性或获得性耐药性。为了克服这些问题,已开发出针对免疫和炎症的PROTAC:
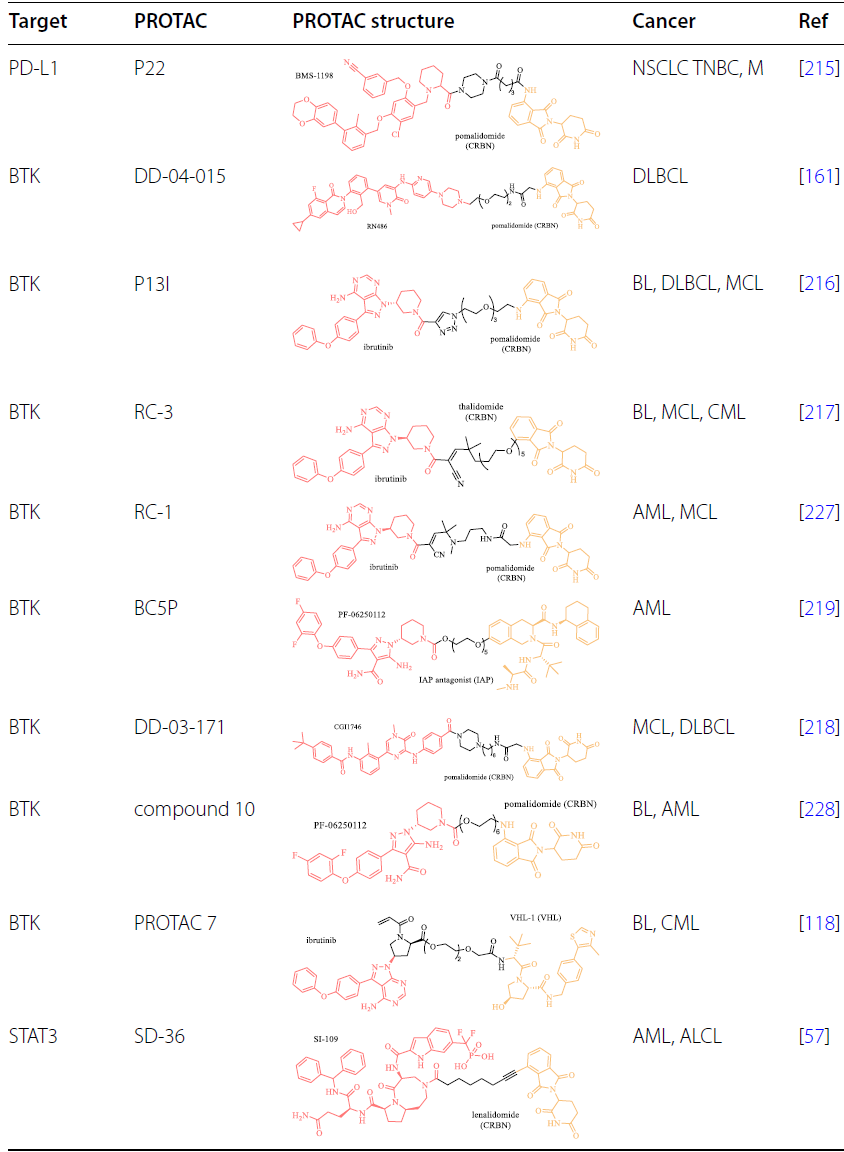

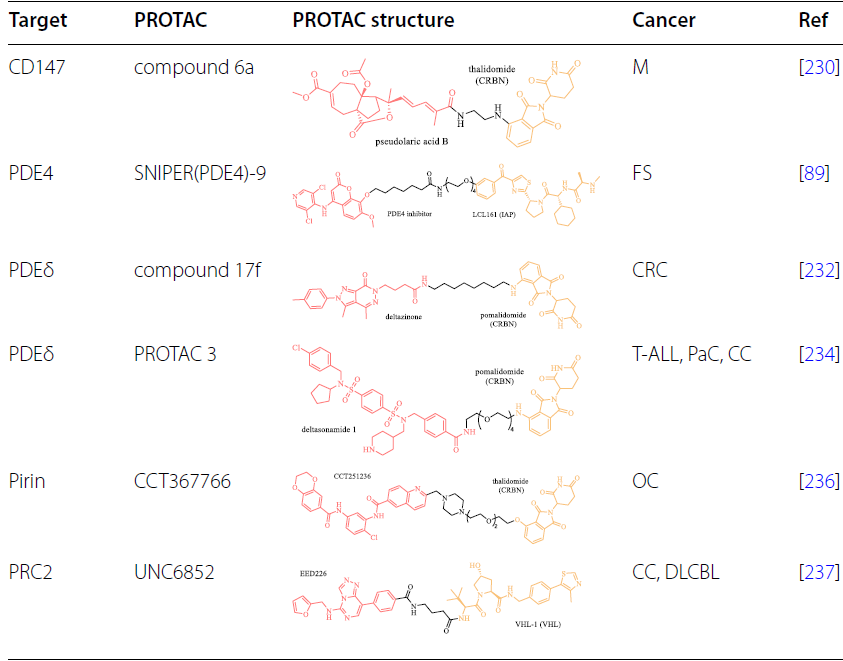

靶向肿瘤转移相关的信号通路
肿瘤细胞通过循环系统从原发灶外渗、扩散并成功定植远处器官以实现转移,导致了全球约90%的癌症死亡病例。上皮-间质转化 (EMT) 是癌转移过程中的关键步骤,可被包括整合素/FAK/PI3K/AKT轴在内的多种上游细胞信号通路激活。在过去的几十年中,针对EMT相关蛋白的PROTAC已被开发用于针对肿瘤转移。
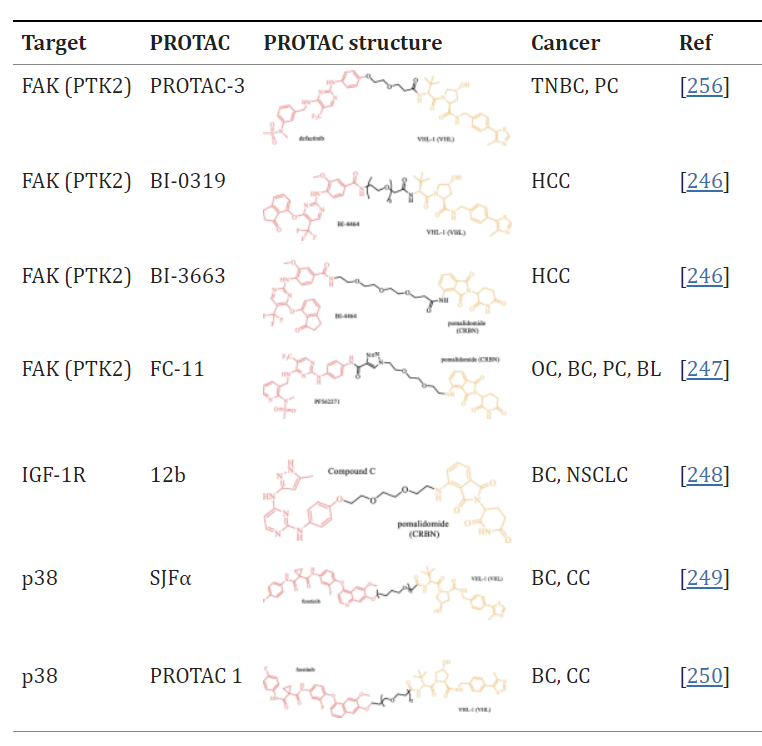
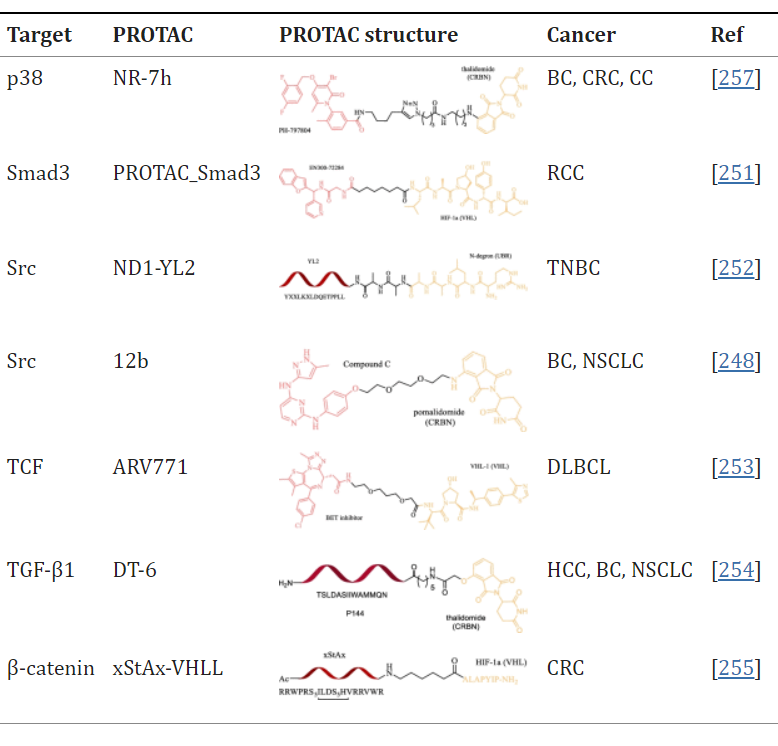
参考来源:
Li X, Pu W, Zheng Q, Ai M, Chen S, Peng Y. Proteolysis-targeting chimeras (PROTACs) in cancer therapy. Mol Cancer. 2022
<END>






































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论