
一、本周国内创新药/改良型新药注册申报分析
根据药融云数据统计,2022.06.20-2022.06.26期间共有56项创新药/改良型新药注册申请获CDE承办(按受理号统计,不含补充申请)。其中,国产药品受理号35个,进口药品受理号21个。本周共计19款创新药/改良型新药临床试验申请获得“默示许可”,其中值得关注的包括:
- DNV3
6月20日,国家药品监督管理局审评中心(CDE)官网公示,时迈药业申报的注射用DNV3的两项适应症均获得临床试验默示许可,拟联合特瑞普利单抗注射液用于复发/转移皮肤罕见肿瘤和用于晚期/转移性实体瘤和淋巴瘤。公开资料显示,DNV3是时迈药业开发的一款抗LAG-3单克隆抗体,LAG-3是一种免疫检查点受体蛋白,主要表达在活化的T细胞、NK 细胞、B细胞和浆细胞树突细胞。LAG-3主要通过与配MHC II 分子的结合,下调T细胞的活性,同时其还可增强调节性T细胞的抑制活性。所以DNV3可精准调控包括T、 B、NK及DC等多类免疫细胞的功能,单药治疗具有显著抗肿瘤药效。同时,DNV3与化疗、小分子靶向药及 PD-1 免疫检查点抑制剂联用可进一步协同提高抗肿瘤药效。
- IBI363
6月20日,国家药品监督管理局审评中心(CDE)官网公示,信达生物1类新药IBI363获得临床试验默示许可,拟开发适应症为晚期肿瘤。公开资料显示,IBI363是将突变IL-2细胞因子与抗PD-1抗体融合的融合蛋白,其作用机制是将IL-2通路刺激与PD-1免疫检查点阻断相结合,从而治疗恶性肿瘤。该药目前正在澳大利亚开展一项1期临床试验,针对晚期恶性实体瘤和淋巴瘤受试者。
- EXG001-307
6月22日,国家药品监督管理局审评中心(CDE)官网公示,杭州嘉因生物自主研发的AAV基因疗法EXG001-307注射液获得临床试验默示许可,拟用于治疗1型脊髓性肌萎缩症(1型SMA),伴有存活运动神经元1(SMN1)基因的双等位基因突变(缺失)。公开资料显示,EXG001-307注射液是中国境内首个被批准进入注册临床试验的静脉注射治疗1型SMA的基因治疗产品。EXG001-307注射液是将正常表达SMN蛋白的转基因装载在AAV9病毒载体中,提高它生成 SMN 蛋白的能力。让患者接受一次治疗之后,能够在细胞中长期表达SMN蛋白,从而达到“治愈性”效果。
- Donanemab
6月25日,国家药品监督管理局审评中心(CDE)官网公示,礼来公司的donanemab注射液获得临床试验默示许可,拟用于早期症状性阿尔茨海默病,包括阿尔茨海默病所致的轻度认知障碍以及轻度阿尔茨海默病。公开资料显示,donanemab是礼来开发的一款与β淀粉样蛋白亚型N3pG结合的单克隆抗体,它能够与阿尔茨海默病患者大脑中淀粉样蛋白沉积中的β淀粉样蛋白结合,从而促进患者大脑中淀粉样蛋白沉积的清除。此前礼来已经启动向美国FDA递交该药的滚动申请,寻求FDA的加速批准。
- PF-06730512
6月25日,国家药品监督管理局审评中心(CDE)官网公示,辉瑞公司的1类新药注射用PF-06730512获得临床试验默示许可,用于局灶节段性肾小球硬化(FSGS)。公开资料显示,注射用PF-06730512是辉瑞开发的含ROBO2配体陷阱(ligand trap)的创新生物制品。配体陷阱是一种重组分子,包含相关配体结合结构域,能以高特异性和高亲和力结合其相应的细胞因子。注射用PF-06730512能够改善肾脏足细胞的功能,开发用于治疗多种和足细胞相关的蛋白尿性肾小球疾病。目前,该产品在全球正处于2期临床研究阶段,拟开发用于治疗一种罕见进行性肾病。
- JDB175片
6月25日,国家药品监督管理局审评中心(CDE)官网公示,嘉葆药银的JDB175片获得临床试验默示许可,拟用于多发性硬化(Multiple Sclerosis,MS)。JDB175片是嘉葆药银自主研发的一类小分子创新药,是一个具有高选择性的第二代布鲁顿氏酪氨酸激酶(BTK)口服抑制剂,公开资料显示JDB175与同类药物相比,具有良好的BTK选择抑制性,且安全性与耐受性表现良好。
本周无新药获批上市。
获批临床创新药/改良型新药信息速览(不含补充申请)
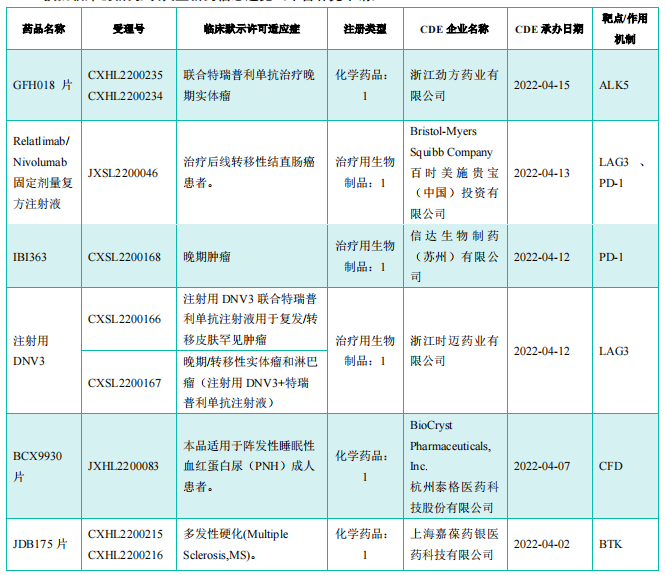

截图来源:《药融云医药行业观察周报》
备注:更多信息如获批临床/获批上市品种全球上市及研发进展详情及相关靶点全局分析等,可通过药融云投融资数据库和(或)联系药融云客服获取并下载 EXCEL 表格。
二、仿制药/生物类似物注册申报分析
根据药融云数据统计,2022.06.20-2022.06.26共有77项仿制药注册申请获CDE承办,其中新注册分类上市申请受理号52项(包括化药3类,4类,5.2类),一致性评价申请受理号25项;共13个品种通过一致性评价仿制药(按受理号计20项),27个品种视同通过一致性评价(按受理号计41项)。本周无生物类似物注册申报动态。
- 本周通过/视同通过一致性评价全局分析
通过一致性评价:本周过评品种主要集中在系统用抗感染药治疗领域,过评产品剂型主要为注射剂,还包括片剂和胶囊剂;本周过评受理号数量TOP2品种分别为注射用头孢呋辛钠和伊班膦酸钠注射液,其中过评企业最多的品种为注射用头孢呋辛钠,共有3家企业,分别为国药集团致君(深圳)制药、珠海经济特区粤康医药和齐鲁安替制药;本周过评企业涉及四川美大康佳乐药业、湖南明瑞制药、上海信谊百路达药业和遂成药业等15家企业。
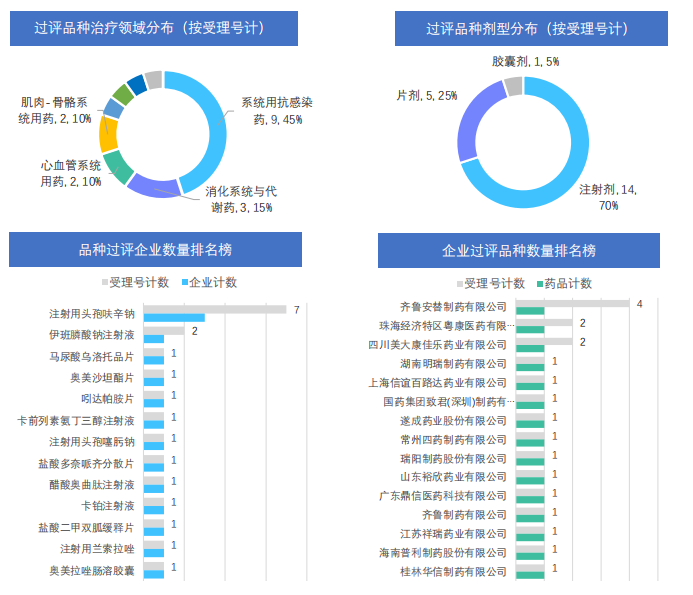
截图来源:《药融云医药行业观察周报》
视同通过一致性评价:本周视同通过的品种主要集中在系统用抗感染药、消化系统与代谢药和神经系统用药三大治疗领域,共计占比近60%;本周包括视同通过的剂型主要为片剂和注射剂,还包括吸入剂、口服混悬剂和乳剂等6种剂型;从品种层面来看,维格列汀片、奥硝唑注射液和左氧氟沙星注射液为过评企业较多的品种,其中维格列汀片共有3家企业视同通过;从企业层面来看,成都倍特药业和石家庄四药在本周领跑,尤其成都倍特在本周收获颇丰,共过评4个品种,分别为伏立康唑片、头孢呋辛酯干混悬剂、氨甲环酸注射液和苯溴马隆片,成都倍特药业不仅拿下了头孢呋辛酯干混悬剂的首家过评,还是苯溴马隆片过评的第3家企业,而石家庄四药则过评3个品种,包括对乙酰氨基酚甘露醇注射液、布南色林片和左氧氟沙星注射液,同时石家庄四药也是布南色林片的首家过评企业。
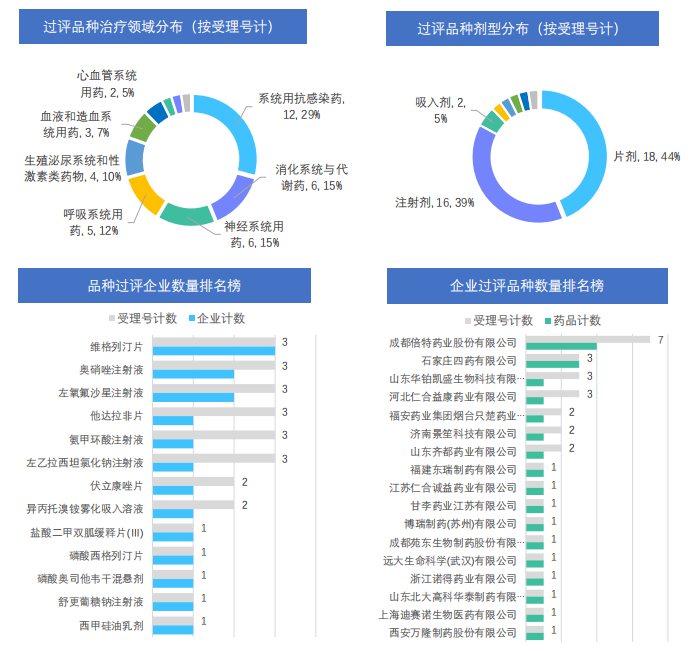
截图来源:《药融云医药行业观察周报》
- 本周首次过评/视同过评及过评/视同过评达3家品种盘点
(1)本周首次过评/视同过评品种

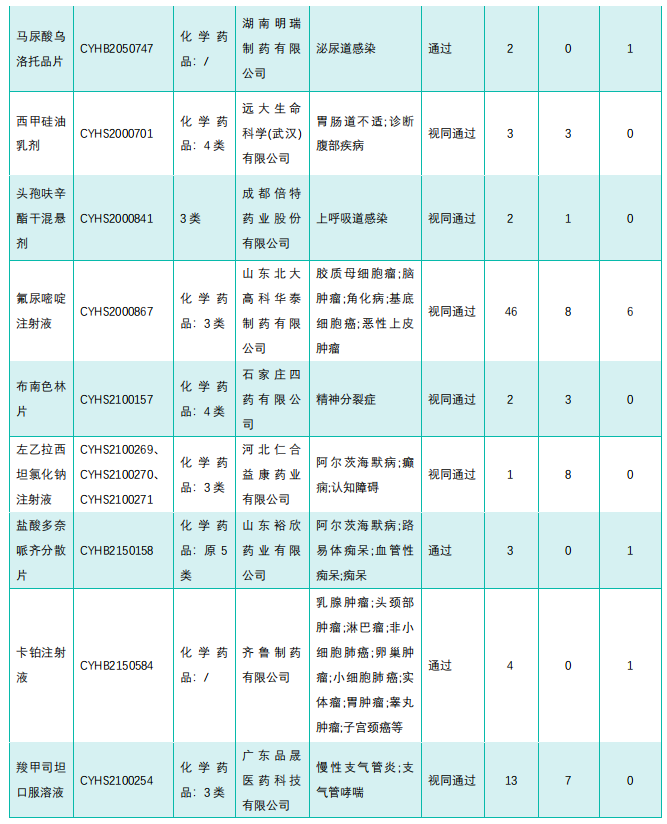
截图来源:《药融云医药行业观察周报》
(2)本周过评/视同过评达3家企业品种

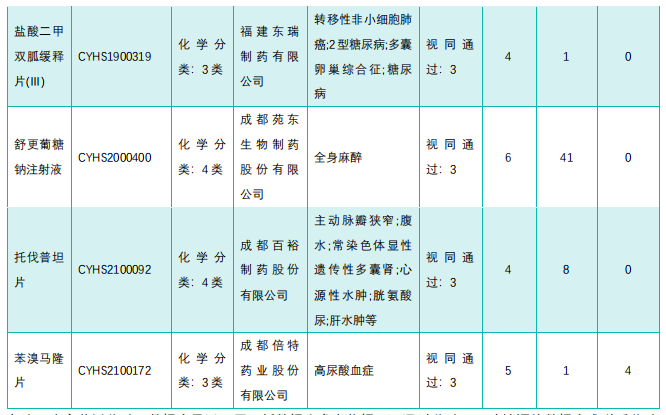
截图来源:《药融云医药行业观察周报》
备注:本章节以药融云数据库最近一周更新数据为参考依据,可通过药融云一致性评价数据库或联系药融云客服获取并下载本周过评/视同过评品种清单。
三、全球医药大健康行业投融资事件盘点
据药融云数据统计,2022年6月20日-6月26日间,全球医药大健康行业共发生投融资事件64起,较上周数量增加了4起,其中创新药类融资共14起,医疗服务投资热度也较高,本周占比为22%,为14起。国内医药大健康行业共发生投融资事件25起,较上周数量增加了4起,其中创新药类为4起,医疗器械、医药制造/服务、医疗服务、医疗/医药信息技术融资事件发生数量分别为8起、2起、5起和1起。本周国内创新药大类中,人工智能技术新药开发、疫苗研发及基因细胞药物开发为热点。从融资金额来看,西湖生物医药科技、华深智药和圆因生物融资金额在1亿元人民币以上。
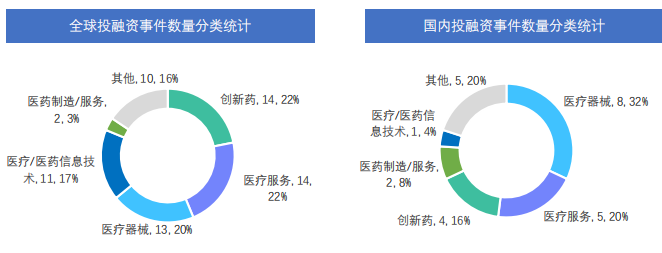
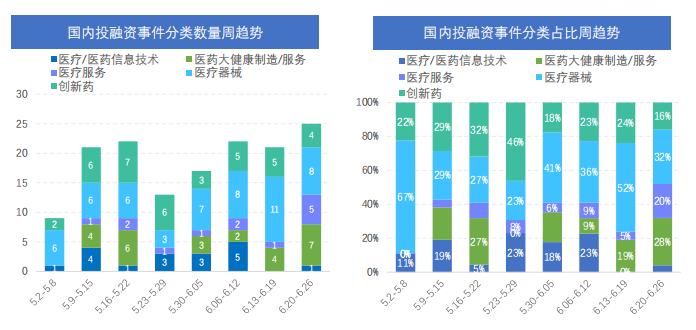
截图来源:《药融云医药行业观察周报》
国内医药大健康行业投融资速览

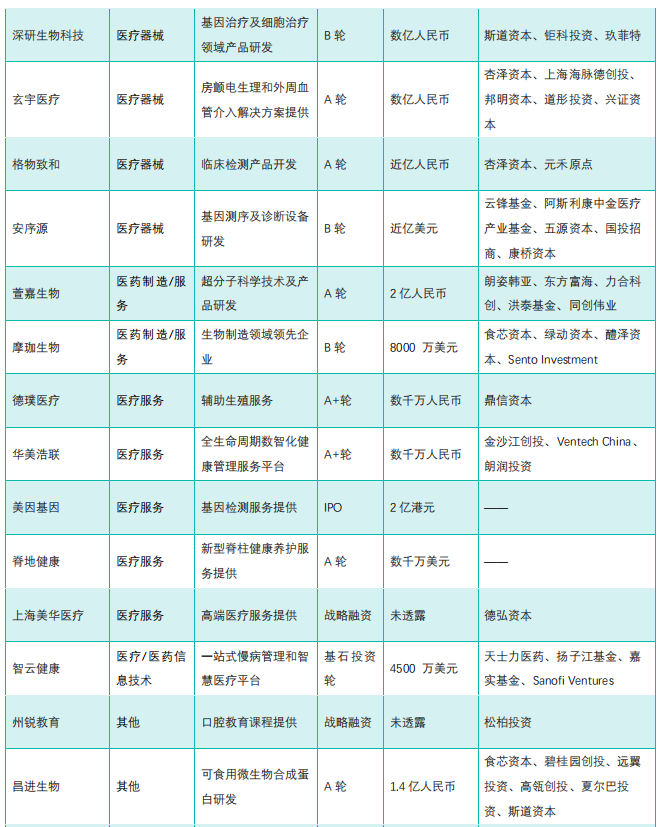
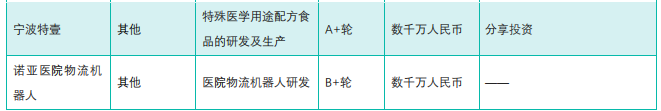

截图来源:《药融云医药行业观察周报》
备注:更多信息如公司简介、历史融资信息、所在地区、最新融资时间等,可通过药融云投融资数据库和(或)联系药融云客服获取并下载 EXCEL 表格。
大额创新药投融资事件详细说明
近日,新一代细胞治疗技术开发商西湖生物医药宣布完成超亿元A+轮融资,本轮融资由倚锋资本领投,翱鹏投资、西湖科创、西湖创新投资跟投。本轮融资款项将主要用于公司红细胞平台多治疗领域管线推进,并加速公司红细胞产品的临床验证及IND申报,进一步完善及扩展公司的团队。
西湖生物医药公司基本信息及投融资情况
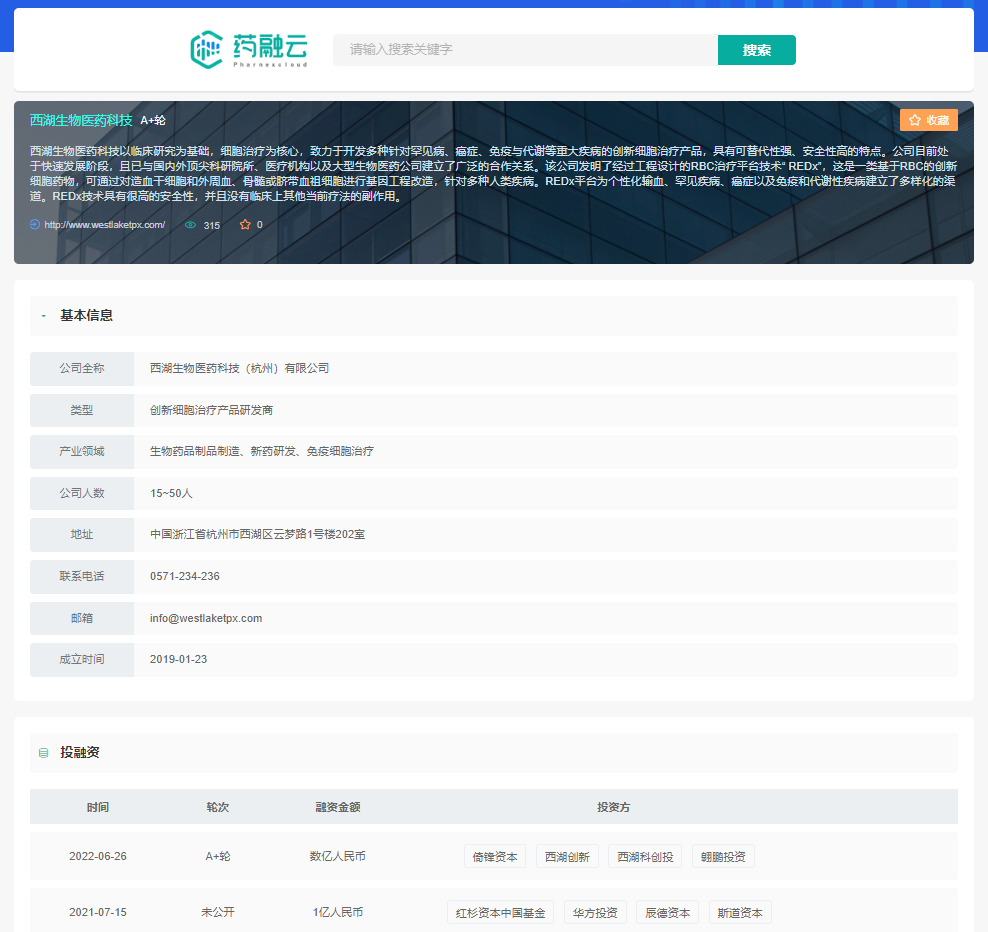
截图来源:药融云投融资数据库
近日,华深智药(Helixon)宣布完成近5亿元A轮融资。本轮融资由五源资本领投,高榕资本、Neumann Capital以及三家天使轮投资方襄禾资本、高瓴创投、清智资本跟投。华深智药将继续深耕于AI+新药开发领域,扩大团队与商务开发,完善AI高性能计算能力,拓展高通量实验平台,并同时推进管线自主研发与对外合作。
华深智药公司基本信息及投融资情况
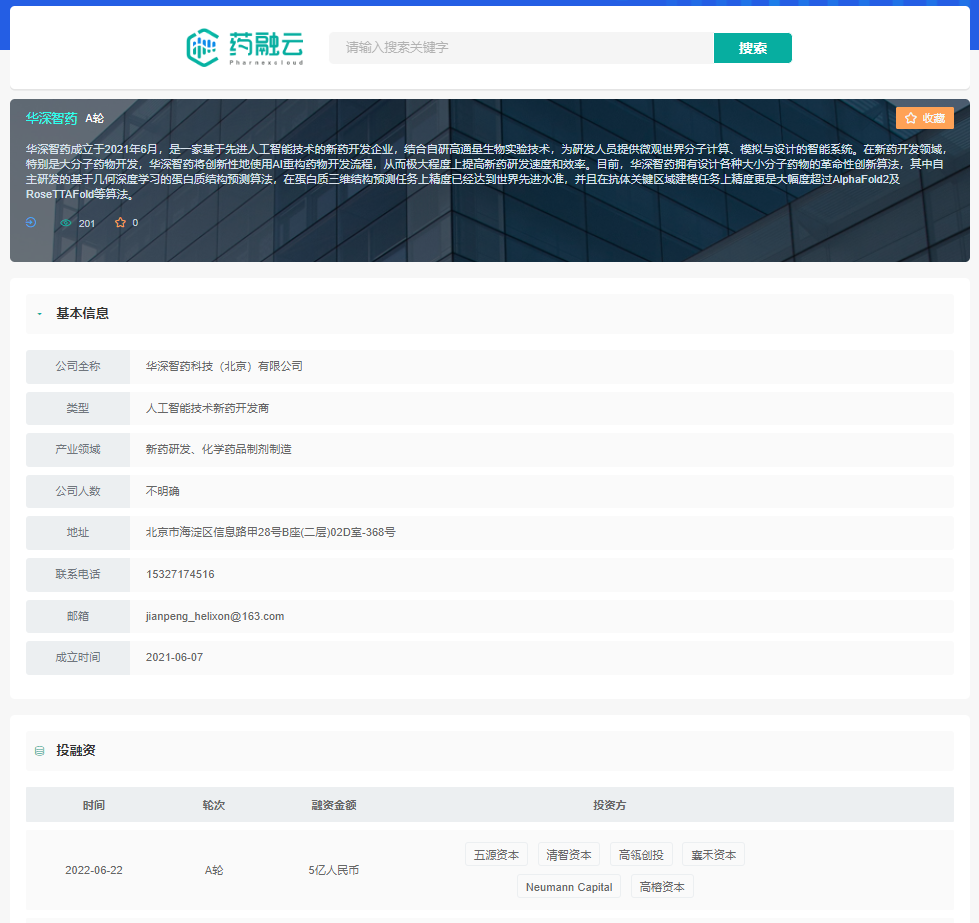
截图来源:药融云投融资数据库
2022年6月21日,专注于国际前沿环状RNA技术开发新型疫苗及多个新型治疗领域的圆因生物(Therorna Inc.),宣布顺利完成超过2.8亿元人民币A轮融资。本次融资由某知名产业投资机构与和玉资本联合领投,夏尔巴投资与三正健康投资跟投,老股东泉创资本与千骥资本也继续追加投资,鼎力支持公司发展。本轮融资后,将加快推进技术平台建设、管线产品研发、临床试验和注册申报及国际合作等。
圆因生物公司基本信息及投融资情况
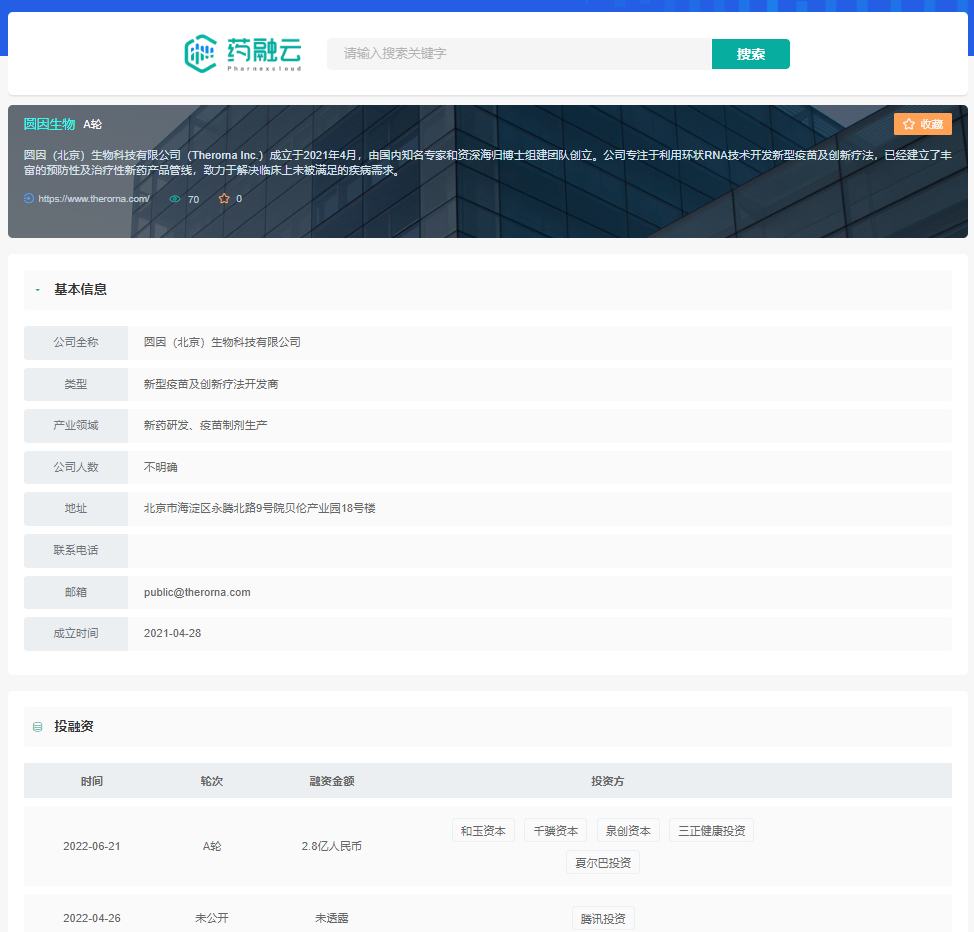
截图来源:药融云投融资数据库
四、国内创新药研发进展
1.三生国健纳乐舒单抗注射液申报上市
6月22日,CDE 官网显示,三生国健1类生物制品纳乐舒单抗注射液提交上市申请并获受理。三生国健的纳乐舒单抗是第2个申报上市的国产CD20单抗,用于治疗非霍奇金淋巴瘤。
2.荣昌生物泰它西普SLE III期临床完成首例患者入组给药
23日,荣昌生物宣布其全球首款、同类首创BLyS/APRIL双靶点新型重组TACI-Fc融合蛋白新药泰它西普,用于治疗系统性红斑狼疮的全球多中心Ⅲ期临床试验,已在美国顺利完成首例受试者入组给药。
3.正大天晴TQ-B3101胶囊上市申请获受理
23日,CDE官网显示,正大天晴TQ-B3101胶囊的上市申请获受理。TQ-B3101是一款靶向ALK/ROS1/MET的新型小分子受体酪氨酸激酶抑制剂。临床前研究显示,该药物具有较好的抗肿瘤活性和疗效持续时间。
4.宜明昂科CD70单抗申报临床
24日,CDE官网显示,宜明昂科的IMM40H注射液临床试验申请获受理,用于治疗液体或实体瘤。这是国内第3款申报临床的CD70单抗。CD70属于肿瘤坏死因子超家族成员,是一种II型跨膜糖蛋白,需与其受体 CD27结合发挥作用。
5.星汉德生物首次公布SCG101临床试验最新研究
23日,在EASL年会暨2022年国际肝脏大会上,星汉德生物首次公布了SCG101治疗乙型肝炎病毒相关肝细胞癌患者的临床试验最新研究。该研究的初步数据显示,SCG101在缺乏有效治疗手段的晚期乙肝病毒相关性肝癌患者中展现出良好的安全性及初步疗效;研究表明,SCG101具有显著的抗病毒和抗肿瘤活性,血清HBsAg快速、持续的降低,疾病控制率达到66%。
6.信立泰DPP-4抑制剂3期临床取得初步数据
24日,信立泰宣布,其用于治疗糖尿病的在研创新药苯甲酸复格列汀片3期临床研究已经完成揭盲并取得初步的统计分析结果。在进行两项随机、双盲的3期临床研究后结果显示,无论是单药治疗还是联合二甲双胍治疗2型糖尿病患者,在给药24周后,苯甲酸复格列汀片对比安慰剂都能显著地降低HbA1c,具有明显的降糖效果。
......
药物的研发是一个极其复杂、费时费力的事情,实时掌握每周医药行业内发生的大小事,对药物的研发有很大的帮助。全面了解市场研发动态,随时跟进药企产品研发进展,及时发现医药行业新契机,研发人员也能站在时讯的至高点,随机应变,及时调整研发策略与方向,知己知彼、少走弯路、统筹全局、运筹帷幄。

药融云咨询团队联合药学数据分析团队每周将会准时推出药融云《医药行业观察周报》,内含一周内医药行业核心数据回顾、行业政策要闻、全球创新药研发进展、本周全球积极/失败临床结果、全球医药企业 BD 交易/战略合作事件盘点、国内上市企业动态、国内医药企业国际化动态等动态。

以上为2022.06.20-2022.06.26期间医药行业发生事件的部分内容,想要获取药融云《医药行业观察周报》完整报告,关注“药融云”公众号(gh_d20f87bd52d9),回复关键词“报告”即可领取。
药融云2022.06.20-2022.06.26医药行业观察周报目录


<END>








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论