引言
CDE审理情况一览
12月13日-12月19日CDE共受理国产和进口临床/上市申请131个。其中,上市注册申请68个,临床试验申请77个,以及一致性评价受理31个。在131个受理号中,1类药品最多占68个,2类药品12个,3类药品25个,4类药品22个,5类药品5个。(文中统计结果不包括补充申请&进口再注册)
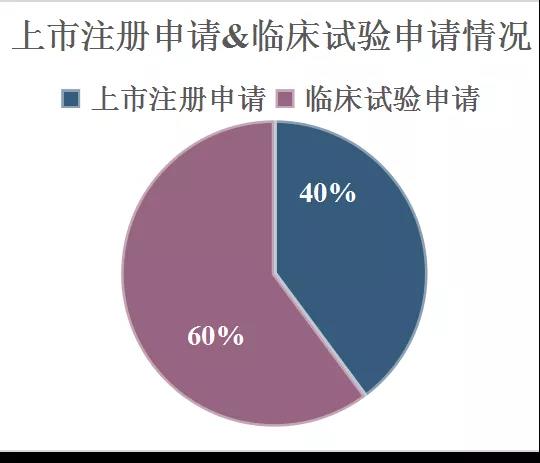
图1.上市注册申请&临床试验申请情况

图2.所承办药品注册分类情况
注册分类:1类
创新药
1类新药受理号收审情况:

注
64个1类新药受理号由42家公司申报,囊括39种药品。其中化药受理号48个,生物制品受理号16个,无中药受理号。其中,重组抗HER2结构域Ⅱ和结构域Ⅳ双特异性抗体是轩竹生物首个1类生物制品。
注册分类:2类
改良型新药
2类新药受理号收审情况:
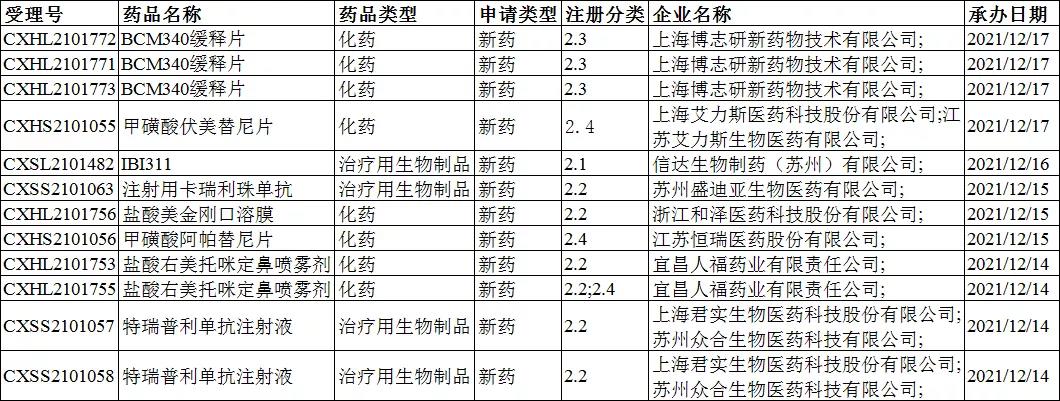
注
12个2类新药受理号由9家公司申报,囊括8种药品。其中化药受理号8个,生物制品受理号4个,无中药受理号。
注册分类:3类
中药:古代经典名方中药复方制剂
生物制品:境内或境外已上市生物制品/疫苗
化药:境内申请人仿制境外上市但境内未上市原研药品的药品
3类药品受理号收审情况:
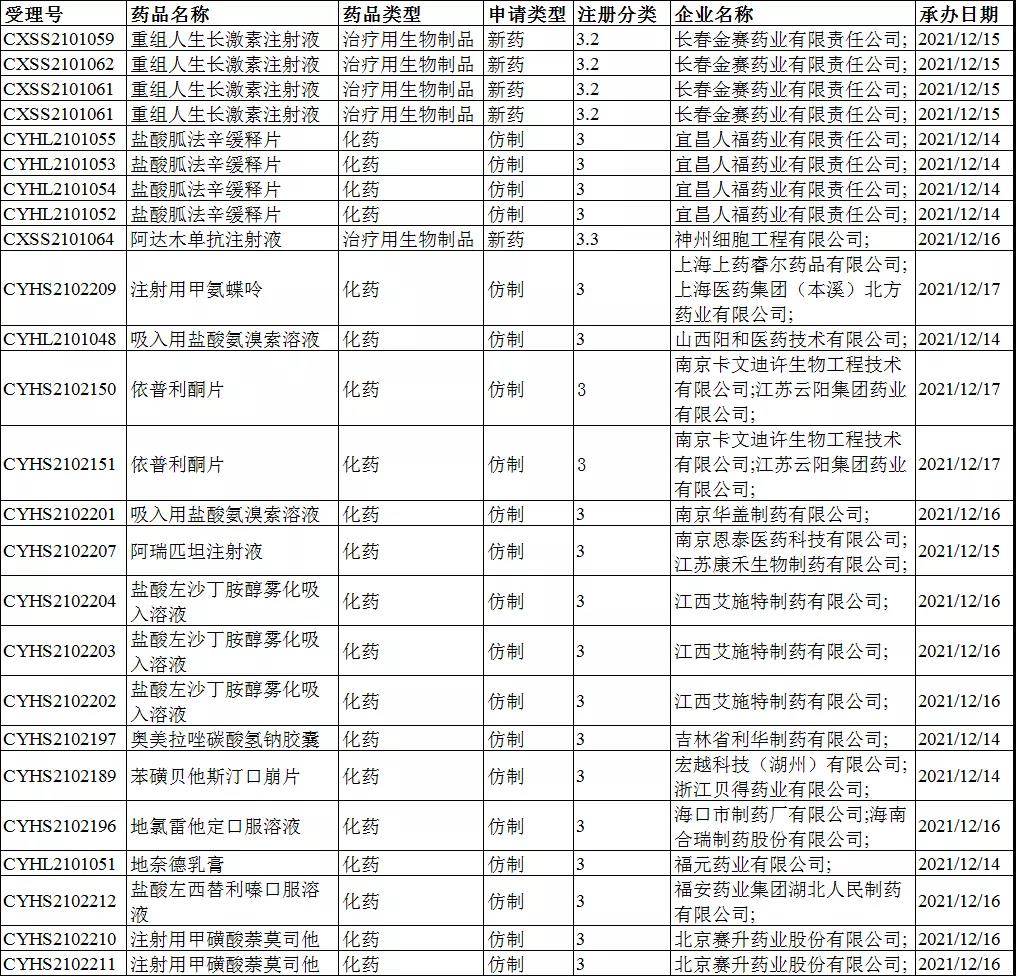
注册分类:4类
中药:中药同名同方药
化药:境内申请人仿制已在境内上市原研药品的药品
4类药品受理号收审情况:

注册分类:5类
境外已上市境内未上市化学药品
5类药品受理号收审情况:
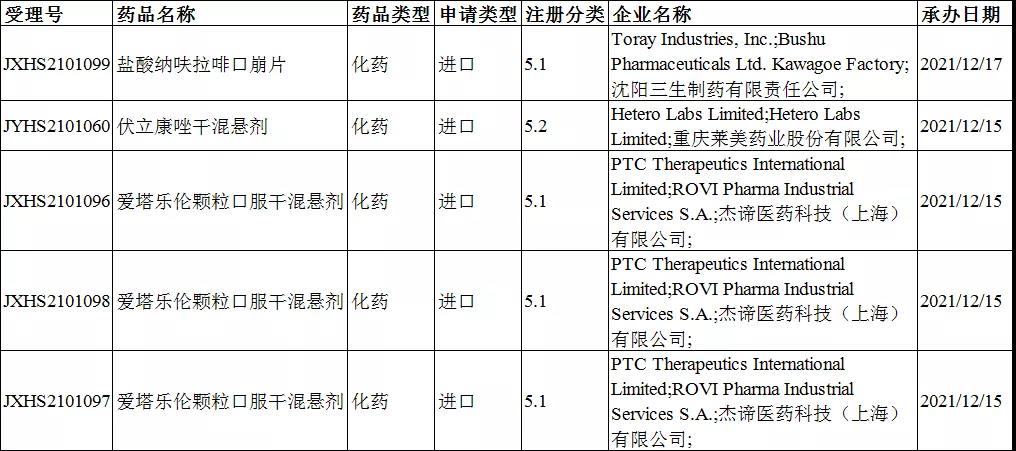
一致性评价受理情况
一致性评价受理情况:







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论