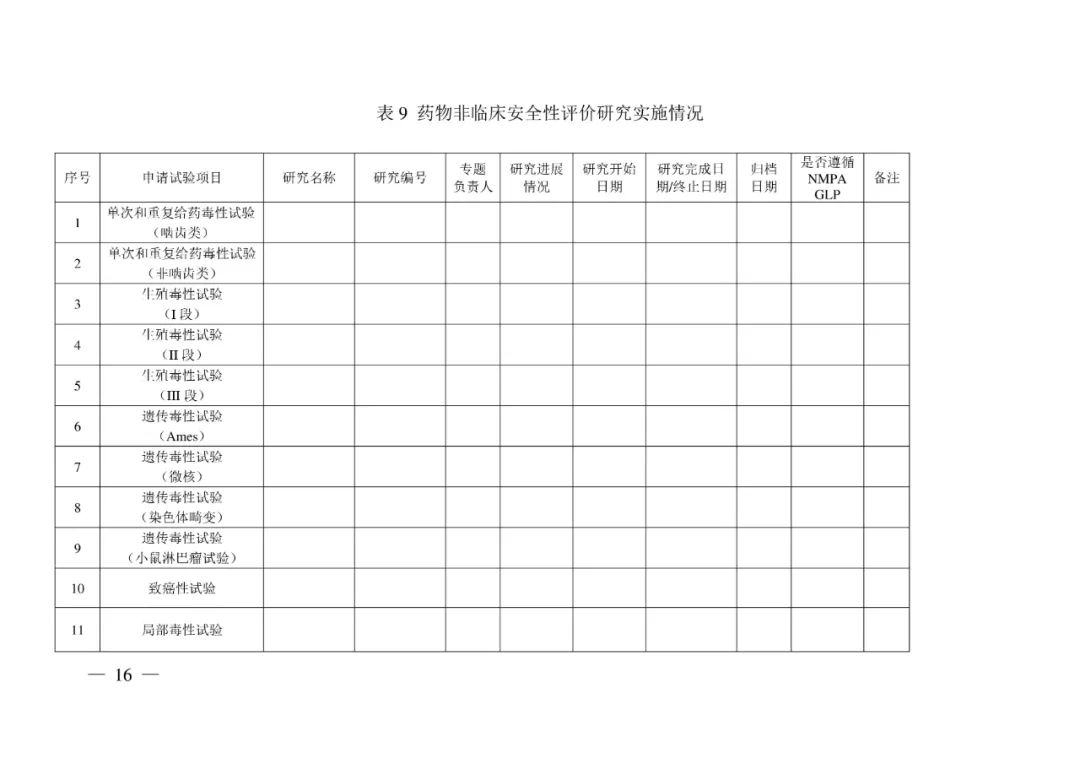
4月24日,国家药品监督管理局食品药品审核查验中心(CFDI)发布《药物非临床研究质量管理规范认证申请资料要求》,自2023年7月1日起施行。
原文如下:

按照《药物非临床研究质量管理规范认证管理办法》规定,为明确药物非临床研究质量管理规范认证申请资料要求,国家药品监督管理局食品药品审核查验中心组织制定了《药物非临床研究质量管理规范认证申请资料要求》(见附件),经国家药品监督管理局同意,现予发布,自2023年7月1日起施行。
特此通告。
附件:药物非临床研究质量管理规范认证申请资料要求.doc
国家药监局核查中心
2023年4月24日







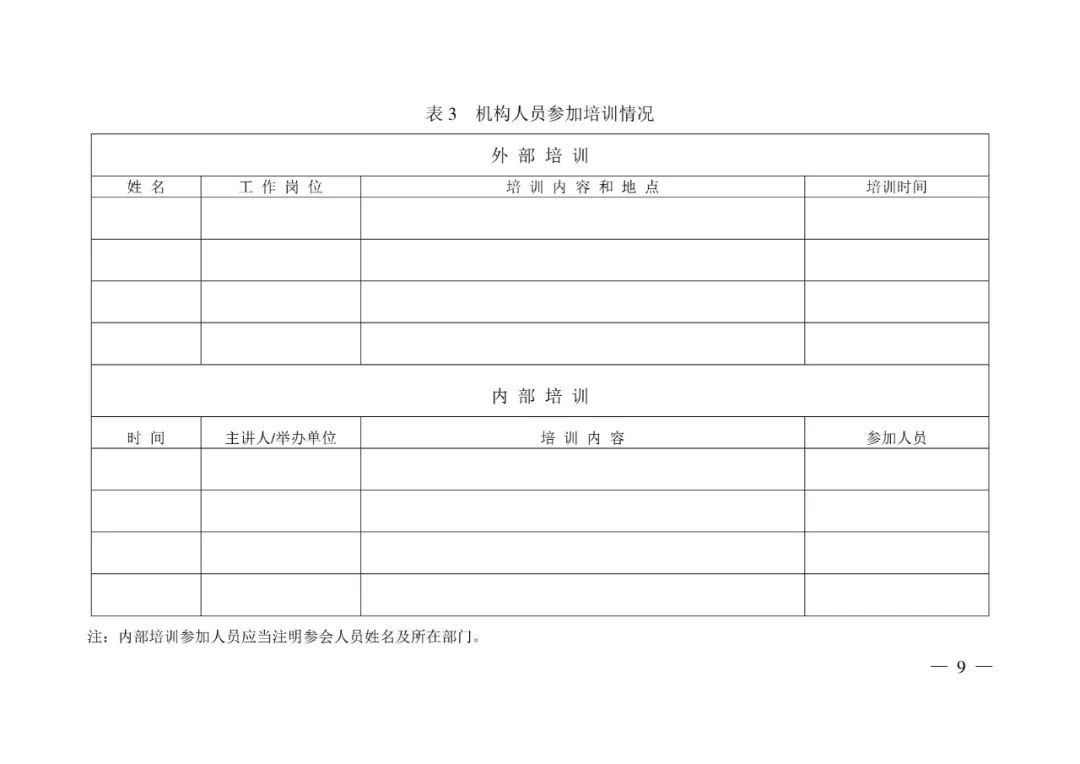
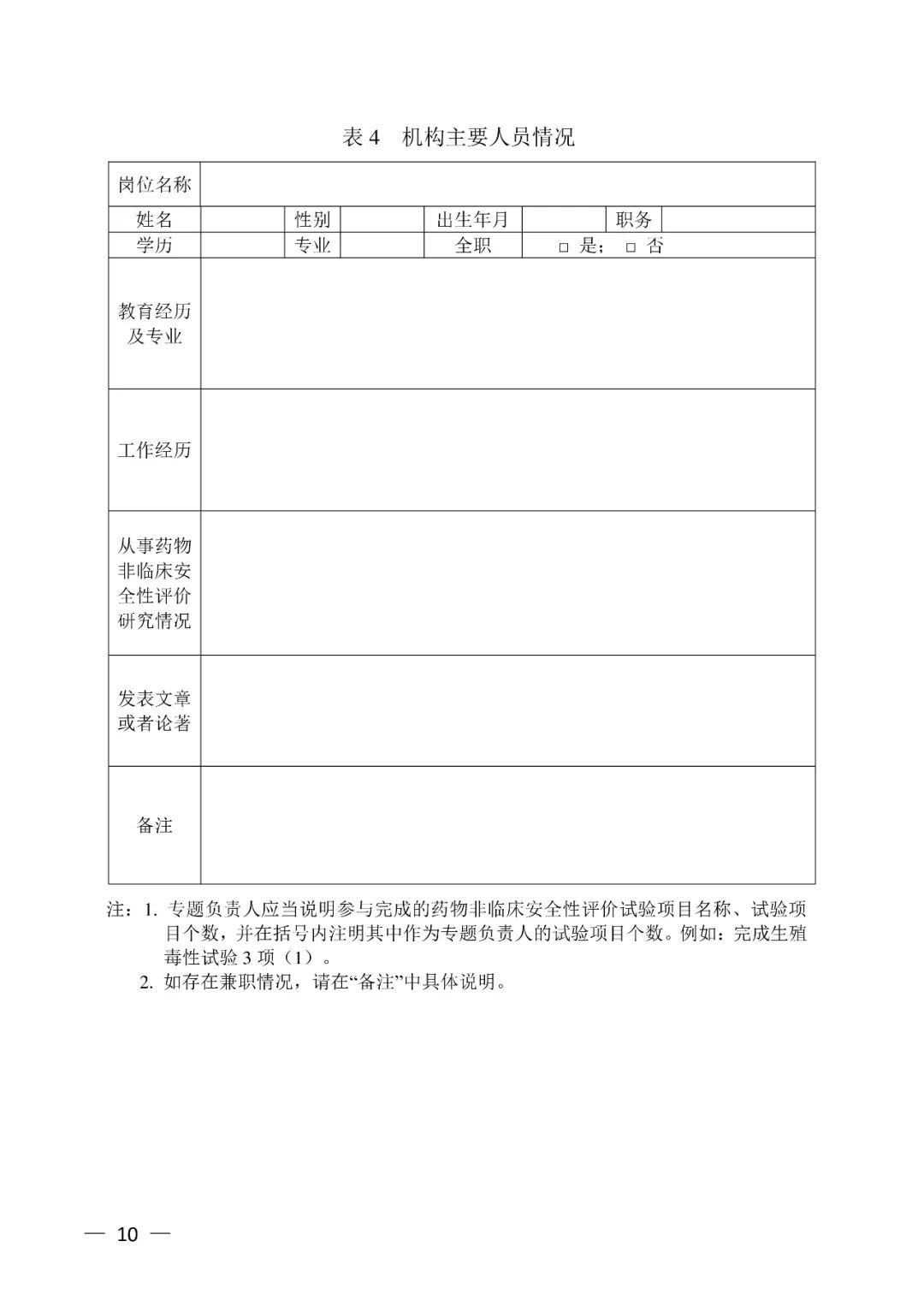

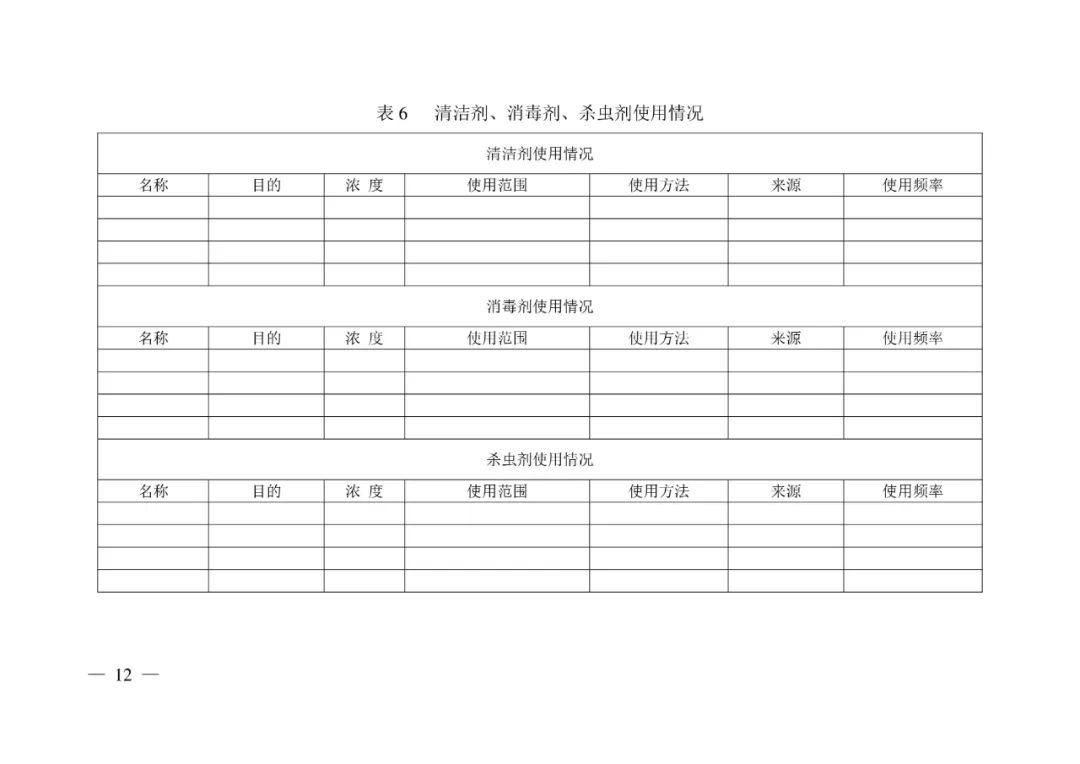
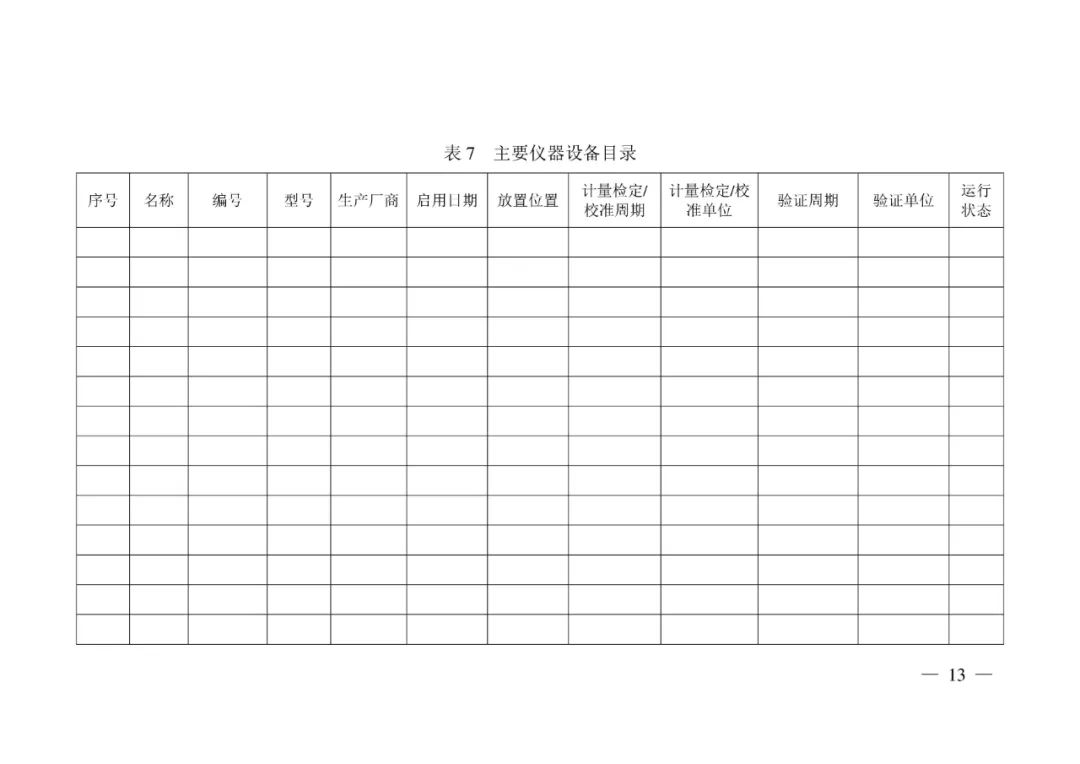



<END>






































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论