
2024年5月28日,康宁杰瑞宣布在未接受系统性治疗的不可切除局部晚期或转移性胰腺导管腺癌(PDAC)患者中,评估其自主研发的PD-L1/CTLA-4双特异性抗体KN046联合白蛋白紫杉醇及吉西他滨对比安慰剂联合白蛋白紫杉醇及吉西他滨的疗效及安全性的III期KN046-303研究已经达到预设的死亡事件数,总生存期(OS)结果未达到预设的统计学终点。

受此消息影响,截至目前公司股价已大跌40%。
关于KN046
KN046,由康宁杰瑞自主研发,是一款拥有完全自主知识产权的PD-L1/CTLA-4双特异性抗体。该药物的创新之处在于其独特的设计:将机制各异的CTLA-4和PD-L1单域抗体进行融合,形成一种新型的双功能分子。KN046能够精准靶向并富集在PD-L1高表达的肿瘤微环境中,同时有效清除那些抑制肿瘤免疫反应的调节性T细胞(Treg细胞)。
目前,KN046正联合化疗用于一线治疗鳞状非小细胞肺癌(NSCLC)和胰腺癌,这两项研究均已进入关键的三期临床试验阶段,此次为一线治疗胰腺癌三期临床的失败。
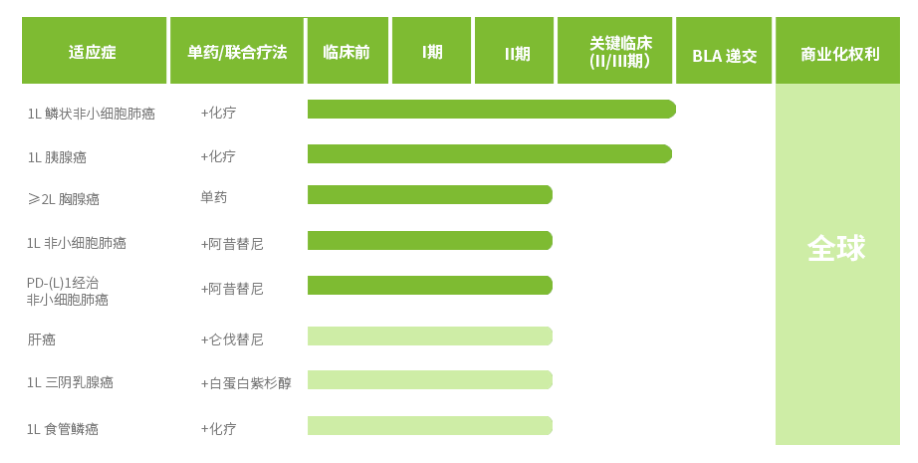
KN046已在澳大利亚、美国和中国针对非小细胞肺癌、胰腺癌、胸腺癌、肝癌、食管鳞癌、三阴乳腺癌等超过10种肿瘤类型,开展了近20项覆盖不同阶段的临床试验。这些试验的结果均表明,患者在使用KN046后展现出了显著的生存获益优势。基于在澳大利亚和中国取得的显著临床成果,美国FDA特别批准了KN046在美国直接进入II期临床试验阶段。此外,KN046于2020年9月还获得了美国FDA授予的用于治疗胸腺上皮肿瘤的孤儿药资格。目前,KN046的多项注册临床试验正在进行中,其中一项KN046联合化疗一线治疗非小细胞肺癌的III期临床研究,中期分析已成功达到了预设的PFS(无进展生存期)终点,预示着其在非小细胞肺癌治疗领域的巨大潜力。
关于KN046-303研究
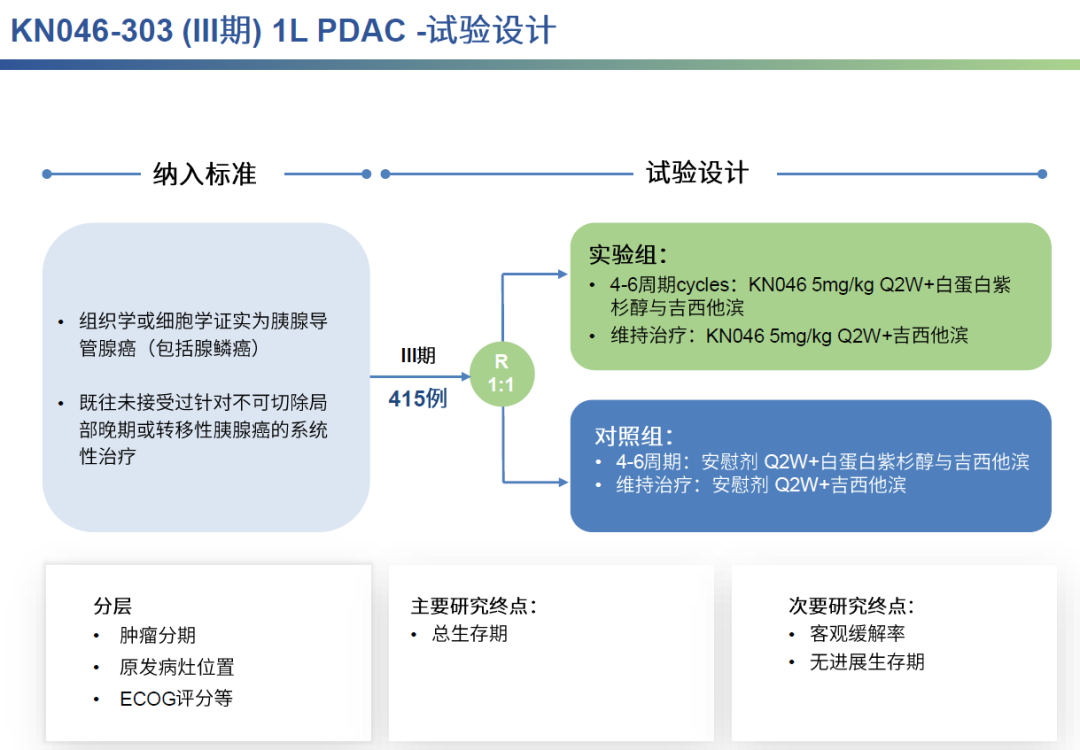
KN046-303是一项精心设计的多中心、随机、双盲、安慰剂对照的III期临床试验,专门针对未接受系统性治疗的不可切除局部晚期或转移性PDAC(胰腺导管腺癌)患者。该试验旨在全面评估KN046联合白蛋白紫杉醇及吉西他滨与安慰剂联合白蛋白紫杉醇及吉西他滨相比的疗效及安全性。研究的主要重点为总生存期,次要终点为客观缓解率和无进展生存期。
令人瞩目的是,今年2月,康宁杰瑞宣布,其PD-L1/CTLA-4双特异性抗体KN046与白蛋白结合型紫杉醇联合一线治疗晚期三阴乳腺癌的II期临床研究结果,已在国际顶级期刊《Nature Communications》(最新SCI影响因子16.6,JCR 1区)上在线发表。该研究表明,KN046与白蛋白结合型紫杉醇的联合治疗方案为三阴乳腺癌患者带来了显著的无进展生存期(PFS)和总生存期(OS)的延长,且耐受性良好,安全性可控,为晚期三阴乳腺癌的治疗提供了新的希望。

总结
截至目前,全球共有12款双抗药物获得上市批准(其中一款已于2017年退市),而康方生物的PD-1/CTLA-4双抗卡度尼利单抗独占鳌头,成为唯一一款国产双抗药物。国外企业凭借早期起步的优势,双抗研发管线相对丰富,其中Roche领跑,Amgen和强生紧随其后。在国内,康宁杰瑞、康方生物、信达生物和友芝友等企业则在双抗药物领域积极布局,展现出强大的研发实力。
目前,全球范围内还有约17款双抗药物(不包括双抗ADC)已进入III期临床阶段或提交上市申请,其中国内自主研发的佼佼者包括:石药集团的CD3/EpCAM双抗M701、康宁杰瑞的CTLA4/PDL1双抗erfonrilimab,以及百利天恒的HER3/EGFR双抗izalontamab,这些产品的进展彰显了我国在双抗药物研发领域的蓬勃活力。
参考来源:康宁杰瑞官网/公告
<END>
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论