
近日,据中国国家药监局药品审评中心(CDE)官网公示,康宁杰瑞重组人源化PD-L1/CTLA-4双特异性单域抗体Fc融合蛋白注射液(KN046)获批临床,拟联合MAX-40279-01治疗晚期/转移性实体瘤。其中,MAX-40279-01为再极医药自研的1类新药。
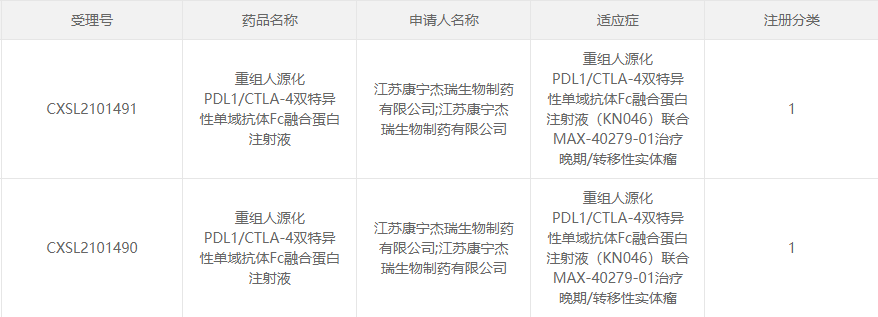 截图来源:CDE官网
截图来源:CDE官网
KN046
KN046是康宁杰瑞自主研发的PD-L1/CTLA-4双特异性抗体,其创新设计包括:采用机制不同的CTLA-4与PD-L1单域抗体融合组成,可靶向富集于PD-L1高表达的肿瘤微环境及清除抑制肿瘤免疫的Treg。
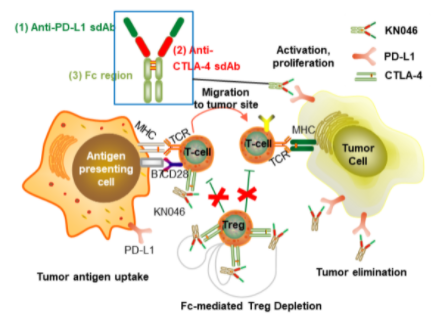
截图来源:康宁杰瑞企业官网
据康宁杰瑞官方消息,KN046在澳大利亚和中国已开展覆盖非小细胞肺癌、胸腺癌、胰腺癌、肝癌、食管鳞癌、三阴乳腺癌等10余种肿瘤的近20项不同阶段临床试验,试验结果显示出良好的安全性和有效性。美国FDA基于在澳大利亚和中国取得的临床试验结果,批准KN046在美国直接进入Ⅱ期临床试验。目前KN046的四项注册临床试验正在进行中。
据康宁杰瑞2月9日公告,KN046的III期临床试验(KN046-303)已成功完成首例患者给药。该试验是一项多中心、随即、双盲、安慰剂对照的临床试验,旨在对未接受系统性治疗的不可切除局部晚期或转移性PDAC(胰腺导管腺癌)患者进行试验,用以评估KN046联合白蛋白紫杉醇及吉西他滨对比安慰剂联合白蛋白紫杉醇及吉西他滨的疗效及安全性。
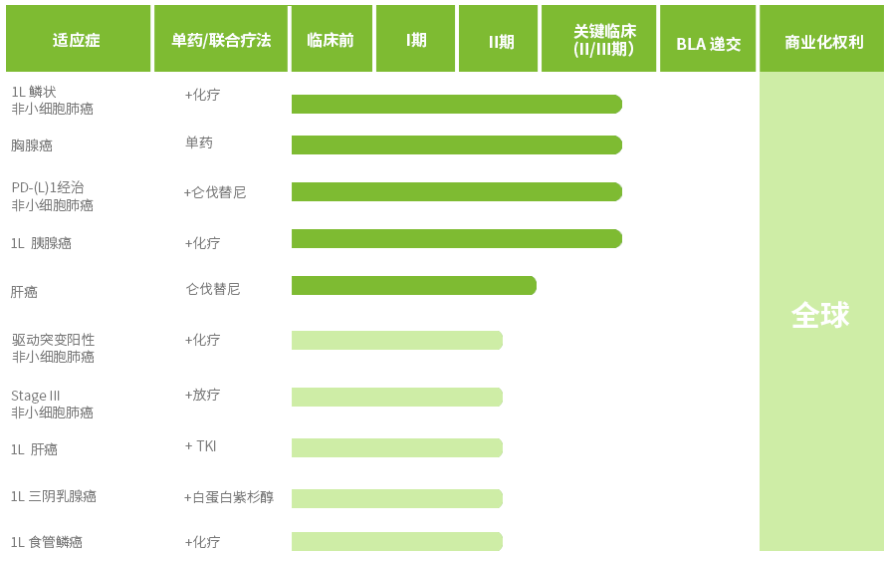
截图来源:康宁杰瑞企业官网
MAX-40279-01
MAX-40279-01(MAX-40279、MAX-4)为再极医药1类新药,该产品在2018年获得了美国FDA孤儿药的资质。MAX-40279通过对FLT3和FGFR的双重强烈抑制和较高的骨髓血药浓度,有效克服当前临床应用药物的骨髓FGF通路激活的耐药性,是国际领先临床试验产品。在实体瘤上MAX-40279还有多重抑瘤机制:临床前研究显示MAX-40279对多种酪氨酸激酶有抑制作用;此外,MAX-40279能够抑制造血祖细胞激酶1(Hematopoietic progenitor kinase 1, 简称HPK1), 解除HPK1对T细胞受体(TCR)通路的负向调节作用。

2021年12月底,再极医药与和康宁杰瑞就MAX-40279(小分子酪氨酸激酶抑制剂)与KN046 (PD-L1/CTLA-4双特异性抗体)的联合治疗达成临床合作协议。双方同意,在互利共赢的前提下,以联合或序贯用药的合作方式共同进行MAX-40279与KN046组合疗法在胃癌(GC)及双方共同决定的其他适应症上的临床合作。同期,再极医药还与君实生物签订协议,将在中国及澳大利亚开展MAX-40279与特瑞普利单抗组合疗法在实体瘤上的I期研究。
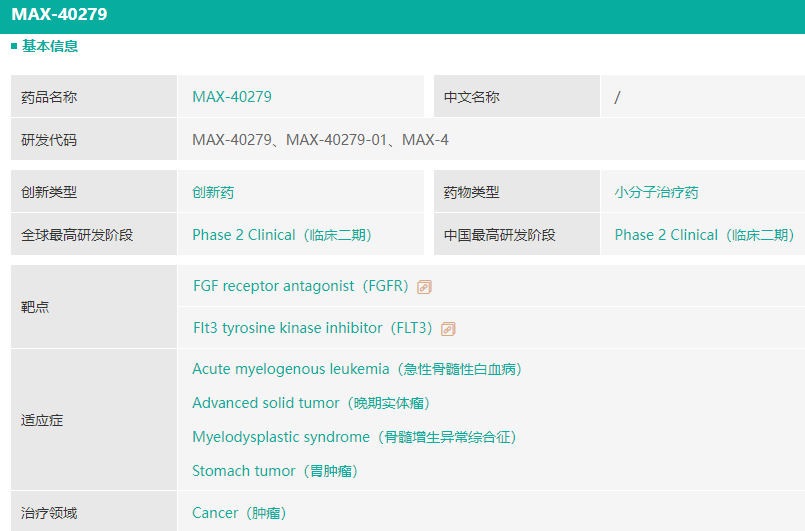
截图来源:药融云全球药物研发数据库
经药融云查询,MAX-40279在国内最高研发进度为临床二期阶段。2022年2月16日,再极医药公示了该药治疗胃癌或胃食管交界处癌的两项临床二期临床试验,该试验主要研究目的为评价MAX-40279治疗二线及以上的晚期胃癌或胃食管交界处腺癌的有效性;次要研究目的为评价MAX-40279治疗二线及以上的晚期胃癌或胃食管交界处腺癌的安全性;评价MAX-40279的药代动力学特性;探索FGFR1OP2相关蛋白的表达水平及突变与疾病预后之间的关系。
除此之外,MAX-40279还开展了针对“晚期结直肠癌”、“成人骨髓增生异常综合征、复发或难治性急性髓系白血病”、“晚期实体瘤”等疾病的临床试验。
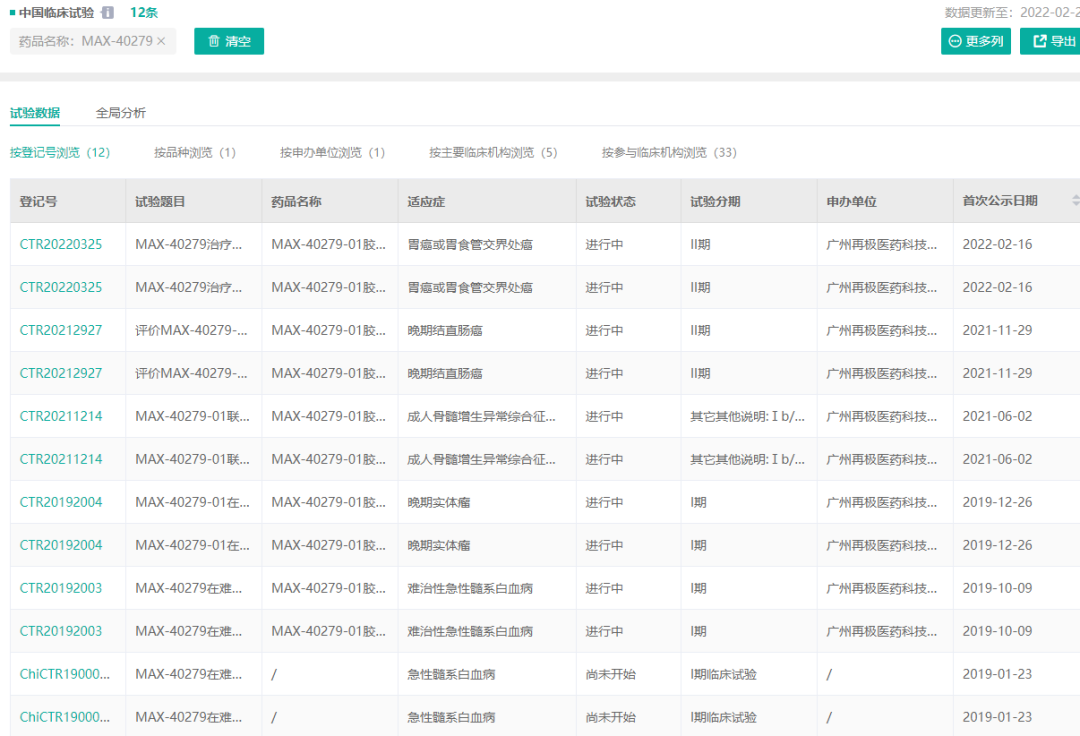
截图来源:药融云中国临床试验数据库
想要解锁更多药物最新进展信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药物竞争格局、最新动态、销售情况、市场规模与前景,可否投入仿制与研发!注册立享15天免费试用和虎年首份医药数据大礼包!

—END—






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论