
2023年11月7日,康方生物(9926.HK)宣布,公司独立自主研发的PD-1/CTLA-4双特异性抗体卡度尼利(开坦尼®)联合奥沙利铂和卡培他滨 (XELOX) 对比安慰剂联合 XELOX 作为一线治疗不可手术切除的局部晚期或转移性胃腺癌或胃食管结合部腺癌(GC/GEJC)的有效性与安全性的随机、双盲、多中心、III期临床研究(AK104-302)在期中分析中达到主要研究终点。
独立数据监察委员会(IDMC)建议基于期中分析结果提前提交卡度尼利该适应症的新药上市申请。
独立数据监察委员会(IDMC)进行的期中分析显示:卡度尼利联合化疗对比安慰剂联合化疗显著延长了全人群(无论PD-L1表达)患者的总生存期(OS),达到预设的优效性标准,安全性特征与既往报道的卡度尼利相关临床研究结果一致,无新的安全性信号。
卡度尼利联合化疗显著降低全人群的死亡风险,包括PD-L1 CPS≥5人群和PD-L1 CPS<5人群,且各人群试验组和对照组间风险比(Hazard Ratio,HR)优于相关PD-1联合化疗联合疗法的已披露数据。
卡度尼利联合化疗在PD-L1 CPS<5人群中同样取得了优异的OS数据,显示卡度尼利联合化疗对于PD-1单抗联合化疗响应不佳的PD-L1低表达及阴性人群的治疗同样高效,很好地延续了此前II期研究的优异表现。
AK104-302研究是全球首个PD-1/CTLA-4双特异性抗体联合化疗一线治疗胃癌的III期临床研究,主要研究终点为比较卡度尼利联合XELOX方案与安慰剂联合XELOX方案在意向治疗(ITT)人群的总生存期(OS)。ITT人群中,PD-L1 CPS<5的患者占比约60%,与真实世界中比例相当。本研究结果将在未来的国际学术会议/学术期刊上予以发表。
AK104-302药物基本信息
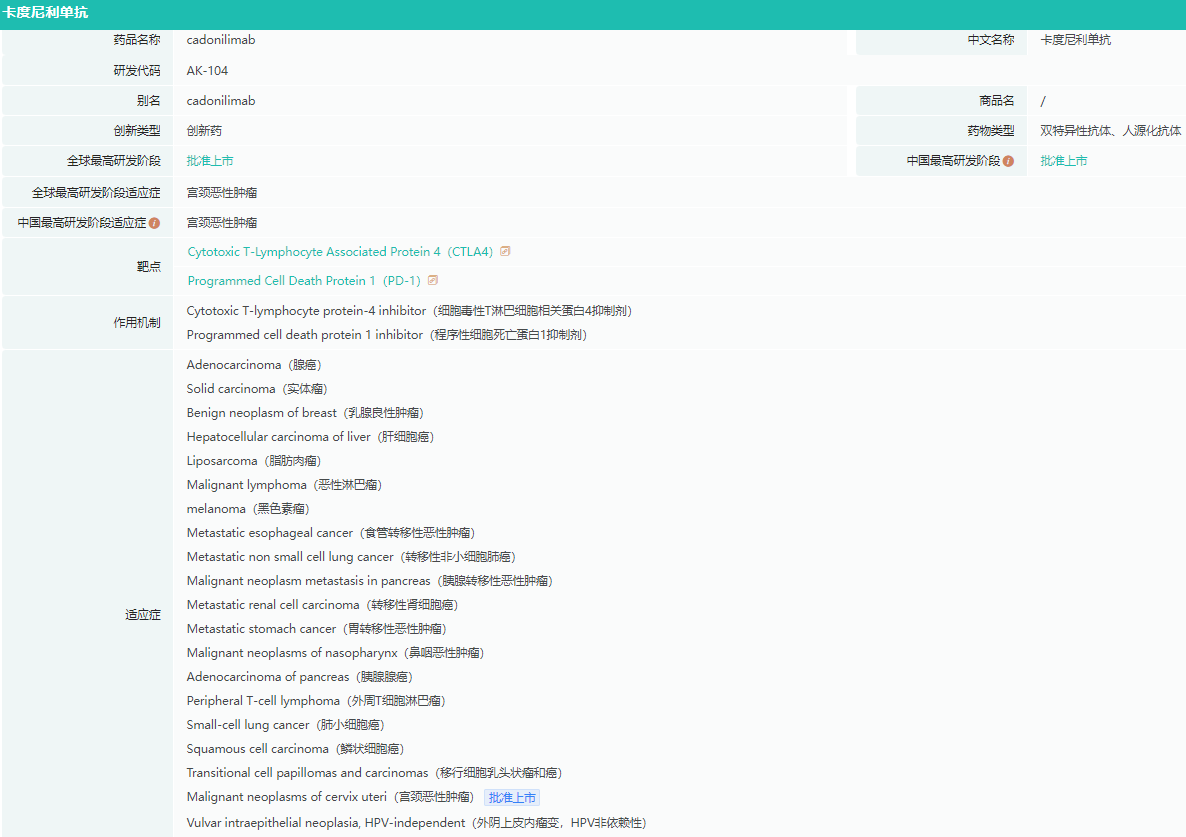
截图来源:药融云全球药物研发数据库
康方生物创始人、董事长、总裁兼首席执行官夏瑜博士表示:“非常欣喜地看到卡度尼利联合化疗一线治疗胃癌取得如此振奋人心的结果,感谢所有推动该临床研究的研究者、参与者和积极参与临床试验的患者,因为你们的努力和付出,中国约50万胃癌患者有望迎来全新机制的双靶点肿瘤免疫双抗联合化疗治疗方案,进一步提升疾病治疗的有效率和生存期。我们将按照IDMC建议,继续高效推进该研究的进行,并就卡度尼利该新适应症的上市申请与国家药品监督管理局(NMPA)积极进行沟通。期待卡度尼利联合化疗一线治疗胃癌适应症早日获批上市,为广大胃癌患者带来全新升级的免疫治疗方案。”
卡度尼利于2022年6月获得NMPA批准,用于治疗二/三线晚期宫颈癌。目前,卡度尼利一线治疗晚期宫颈癌的注册性III期临床已经入组完成,卡度尼利用于高复发风险肝细胞癌根治术后辅助治疗的注册性III期临床研究以及卡度尼利联合化疗对比替雷利珠单抗联合化疗一线治疗PD-L1表达阴性非小细胞肺癌的注册性III期研究正在高效开展中。同时,卡度尼利针对超过20项适应症已启动/开展超过60项(含研究者发起的研究)临床研究。
参考资料:
1.康方生物Akeso
2.药融云数据库
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论