
10月10日,Akero Therapeutics报告了为期96周2b期SYMMETRY研究的36周分析结果,该研究评估了其主要候选产品Efruxifermin(EFX)在非酒精性脂肪性肝炎(NASH)引起的代偿性肝硬化(F4)患者中的疗效和安全性,结果显示对于主要终点纤维化改善,EFX治疗表现出改善趋势,但不具有统计学意义,不及预期。

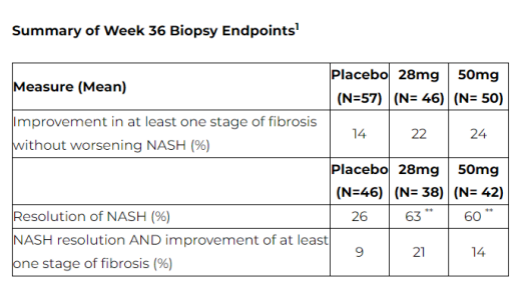
结果显示,22 % ( 28mg EFX )和24 % ( 50mg EFX )的患者在36周时肝纤维化至少有一个阶段的改善,而NASH没有恶化,而安慰剂组为14 %,不具有统计学意义 。
与安慰剂组的0 %相比,EFX各剂量组中4 %的患者经历了3期或2期的纤维化逆转,但没有NASH的恶化。
在第36周时,28毫克和50毫克EFX治疗组分别有63%和60%的患者NASH得到明显改善,而安慰剂治疗组仅有26%的患者NASH得到明显改善,因此两个剂量都达到统计学显著改善。这是迄今为止在该患者群体中NASH改善的最高反应率。在肝损伤和肝纤维化的非侵入性指标、胰岛素敏感性和脂蛋白方面,EFX 两组也都观察到了统计学意义上的明显改善。
安全性方面,总体耐受性良好,仅安慰剂组有一例患者死亡。研究中共报告了21例严重不良事件,各剂量组之间基本平衡;共有12名患者因研究者确定为药物相关的不良事件而停药,安慰剂组1名,28mgEFX组3名,50mgEFX组8名,多为1-2级腹泻。
Efruxifermin药物基本信息

截图来源:药融云全球药物研发数据库
受此消息影响,Akero股价大跌63%,目前市值为10亿美元。
去年9月,Akero Therapeutics宣布Efruxifermin在IIb期HARMONY研究中获得了积极数据,Efruxifermin 28和50mg剂量组均达到了改善肝脏纤维化的主要终点以及多个次要终点。受此消息影响,当天该公司股价大涨135%。

Akero的SYMMETRY研究首席研究员Stephen Harrison医学博士说:"虽然没有进行头对头的比较研究,尽管EFX治疗时间很短,但第36周的SYMMETRY结果是迄今为止在NASH肝硬化患者的安慰剂对照试验中报告的最强的数据集。肝硬化患者具有高水平的肝胶原蛋白,尽管EFX能迅速而大幅度地减少胶原蛋白的合成,但这需要时间来吸收。令人鼓舞的是,在接受EFX治疗的患者中,观察到NASH发病机制的多项指标在统计学上有显著改善。EFX显示出稳定和改善肝脏健康的前景。”
参考资料:
1.https://ir.akerotx.com/news-releases/news-release-details/Akero-therapeutics-reports-encouraging-36-week-analysis-96-week
2.药融云数据库
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论