
2023年8月1日,精准医疗领军企业索元生物宣布,美国食品药品监督管理局(FDA)批准关于索元生物基因疗法DB107的临床 II 期试验。

该临床试验由全球脑瘤领域知名研究机构:加州大学旧金山分校(UCSF),加州大学圣迭戈分校(UCSD)、以及南加州大学(USC)的研究者共同发起,将验证全新生物标志物DGM7作为预测性生物标志物指导下,DB107治疗高级别神经胶质瘤(HGG)的有效性。
本次试验是一项多中心开放性临床研究,预计将招募约 70 名新诊断的高级别神经胶质瘤的成年患者,试验的主要终点为无进展生存期(PFS)。
公司研发管线
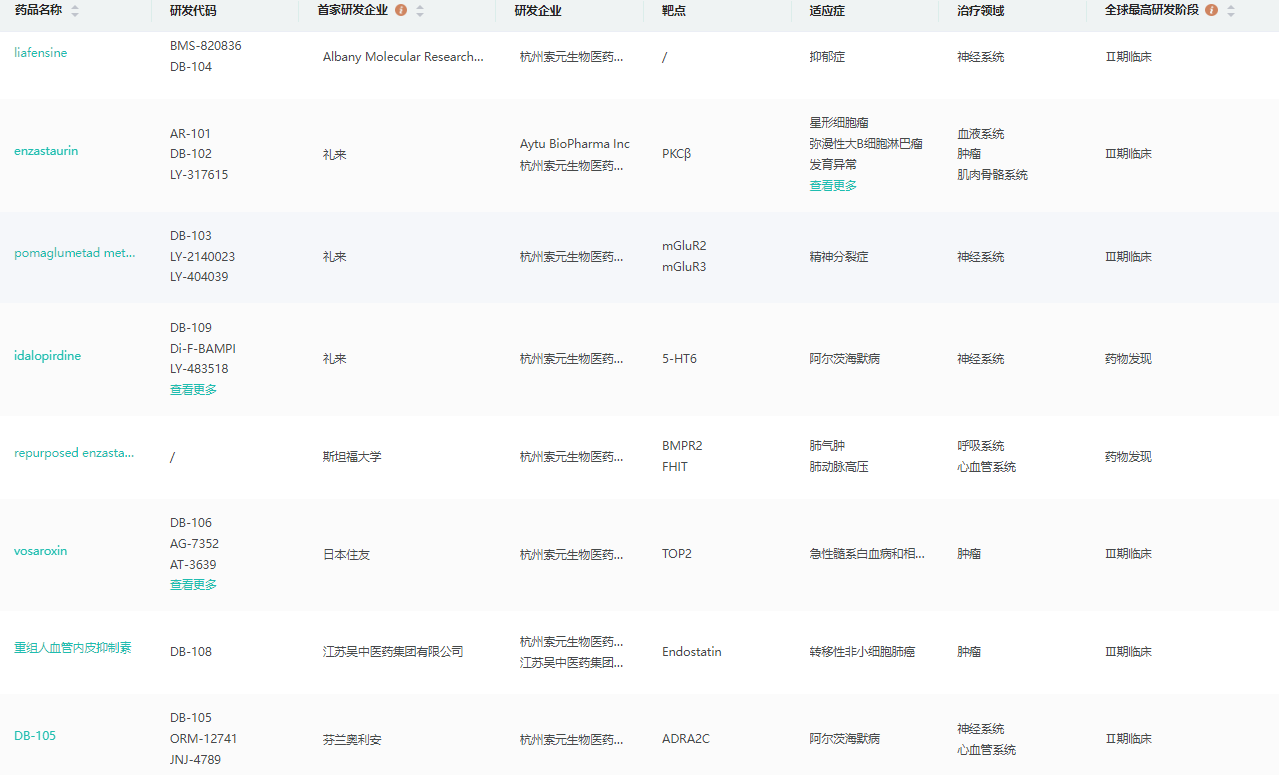
截图来源:药融云全球药物研发数据库
索元生物于2020年从Tocagen收购了Toca 511/FC组合疗法(现称“DB107”)及其独特的重组逆转录病毒载体(RRV)基因治疗平台,Toca 511/FC组合疗法在Tocagen开展的一项国际Ⅲ期临床试验中展现出良好的安全性及耐受性,但在整体人群中没有显现出优于标准疗法的药效而未获成功。索元生物收购DB107后,经过一年多的探索,利用其独特的生物标志物平台发现了一个全新的生物标志物DGM7(Denovo Genomic Marker 7)可预测DB107的疗效。
作为针对严重未满足临床需求的全球首创基因疗法,DB107一直受到各界的关注。DB107获得了美国FDA及欧洲药监局(EMA)的孤儿药认证、还曾获得美国FDA授予的突破性疗法认证(Breakthrough Therapy Designation)。由于本实验的独创性,来自加州大学圣迭戈分校(UCSD)、加州大学旧金山分校(UCSF)以及南加州大学(USC)的脑瘤领域知名学者,共同发起本次临床试验,借助DGM7的预测性使DB107“起死回生”,帮助亟需有效疗法的高级别神经胶质瘤患者。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论