5月14日,美国生物制药公司Athenex宣布,经过持续的战略审查,公司已与贷款机构达成协议,以加快其主要资产的销售,之后将退出市场,并偿还贷款。公司预计在7月1日前完成资产出售。
出售资产包括Athenex Pharmaceutical Division(APD)、Orascovery和细胞疗法。公司破产的原因是主要研发项目重大挫折接连不断。
受此消息影响,5月15日收盘,Athenex(ATNX)收盘暴跌超60%,总市值仅有387.68万美元。

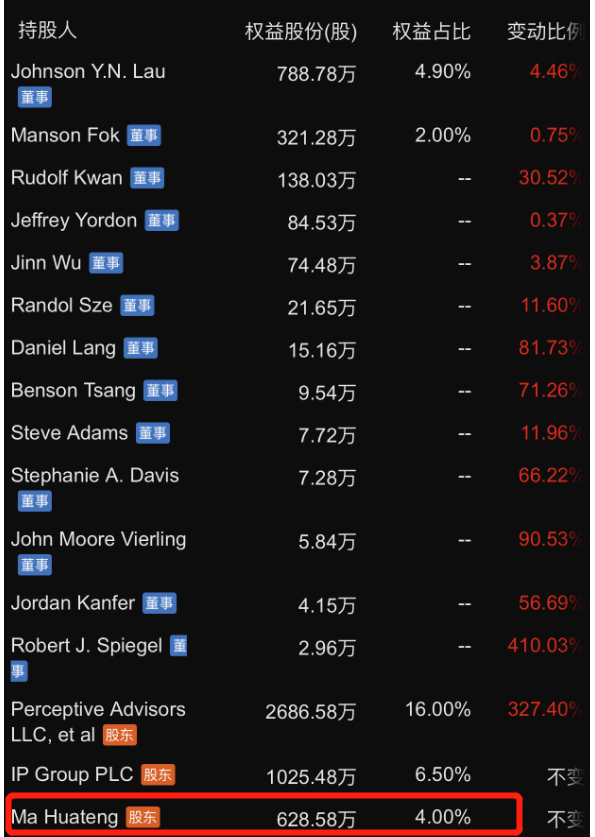
其实,Athenex也受到马化腾的支持,他曾以10.3%的持股排在重要投资者的第二位。截止2022年9月,马化腾持有公司628万股,占比4%。
Athenex以开发口服紫杉醇闻名,但道路曲折坎坷。2020年9月,口服紫杉醇获FDA优先审评,2021年3月FDA发出完整回复函(CRL),表明该药物不具备上市条件。同年10月,公司停止在美国寻求批准。

Johnson Lau
联合创始人兼首席执行官Johnson Lau表示,口服紫杉醇候选产品上市申请遭到FDA拒绝。这一重大挫折,给我们的资金带来了巨大的压力。
在遭到拒绝后,Athenex调整了研发战略,进行了裁员,2022年7月,公司以1.24亿元的价格将位于中国的API原料药工厂出售给泰和中投投资基金管理(北京)有限公司。
除此之外,Athenex还在2021年以7000万美元的价格收购了Kuur Therapeutics公司,获得该公司旗下一系列细胞疗法在研项目,重组了其整体战略并缩减了规模,自此将重心转向细胞疗法。

但在今年3月,Athenex在公布全年财报时披露,因出现患者死亡,其自主研发的自体细胞疗法KUR-501又遭到FDA临床暂停。
Athenex于2003年成立于纽约州布法罗市,是一家同时在美国、中国和英国拥有业务的跨国生物制药公司。根据最新财报显示,Athenex2022全年营收为1.028亿美元。截至2022年12月31日,公司拥有现金、现金等价物、限制性现金和短期投资3670万美元。
在研管线

参考资料:
www.endpts.com
www.athenex.com
<END>





























![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://yaorongyun-public.oss-cn-shanghai.aliyuncs.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)










 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论