
3月13日,GenSight Biologics公布其眼科AAV基因疗法Lumevoq的3期临床试验积极结果。结果显示,遗传性视神经病变(LHON)患者在接受Lumevoq双侧玻璃体内注射基因疗法具有持续的有效性和良好的安全性,双眼的视力的改善,与单侧注射相比,双侧注射获得更多的益处。
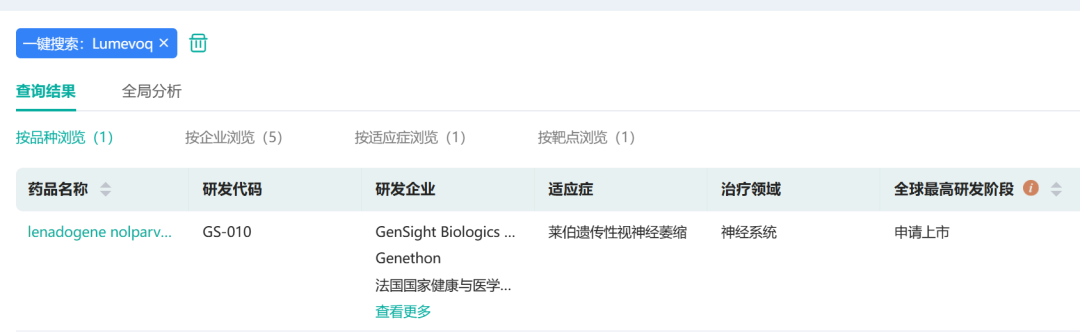
截图来源:药融云全球药物研发数据库
Lumevoq是一种利用腺相关病毒2(AAV2)载体递送正常人类线粒体ND4基因的眼科AAV基因疗法。这次所公布的REFLECT试验是是根据美国FDA的特殊协议评估设计的,是一项随机、双盲、安慰剂对照的 III 期试验,涉及98名因由突变的ND4线粒体基因引起的LHON患者;入组的ND4受试者从发病起有长达一年的视力丧失。
Emory大学医学院眼科学和神经病学教授、REFLECT的国际首席研究员Nancy J Newman医学博士表示,REFLECT试验提供了进一步的结果,证明lenadogene nolparvovec的持续益处,同时再次确认了其安全性。此外,双侧治疗患者的额外益处表明,双眼注射可能是伴有ND4突变的LHON患者的最佳选择。
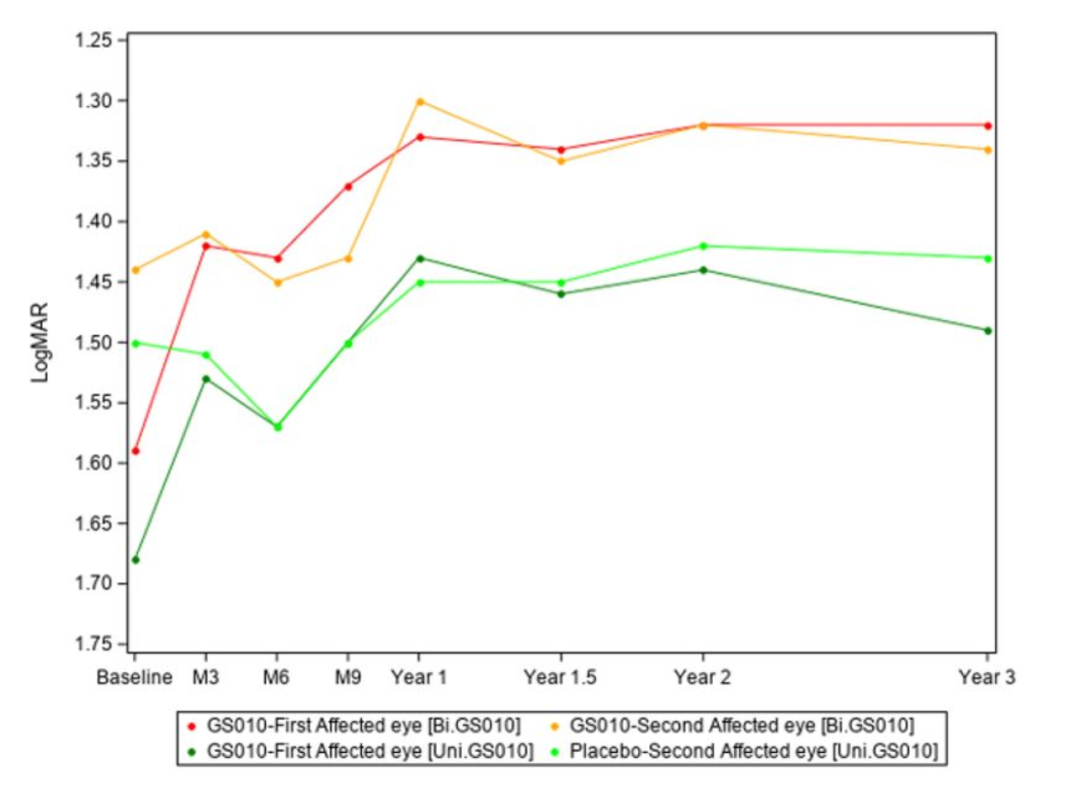
接受Lumevoq治疗患者的三年视力变化图(来源:公司官网)
视力随时间的变化表明,所有接受Lumevoq治疗患者的视力随着时间改善。双眼注射比单眼注射有额外的获益。第3年的分析证实了在第1.5年和第2年观察到剂量效应,并在第3年持续维持,双眼治疗组患者视力显著改善,较单眼治疗组患者共多看到6.5个ETDRS视力表字母,且基线最低点视力相较时,两眼则分别多看见+17至+20个字母。
接受Lumevoq治疗患者三年视力变化数据
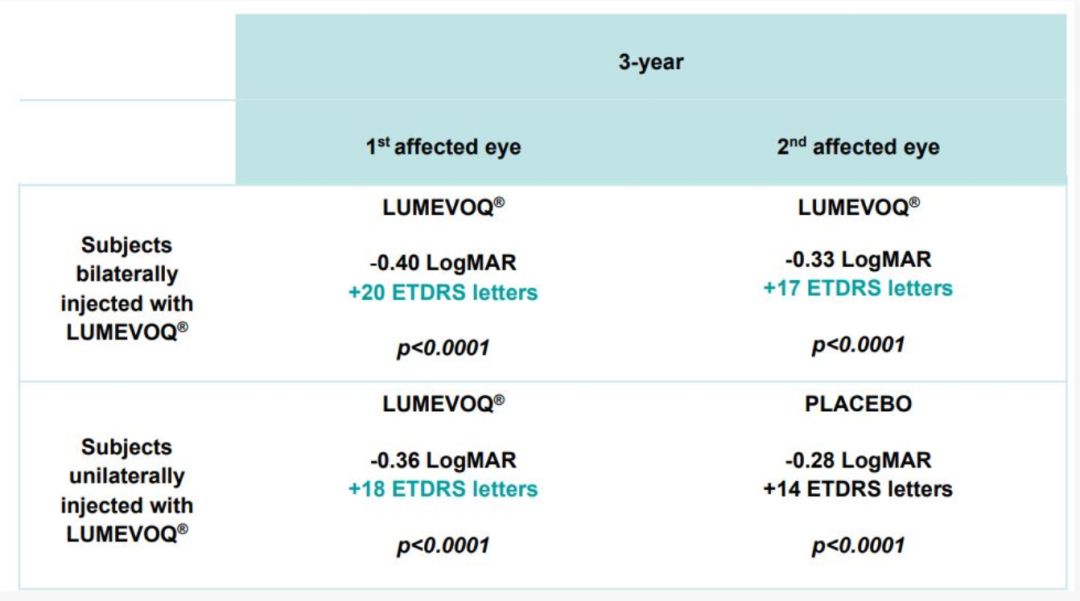
来源:公司官网
据药融云数据库显示,Lumevoq已于2020年9月在欧盟递交了上市申请,并获得了莱伯遗传性视神经萎缩症的孤儿药、儿科用药研究计划特殊审批认证。该眼科AAV基因疗法在美国、英国、欧洲等地的临床试验也推进到了3期阶段。
Lumevoq适应症研发现状
截图来源:药融云全球药物研发数据库
参考资料:
[1] 公司官网
[2] 药融云数据库
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>



































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)



















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论