
-在67名既往未经ROS1酪氨酸激酶抑制剂(TKI)治疗的受试者中,确认的客观缓解率(cORR)和疾病控制率(DCR)分别为92.5%和95.5%。
-在 38 名既往接受克唑替尼(crizotinib)治疗失败的受试者中,确认的客观缓解率(cORR)和疾病控制率(DCR)分别为50%和78.9%。
-在基线存在可测量脑转移病灶(基于RANO-BM标准)的 12 名受试者中,颅内确认的客观缓解率(IC-ORR)和颅内疾病控制率(IC-DCR) 分别为 91.7% 和 100%
-在 5 名 存在ROS1 G2032R 突变的受试者中,有4名达到确认的部分缓解(cPR),1名达到疾病稳定(SD)。
-他雷替尼耐受性良好,观察到的神经系统不良事件的发生率较低,这可能得益于他雷替尼对 ROS1 的选择性抑制超过 TRKB。
美国纽约,2022年6月6日——葆元医药(“葆元”),一家专注于开发新型精准肿瘤疗法的临床阶段全球性生物制药公司,与信达生物制药集团(“信达生物”,港交所代码:01801),一家致力于研发、生产和销售肿瘤、自身免疫、代谢、眼科等重大疾病领域创新药物的生物制药公司,今日共同宣布在2022年美国临床肿瘤学会年会(ASCO)上展示他雷替尼(Taletrectinib,ROS1酪氨酸激酶抑制剂)临床二期试验在ROS1阳性非小细胞肺癌患者中的更新的有效性和安全性数据。
他雷替尼(Taletrectinib)临床二期试验在既往未经ROS1-TKI治疗或既往接受克唑替尼治疗失败的ROS1阳性非小细胞肺癌患者中的有效性和安全性数据
海报展示,摘要#:8572
本项TRUST(Taletrectinib ROS1 LUng STudy)研究是一项多中心、开放标签、单臂的临床二期研究,用于评估他雷替尼(Taletrectinib)在治疗中国的既往未经ROS1-TKI治疗或既往接受克唑替尼治疗失败的ROS1 融合阳性非小细胞肺癌患者的有效性和安全性,试验注册编号:NCT04395677。
截至2022年2月23日,TRUST二期试验招募了67名既往未经ROS1-TKI治疗和42名既往接受克唑替尼治疗失败的患者。患者每日接受他雷替尼给药 600 mg ,并由独立审查委员会(IRC)评估关键疗效终点,包括客观缓解率(ORR)、缓解持续时间(DOR)、疾病控制率(DCR)、颅内客观缓解率( IC-ORR)、颅内疾病控制率 (IC-DCR)、无进展生存期 (PFS)、总生存期 (OS) 和安全性。
在未经ROS1-TKI治疗受试者中,确认的客观缓解率 (cORR) 为 92.5% (62/67),包括 2 例确认的完全缓解 (cCR);确认的疾病控制率(DCR)为 95.5% (64/67)。
在既往接受克唑替尼治疗失败的受试者中,确认的客观缓解率为50%(19/38),确认疾病控制率为78.9% (30/38)。
在 5 名既往接受克唑替尼治疗失败且存在ROS1 G2032R 突变的受试者中,有4名达到确认的部分缓解(cPR),1名达到疾病稳定(SD)。
在基线存在可测量脑转移病灶(基于RANO-BM标准)的12 名受试者中,颅内客观缓解率和颅内疾病控制率分别为91.7% 和100%。有1名基线存在不可测量脑转移病灶的受试者经治疗后脑转移灶完全消失。
他雷替尼耐受性良好。大多数治疗期间出现的不良事件 (TEAE) 为 1 级或 2 级。最常报告的治疗相关不良事件 (TRAE) 是轻度腹泻和短暂的 AST/ALT 升高不伴胆红素升高。神经系统不良事件的发生率较低,可能在于他雷替尼对ROS1 而非TRKB 的选择性抑制有助于减少与 TRKB 相关的中枢神经系统不良事件。在其他 ROS-TKI中经常报告的一些常见不良事件,如视力障碍、水肿、头痛、头晕和肌肉骨骼疾病,在他雷替尼中观察到的频率较低。
“他雷替尼是一种新一代的、潜在最优的ROS1抑制剂,在未经ROS1-TKI治疗和既往经克唑替尼治疗失败的非小细胞肺癌患者中有潜在的巨大需求。”上海市肺科医院肿瘤科主任周彩存教授表示,“TRUST临床试验显示,他雷替尼在 ROS1 阳性非小细胞肺癌的一线和二线治疗中,客观缓解率很高,对克唑替尼耐药突变(包括 G2032R 溶剂前沿突变)也具有出色的效力。我们还高兴地看到他雷替尼在脑转移患者中也显示出颅内抗肿瘤活性。”
“与其他 ROS1 抑制剂相比,他雷替尼显示出更好的脑渗透和颅内活性以及良好的安全性,”葆元医药首席医疗官和联合创始人颜冰博士表示,“我们非常期待推进他雷替尼的研究,因为我们相信它是潜在的同类最佳的新一代 ROS1 抑制剂,适用于既往未经ROS1-TKI治疗和既往接受ROS1-TKI治疗失败的非小细胞肺癌患者,临床急需对抗耐药突变和脑转移的抗肿瘤新疗法。
“他雷替尼客观缓解率和疾病控制率的更新数据证明了其对中国 ROS1 阳性非小细胞肺癌患者具有疗效和安全方面的潜在优势。”信达生物高级副总裁周辉博士表示,“我们对结果感到鼓舞,并将继续推进他雷替尼的临床开发,以探索下一代 ROS1抑制剂的潜力,并在未来造福更多的非小细胞肺癌患者。”

患者案例:图示为一位既往未经ROS1-TKI治疗患者的影像图。经过他雷替尼(600mg QD)的12周治疗后,脑部病灶(上图)及肺部病灶(下图)几乎完全消失。
ROS1 致癌融合基因在非小细胞肺癌患者中发生频率为1-2%. 也在胆管癌、胶质母细胞瘤、卵巢癌、胃癌和结直肠癌当中能观察到。中枢神经系统转移在既往未经ROS1-TKI治疗的ROS1 阳性非小细胞肺癌患者中发生率为20-30%,在既往接受克唑替尼治疗失败的ROS1 阳性非小细胞肺癌患者中发生率高达50%。对第一代 ROS1-TKI的耐药通常是由于继发性突变的产生,例如 ROS1 G2032R 耐药突变,对此尚未有 FDA 批准的治疗方法。
他雷替尼(Taletrectinib)是一种新一代的具有血脑屏障穿透性、高选择性 的ROS1 抑制剂。2022年3月,中国国家药品监督管理局将他雷替尼纳入突破性治疗药物品种(BTD),用于一线既往未经ROS1-TKI治疗和二线既往接受ROS1-TKI治疗的ROS1 阳性非小细胞肺癌患者。
此外,他雷替尼的一项全球二期TRUST-II试验 (NCT04919811) 正在北美、欧洲和亚洲的临床中心积极招募患者。TRUST-II 研究的设计在 2022年美国临床肿瘤学会的海报 (#TPS8601) 中进行了介绍。
关于他雷替尼
他雷替尼是一种新型的、潜在最优的新一代 ROS1 抑制剂,旨在有效靶向治疗ROS1 融合突变,具有治疗既往未经ROS1 TKI治疗患者和既往接受ROS1 TKI治疗患者的潜力。据估计,ROS1 基因融合突变是约1%至2%的非小细胞肺癌患者的致癌驱动因素。也在胆管癌、胶质母细胞瘤、卵巢癌、胃癌和结直肠癌当中能观察到. 他雷替尼在ROS1 融合阳性非小细胞肺癌患者中表现出优异的抗克唑替尼耐药性、良好的脑渗透和颅内抗肿瘤活性以及良好的安全性。在这些患者中只观察到少量神经系统不良反应,这可能得益于他雷替尼对 ROS1 而非 TRKB 的选择性抑制。如需了解中国 TRUST(Taletrectinib ROS1 LUng STudy)2期试验及全球 TRUST-II 2期试验的更多信息,请访问药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)或 www.clinicaltrials.gov并输入临床试验编号 NCT04395677和NCT04919811进行查询。
他雷替尼临床试验信息
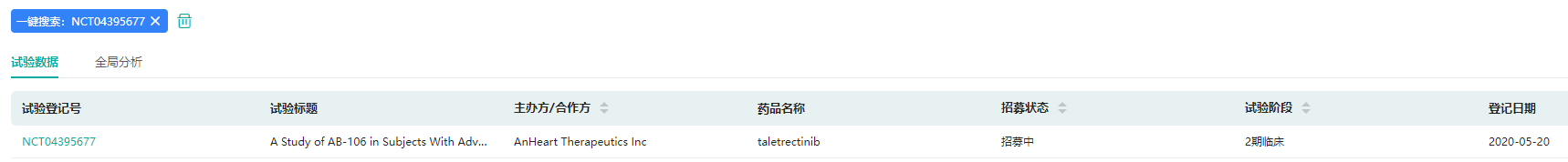
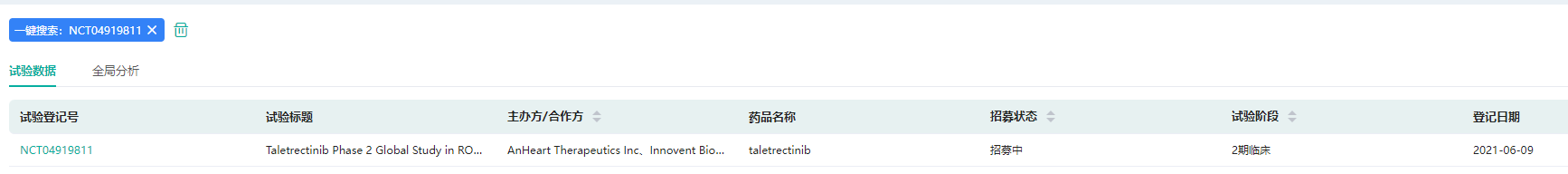
截图来源:药融云临床试验数据库
2021年6月,葆元和信达生物签署了在大中华地区联合开发和商业化他雷替尼的独家许可协议,包括中国大陆、香港、澳门和台湾地区。
经药融云数据库查询,目前他雷替尼针对转移性非小细胞肺癌、实体瘤的适应症在中国的临床试验最高已经开展到二期临床,且还在持续推进中。
他雷替尼基本信息


截图来源:药融云全球药物研发数据库
如对试验有任何问题,请联系trials@anhearttherapeutics.com。
关于葆元医药
葆元医药(“葆元”)是注册于开曼群岛(注册名AnBio Therapeutics Ltd.)的一家临床阶段的全球性生物制药集团公司,致力于开发广泛的创新性新一代精准肿瘤治疗药物管线,用于医疗需求满足程度较低的领域。其主要研发药物他雷替尼是新一代同类中潜在最优的 ROS1 抑制剂,目前正处于 2 期试验,用于治疗 ROS1 融合阳性非小细胞肺癌的既往未经ROS1-TKI治疗和既往接受 ROS1-TKI 治疗的患者。公司的产品管线还包括:AB-218,一种处于2期试验的 mIDH1抑制剂,具有良好的脑渗透性,可用于治疗具有 mIDH1突变的多种实体瘤;AB-329,一种处于1期研究的 AXL 抑制剂,可用于与检查点抑制剂或化疗联合使用治疗非小细胞肺癌或其他实体肿瘤。葆元在美国和中国设有办公室。如需更多信息,请访问 www.anhearttherapeutics.com。
关于信达生物
“始于信,达于行”,开发出老百姓用得起的高质量生物药,是信达生物的理想和目标。信达生物成立于2011年,致力于开发、生产和销售肿瘤、自身免疫、代谢、眼科等重大疾病领域的创新药物。2018年10月31日,信达生物制药在香港联合交易所有限公司主板上市,股票代码:01801。
自成立以来,公司凭借创新成果和国际化的运营模式在众多生物制药公司中脱颖而出。建立起了一条包括32个新药品种的产品链,覆盖肿瘤、自身免疫、代谢、眼科等多个疾病领域,其中7个品种入选国家“重大新药创制”专项。公司已有 7个产品(信迪利单抗注射液,商品名:达伯舒®,英文商标:TYVYT®;贝伐珠单抗生物类似药,商品名:达攸同®,英文商标:BYVASDA ®;阿达木单抗生物类似药,商品名:苏立信®,英文商标:SULINNO ®;利妥昔单抗生物类似药,商品名:达伯华®,英文商标:HALPRYZA®; 佩米替尼片,商品名:达伯坦®,英文商标:PEMAZYRE®; 奥雷巴替尼,商品名:耐立克®;商品名:希冉择®,英文商标:CYRAMZA®)获得批准上市, 2个品种在NMPA审评中,4个品种进入III期或关键性临床研究,另外还有19个产品已进入临床研究。
信达生物已组建了一支具有国际先进水平的高端生物药开发、产业化人才团队,包括众多海归专家,并与美国礼来制药、Adimab、Incyte、MD Anderson 癌症中心和韩国Hanmi等国际合作方达成战略合作。信达生物希望和大家一起努力,提高中国生物制药产业的发展水平,以满足百姓用药可及性和人民对生命健康美好愿望的追求。
详情请访问公司网站:www.innoventbio.com或公司领英账号:Innovent Biologics。
信达生物前瞻性陈述
本新闻稿所发布的信息中可能会包含某些前瞻性表述。这些表述本质上具有相当风险和不确定性。在使用“预期”、“相信”、“预测”、“期望”、“打算”及其他类似词语进行表述时,凡与本公司有关的,目的均是要指明其属前瞻性表述。本公司并无义务不断地更新这些预测性陈述。
这些前瞻性表述乃基于本公司管理层在做出表述时对未来事务的现有看法、假设、期望、估计、预测和理解。这些表述并非对未来发展的保证,会受到风险、不确性及其他因素的影响,有些乃超出本公司的控制范围,难以预计。因此,受我们的业务、竞争环境、政治、经济、法律和社会情况的未来变化及发展的影响,实际结果可能会与前瞻性表述所含资料有较大差别。
本公司、本公司董事及雇员代理概不承担 (a) 更正或更新本网站所载前瞻性表述的任何义务;及 (b) 若因任何前瞻性表述不能实现或变成不正确而引致的任何责任。
联系方式
- 葆元医药
投资人联系:
ir@anhearttherapeutics.com
212-466-6378
媒体联系:
Kimberly Ha
KKH Advisors
917-291-5744
kimberly.ha@kkhadvisors.com
- 信达生物
媒体:
pr@innoventbio.com
+86 512-6956 6088
投资者:
ir@innoventbio.com
+86 512-6956 6088
想要解锁更多药企创新药研发信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、研发阶段、最新进展、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论