
引言
2022年3月22日,药审中心官网显示已承办齐鲁制药有限公司3.4类生物制品注射用罗普司亭的上市申请,距唯一进口药品获批上市仅仅两个月。罗普司亭是第二代口服TPO-R激动剂,适用于免疫性血小板减少症。此次是国内首个申报上市的罗普司亭生物类似药。
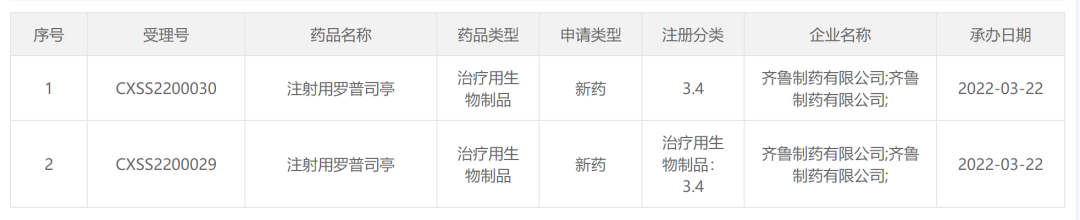
(图源:CDE官网)
超十亿元免疫性血小板减少症药物
免疫性血小板减少症(ITP)是一种罕见的、严重的获得性自身免疫性疾病。其特征是血液中的血小板计数较低,可导致严重的出血事件。患者主要表现为皮肤和黏膜出血,目前尚无根治方法,治疗以对疾病止血治疗为主。免疫性血小板减少症在临床极为常见,成年人的发病率为5~10\10万,60岁以上老人是该病的高发群体。患有慢性ITP的人要面临严重出血事件的风险增加,可能导致严重的并发症甚至死亡。
罗普司亭是安进(Amgen)公司研发的一款血小板生成素(TPO)受体激动剂,通过与TPO受体结合刺激细胞内的转录途径,从而使血小板生成增加,用于治疗免疫性血小板减少症(ITP)。该药最早于2008年在澳大利亚获批,后经FDA批准在美国上市,目前已在全球数十个国家和地区获批上市。据公开资料显示,协和发酵麒麟拥有安进的罗普司亭在大中华区、韩国、新加坡、马来西亚等地区的开发权。
经药融云数据库查询,2022年1月11日,日本协和麒麟(Kyowa Kirin)申报的注射用罗普司亭(曾用名:注射用罗米司亭|商品名:惠尔凝)已获得批准在中国上市,用于治疗原发慢性免疫性血小板减少症。且目前仅此一家拥有中国药品批文,尚无仿制药报产。
注射用罗普司亭药品批文信息

截图来源:药融云中国药品批文数据库
据药融云数据统计,罗普司亭近几年的整体销售额呈持续增长趋势,2020年全球销售额超9亿元,2021年预计可突破10亿大关。销售市场非常可观,潜力巨大。
罗普司亭全球销售额
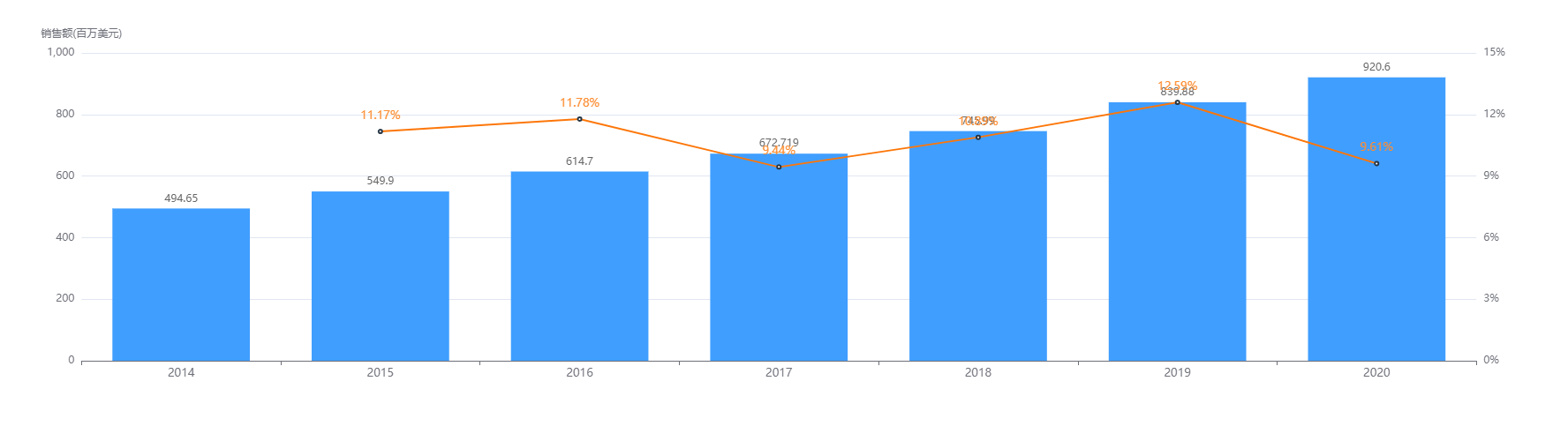
图片来源:药融云全球药物研发数据库
齐鲁制药进展最快
而齐鲁制药开发的罗普司亭生物类似药(研发代码:QL0911 )是是国内首款报上市的罗普司亭生物类似药,也是TPOR靶点国内研发进度最快的产品,其次是三叶草生物制药的SCB-219,三生制药的艾曲泊帕,北京泰德制药的重组人血小板生成素,以及科伦药业的罗普司亭生物类似药。
TPOR靶点产品研发阶段(部分)
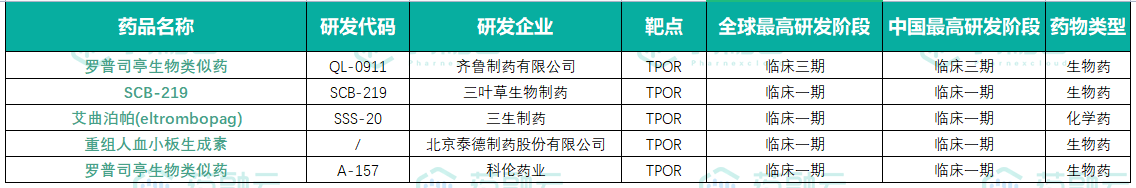
数据来源:药融云全球药物研发数据库
参考来源:
[1] CDE官网
[2] 药融云数据库 https://www.pharnexcloud.com/?zmt-mhwz
想要解锁更多药企创新药申报信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药申报情况、最新进展、研发阶段、临床试验、竞争格局、涉及靶点适应症、销售情况、市场规模与前景,可否投入研发与仿制!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>






































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论