1月5日,NMPA发布一批药品批准证明文件待领取信息,其中,石药集团恩必普药业的3类仿制药唑来膦酸注射液上市申请获NMPA批准。这是石药集团恩必普药业过评的第3款药品。

截图来源:NMPA官网
唑来膦酸注射液是第三代双膦酸盐,与第一、二代相比,具有抗骨吸收作用更强、降低骨相关事件发生率疗效更优的临床优势。其原研来自诺华(Novartis),最早于2001年在欧盟首获批,后相继在美国、日本等批准上市,用于治疗恶性肿瘤引起的高钙血症,以及联合标准抗肿瘤药物用于治疗实体肿瘤骨转移患者和多发性骨髓瘤患者的骨骼损害。
据药融云统计,唑来膦酸院内销售额峰值为15亿元,今年上半年同比增加97%,年总额有望突破20亿元大关。总体来看,原研诺华制药无疑占领市场高地,拥有近半的份额;但近年来,国产仿制药不断发力,2020年正大天晴以40%的市场占比,超越诺华(38%)跃居榜首。其余20%左右的市场份额,则由恒瑞、扬子江、成都天台山、科伦、奥赛康等企业共享。
唑来膦酸相关制剂近年院内销售概况
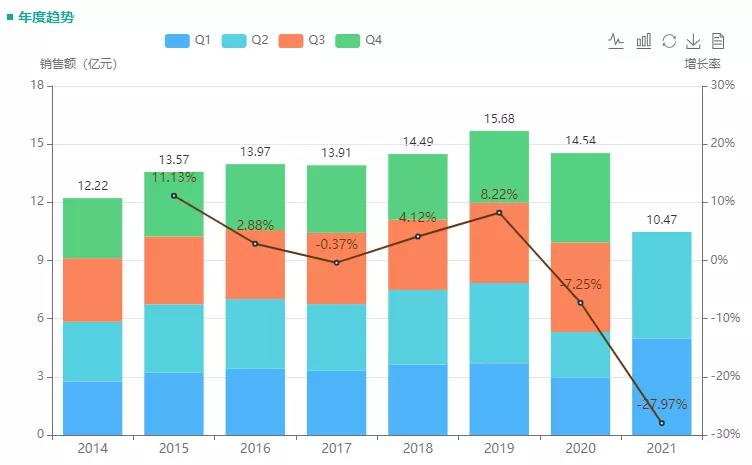
截图来源:药融云全国医院销售数据库
国内获批的唑来膦酸制剂均为注射剂(注射用唑来膦酸、唑来膦酸注射液和注射用唑来膦酸浓溶液)。其中唑来膦酸注射液和注射用唑来膦酸浓溶液已有企业陆续过评,其首家过评分别由科伦药业和正大天晴拿下。
国内唑来膦酸报产/一致性评价情况
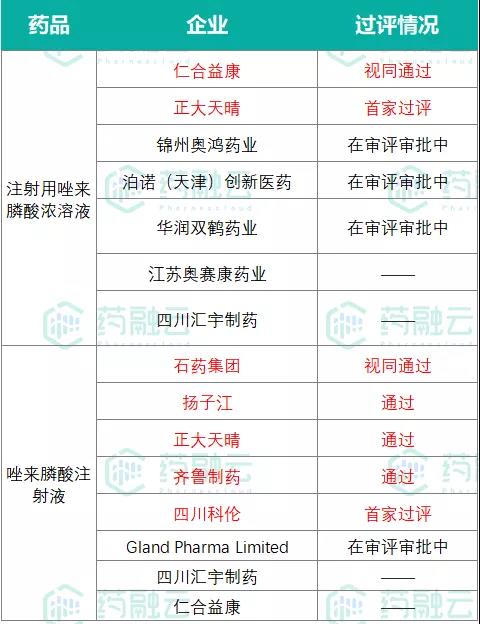
数据来源:药融云一致性评价数据库
—END—







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论