溶瘤病毒(oncolytic virus,OV)是一类天然或经过基因改造的病毒,它通过直接裂解肿瘤细胞或者抗肿瘤免疫反应达到杀伤肿瘤细胞的目的,并且不损伤正常细胞,为广大恶性肿瘤患者带来新的治疗选择。
据药融云数据显示,目前全球共有5款溶瘤病毒产品获批上市,分别是赛百诺的今又生、Latima的Rigvir、三维生物的安科瑞、安进的Imlygic以及第一三共的Delytact。
与其他肿瘤免疫疗法相比,溶瘤病毒作为一种新型肿瘤免疫疗法,不仅杀伤效率高、靶向性好、不良反应小、避免耐药性,而且成本低廉。目前常用的溶瘤病毒主要有腺病毒、疱疹病毒、痘病毒、呼肠孤病毒和科萨基病毒等。
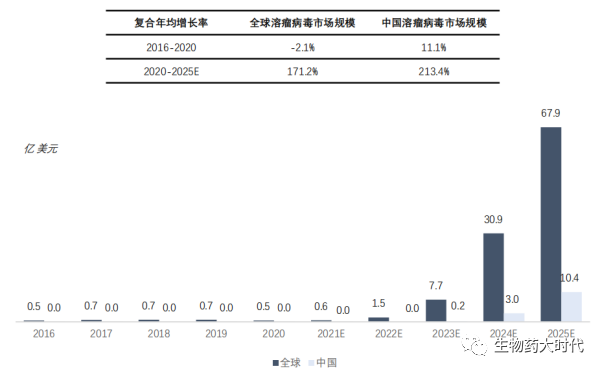
来源:沙利文分析
据沙利文数据显示,预计2025年全球溶瘤病毒市场规模达到67.9亿美元,2020~2025年复合年增长率为171.2%;2025年中国溶瘤病毒市场规模达到10.4亿美元,2020~2025年复合年增长率为213.4%。
由此可见,溶瘤病毒市场需求量持续攀升,规模也随着扩大。据统计,目前国内布局溶瘤病毒的公司已超60家。
国内溶瘤病毒疗法部分公司分部图

来源:生物药大时代整理
由上图可见,国内溶瘤病毒公司主要分部在北上广。其中,乐普生物、阿诺医药、恒翼生物、康弘生物、滨会生物、中生集团、天士力、奥源和力、合生基因、上海医药、亦诺微医药、康万达医药等公司溶瘤病毒产品临床研发阶段处于前列。
乐普生物、恒翼生物、天达康基因、阿诺医药的溶瘤病毒候选产品已进入临床3期试验阶段;而复诺健生物、滨会生物、康弘生物、奥源和力等溶瘤病毒产品已进入2期试验,其它公司多款溶瘤病毒产品进入1期临床试验或获批IND。
一、2023年最新进展
3月29日,亦诺微医药治疗恶性脑胶质瘤溶瘤产品MVR-C5252通过中国国家药品监督管理局审核,获准进入临床阶段。
3月28日,康万达首款溶瘤痘苗病毒产品hV01获批临床,拟用于治疗具有可注射病灶的晚期难治/复发性恶性实体瘤。
3月16日,中生复诺健溶瘤病毒产品“重组人IL12/15-PDL1B单纯疱疹Ⅰ型溶瘤病毒注射液(Vero细胞)”(产品代号:VG161),再获国家药监局临床试验批件,适应症为:VG161联合卡瑞利珠单抗治疗既往至少接受过一线治疗方案治疗的晚期原发性肝细胞癌。
2月25日,滨会生物首款溶瘤病毒候选药物重组人GM-CSF溶瘤II型单纯疱疹病毒(OH2)注射液(Vero细胞)获得国家药品监督管理局药品审评中心(CDE)批准,纳入突破性治疗品种。
2月份,功楚生物研发的“GC001溶瘤痘苗病毒注射液”获得CDE临床默示许可,用于治疗晚期或转移性实体瘤。
二、融资情况

来源:生物药大时代整理
据不完全统计,2021年~2023年6月,国内溶瘤病毒疗法公司总融资超33亿人民币。有7家企业融资过亿,分别是:威溶特医药、滨会生物、复诺健生物、阿诺医药、安龙生物、复诺健生物、恒润达生,其中滨会生物于2021年2月,2022年4月分别融资6亿元、3亿元(《2022年全球溶瘤病毒领域的投融资TOP9!》)。
滨会生物
滨会生物成立于2010年,深耕溶瘤病毒研究领域十余年,已成为肿瘤免疫治疗溶瘤病毒细分领域的领军企业。公司搭建了溶瘤病毒(oHSV2)技术平台,研发的首款产品BS001(OH2)注射液已获得NMPA批准的单药和联合用药3个临床批件,是国内唯一多适应症单药及联合用药均进入临床Ⅱ期且取得积极数据的溶瘤病毒候选产品。2021年8月,BS001(OH2)注射液获得美国FDA许可,在美国开展多种实体瘤的临床试验。
滨会生物研发管线
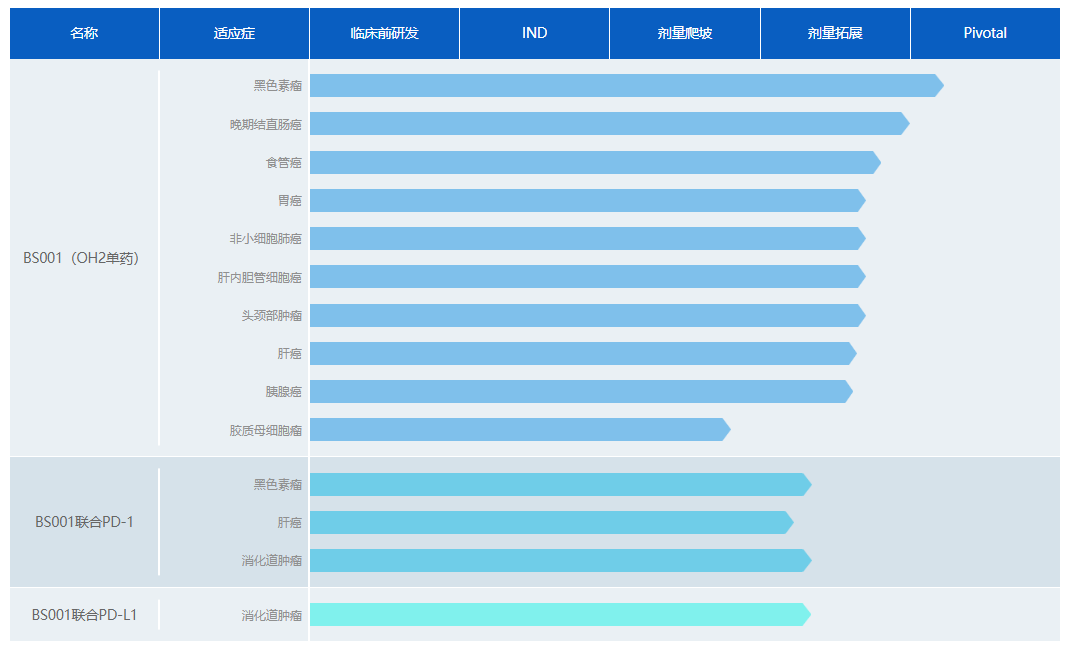
来源:官网
复诺健生物
复诺健生物成立于2015年,2018年在上海南翔精准医学产业园建立临床转化中心,2021年9月完成D2轮融资,融资用于推进现有溶瘤病毒临床项目的研发,mRNA技术平台的建立、上海南翔复诺健全球研发生产中心的建设,以及潜在的战略合作等。作为全球溶瘤病毒研发领域的领跑者,复诺健依托其独创的SynerlyticTM技术平台,通过表达多个协同性免疫调控因子,显著提高病毒溶瘤活性并大幅改善肿瘤微环境,从而有效地激活抗肿瘤免疫。复诺健生物第一个临床产品VG161于2022年进入美国临床II期试验,同年通过CDE批准开展联合临床I/II期试验。2023年2月13日,VG161获批FDA孤儿药用于肝内胆管癌的治疗。
复诺健生物研发管线

来源:官网
华津医药
广州华津医药于2016年成立,重点研究开发一系列利用肿瘤异常代谢的主动靶向肿瘤的溶瘤细菌以及溶瘤病毒药物。公司逐步建立了全球首个快速广谱溶瘤细菌技术平台,并完成了核心产品SGN1(桑美威克®,SalMet-Vec®)的临床前研究、CMC生产工艺开发以及符合GMP标准的规模化生产设施建设。2023年4月21日,SGN1在中国台湾临床试验中心完成首例受试者瘤内给药,该受试者为一线治疗手段失败后复发肺转移的肿瘤患者。目前SGN1瘤内注射治疗晚期实体瘤患者I/IIa期临床试验正在美国和中国台湾地区同步开展。
华津医药研发管线
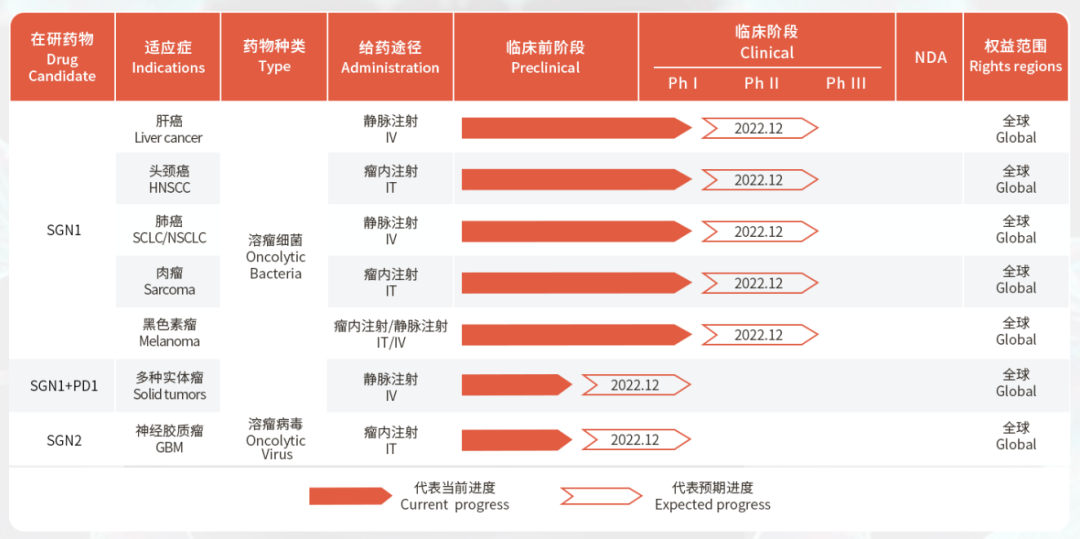
来源:官网
参考资料:
[1] 各公司公告
[2] 药融云数据库
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论