
在过去的2021年里,国产创新药获批数进入爆发期,仿制药获批数也大幅激增,国内药企收获了多款重磅品种。那2022仿制药的情况是怎样的呢?
据药融云中国药品审评数据库显示,截至2022年7月28日,2022年获CDE承办的仿制药数量按受理号计为1241个,按申报产品计为482个,按申报企业计为594家。对比2021年同期数据,承办的仿制药受理号同比增加46.17%,产品数量同比增加31%,申报企业同比增加41.8%。
一、仿制药申报药品TOP10
其中,仿制药申报药品TOP10排名分别为:氧、他达拉非片、利伐沙班片、盐酸达泊西汀片、盐酸莫西沙星滴眼液、哌柏西利胶囊、玻璃酸钠滴眼液、盐酸乌拉地尔注射液、磷酸奥司他韦干混悬剂、阿普米司特片。
2022年仿制药申报药品TOP10(截至2022.7.28)

图片来源:药融云中国药品审评数据库
- 热门仿制药——利伐沙班片
利伐沙班是一种直接Xa因子抑制剂,最早于2009年在国内获批上市,同年进入国家医保目录,2018年进入国家基本药物目录,是目前安全用药经验人群最广的新型口服抗凝药。与其他新型口服抗凝药相比,利伐沙班优势突出:适应症最丰富、医保报销范围最广(限华法林治疗控制不良或出血高危的非瓣膜性房颤、深静脉血栓、肺栓塞患者;下肢关节置换手术患者)。自上市以来,利伐沙班逐渐被房颤卒中预防、VTE治疗、VTE预防等领域的国内外相关权威指南一线推荐,广泛用于心血管内科、血管外科、神经内科、老年医学科、呼吸与危重症医学科、骨科、肿瘤科,以及外科相关科室。
国内首仿是由正大天晴拿下,正大天晴利伐沙班片(安日欣)获批适应症为:用于择期髋关节或膝关节置换手术成年患者,以预防静脉血栓形成(VTE);用于治疗成人深静脉血栓形成(DVT)和肺栓塞(PE),在完成至少6个月初始治疗后DVT和/或PE复发风险持续存在的患者中,用于降低DVT和/或PE复发的风险;用于具有一种或多种危险因素的非瓣膜性房颤成年患者,以降低卒中和体循环栓塞的风险。
- 热门仿制药——盐酸莫西沙星滴眼液
2021年3月9日,国家药品监督管理局签发盐酸莫西沙星滴眼液药品批件,华润紫竹成为该产品国内首仿获批单位。盐酸莫西沙星滴眼液为第四代喹诺酮类广谱抗菌药,在继承了喹诺酮类药物良好的抗革兰氏阴性菌活性的基础上,抗革兰氏阳性菌的活性大大提高,在有效性、安全性、耐药性方面均具有明显优势。
盐酸莫西沙星滴眼液历年审评趋势
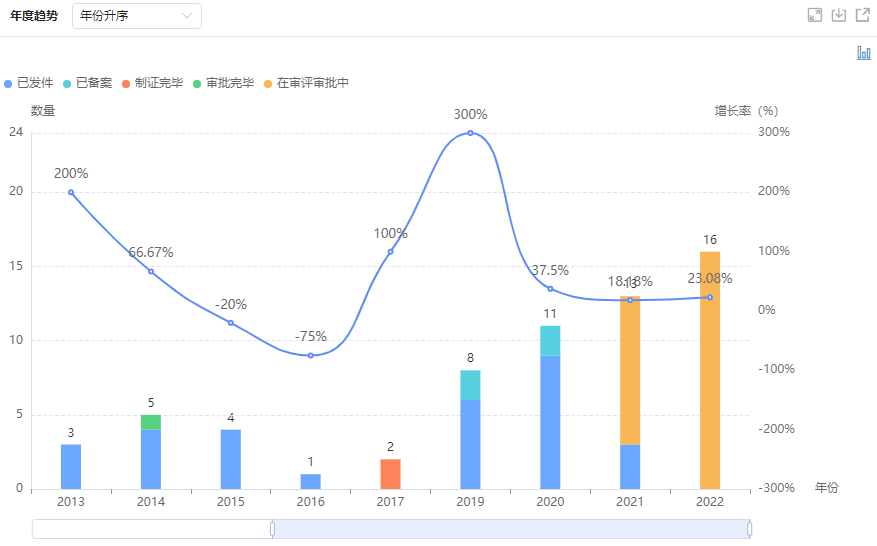
图片来源:药融云中国药品审评数据库
相比同类喹诺酮类滴眼液,盐酸莫西沙星滴眼液具有明显的临床优势,尤其是在儿童用药方面可用于包括婴幼儿(包括新生儿)在内的广大年龄层患者,该产品不含防腐剂,pH值近中性,能有效防止因加入防腐剂带来的眼睛局部刺激性及不良反应,对眼部组织有很好的渗透性,安全性好,副作用少。
盐酸莫西沙星滴眼液是继复方樟柳碱注射液、拉坦前列素滴眼液上市之后,华润紫竹药业推出的又一重磅产品。随着国内药企不断发力,眼用制剂市场也在不断壮大,2019年在中国公立医疗机构终端眼用制剂的销售规模已上涨至接近70亿元。
- 热门仿制药——玻璃酸钠滴眼液
玻璃酸钠滴眼液为治疗干眼症的药品,在国内使用较多。数据显示,2020年该产品院内销售额已经超8亿。2021年前三季度,该产品在全国医院的销售额更是逼近90亿,有望成为又一大百亿用药品种。
从市场份额来看,德国悟兹法姆药业占比较高,其次是参天制药,这两家药企产品2020年在院内占了超八成的市场份额。剩下的市场由珠海联邦、齐鲁制药、浙江尖峰药业等分羹。
目前在国内以新注册分类申报上市的企业已超20家,其中成都普什制药(首家过评)、江西珍视明药业、中山万汉制药、扬子江和中山万远等5家企业已经过评。
玻璃酸钠滴眼液-新注册分类仿制药申报企业TOP10
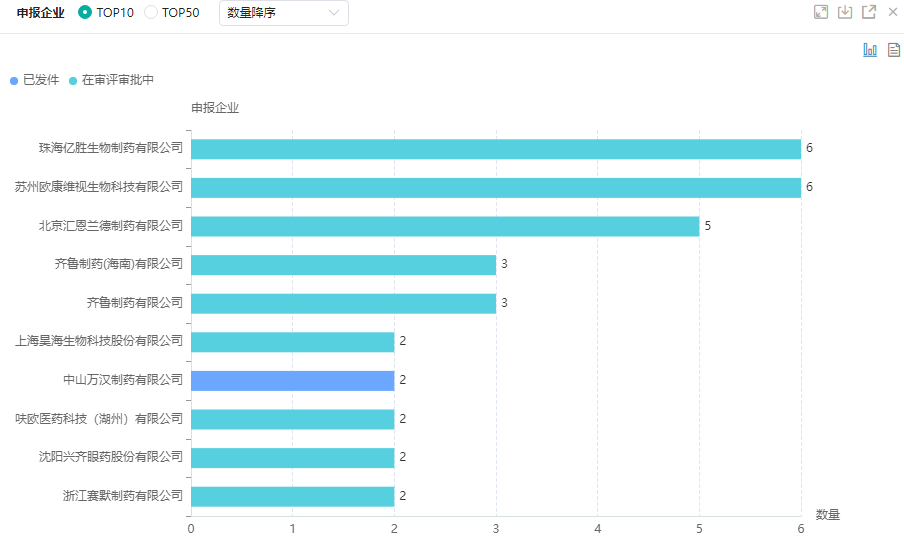
图片来源:药融云中国药品审评数据库
二、仿制药申报企业TOP10
截至2022年7月28日,获CDE承办的仿制药申报企业TOP10排名分别为:浙江赛默制药有限公司、石家庄四药有限公司、齐鲁制药有限公司、宜昌人福药业有限责任公司、浙江华海药业股份有限公司、江苏万高药业股份有限公司、南京海纳制药有限公司、成都苑东生物制药股份有限公司、湖南科伦制药有限公司、齐鲁制药(海南)有限公司。
2022年仿制药申报企业TOP10(截至2022.7.28)
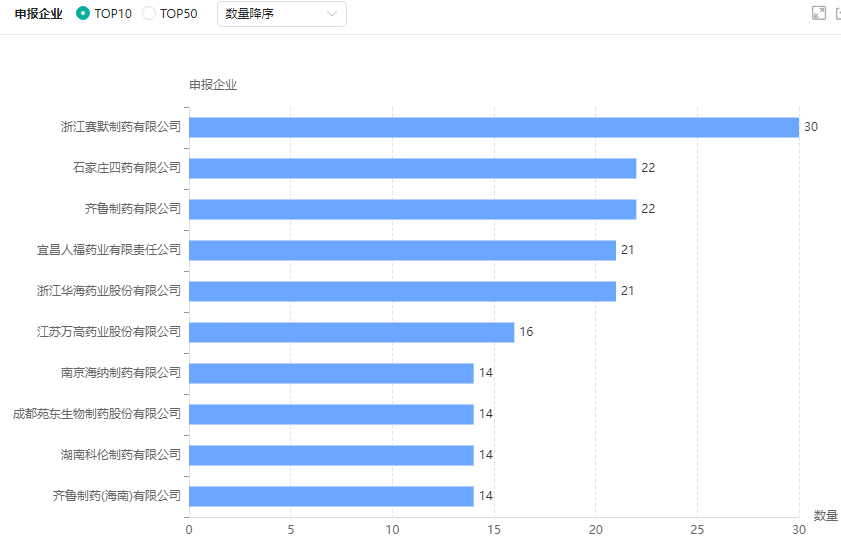
图片来源:药融云中国药品审评数据库
仿制药承办总数位列榜首的浙江赛默制药有限公司,成立于2019年,位于金华经济技术开发区生物健康产业园,是一家集原料药、制剂、医疗器械和保健食品的研发、生产、销售为一体的企业,主要生产原料药、口服固体制剂、口服液、贴片、软膏、注射液等产品。
仿制药承办总数位居第二的石家庄四药有限公司,是中国医药工业百强企业,始建于1948年,历经七十余年的历史变迁,现已发展成为大型综合制药集团,形成以化学制剂、原料药、中药制剂和医用包材为主,产业链较为齐全的新型产业发展格局。2007年在香港主板上市。
3月18日,石家庄四药有限公司开发的化学药品4类药品盐酸莫西沙星滴眼液、左氧氟沙星氯化钠注射液两产品取得国家药品监督管理局颁发的《药品注册证书》,并视同通过仿制药质量和疗效一致性评价。石家庄四药集团子公司申报的依帕司他原料药也获国家药品监督管理局批准,可在上市制剂中使用。截至6月下旬,石家庄四药有限公司共获批20个新产品项目,月均超过3个,申请报批新产品项目达31个。
石家庄四药申报药品TOP10
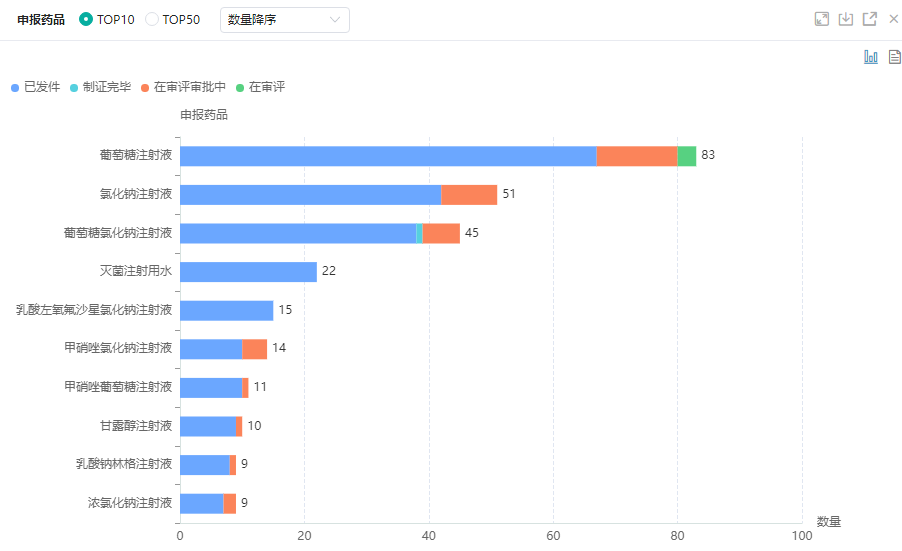
图片来源:药融云中国药品审评数据库
齐鲁制药有限公司是中国大型综合性现代制药企业,主要从事肿瘤、心脑血管、感染、精神系统、神经系统、眼科疾病的制剂及原料药的研制、生产与销售。2021年,齐鲁制药共有21款仿制药(37个品规)获批上市。其中,注射用头孢他啶阿维巴坦钠、甲磺酸雷沙吉兰片、二甲双胍维格列汀片等3个品种为国内首仿+首家过评。
2022年,齐鲁制药在传统仿制药方面收获颇丰。仅4月就已拿下3款仿制药,分别为枸橼酸托法替布缓释片(仿制药首家过评)、头孢丙烯片和磷酸奥司他韦胶囊,其中枸橼酸托法替布缓释片还是齐鲁制药首个获批的渗透泵工艺的口服缓控释制剂。
齐鲁制药药品申请情况分析
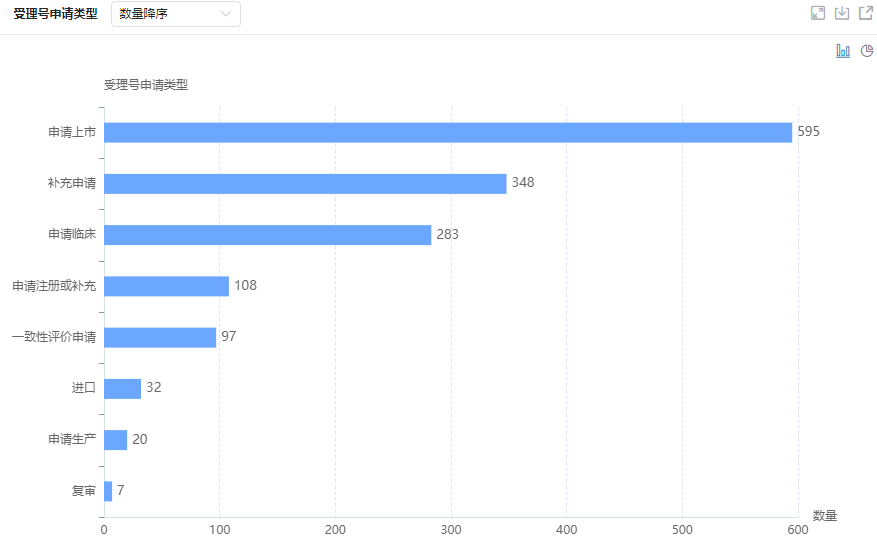
图片来源:药融云中国药品审评数据库
我国是仿制药使用大国,仿制药是我国医药市场的主导力量。据国家药品监督管理局统计,截至2017年底,中国有5000多家原料药和制剂生产企业,其中90%都是仿制药企业。近17万个药品批号中,95%以上都是仿制药。截至2019年,我国仿制药约占化学药市场的66%,占全部药品市场近半壁江山。
国内正在推进的仿制药一致性评价就是与国际接轨的手段之一,这正不断倒逼中国药企重视提升研发能力、工艺能力和质量管理能力。随着我国仿制药综合生产能力的提升,仿制药凭借原料药和品质优势,在全球市场正获得更多竞争力,出口前景也开始越来越广阔。
想要解锁更多仿制药信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握仿制药申报情况、药企审批信息、最新进展、一致性评价、市场竞争格局、销售情况,市场规模与前景,可否投入!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论