
研发界存在这样一种情形:《进口质量标准》已告知某杂质校正因子(如0.82),很多同仁不敢采用,买来价格不菲的对照品验证;更有甚者,用不同型号色谱柱/液相和标准曲线验证,结果却不一致(如0.68)。
为不辜负劳动成果,制定0.68上报至CDE后收到发补:请回答、为何色谱条件与进口质量标准一致、且波长未做改变,而杂质校正因子却与之不符?也就是说,审评老师怀疑您的验证结果。有同仁感到委屈,向本人咨询,回复:您这是自寻烦恼——根本无须验证、直接采用原研药色谱条件和杂质校正因子便是。
为此,将“无需验证观点”公布于朋友圈,得到多位同仁反馈、本人也做了互动交流,具体如下:
★有支持,不解为何还要验证的
★有豁然开朗、顿感轻松的
★有因药检所要复核,只好无奈先行验证;至于直接撷取、做梦都不敢想的 // 您直接采用,药检所就不复核了;正是因为贵公司重新验证,药检所才复核的
★有提升至“绝对值与相对值理论”高度的 // 研究生期间曾学过一门《模糊数学》课程,对我后来的工作影响极大。
★有断然否定、驳斥“做研发不能想当然”的 // 不是想当然,是勇于突破自我、跳出思维窠臼。不信您拿一品种试试,若成功,将节省的5万元奖励给研发人员,因本人始终坚持“研发不是做得越多越代表水平高,恰恰相反”思想。
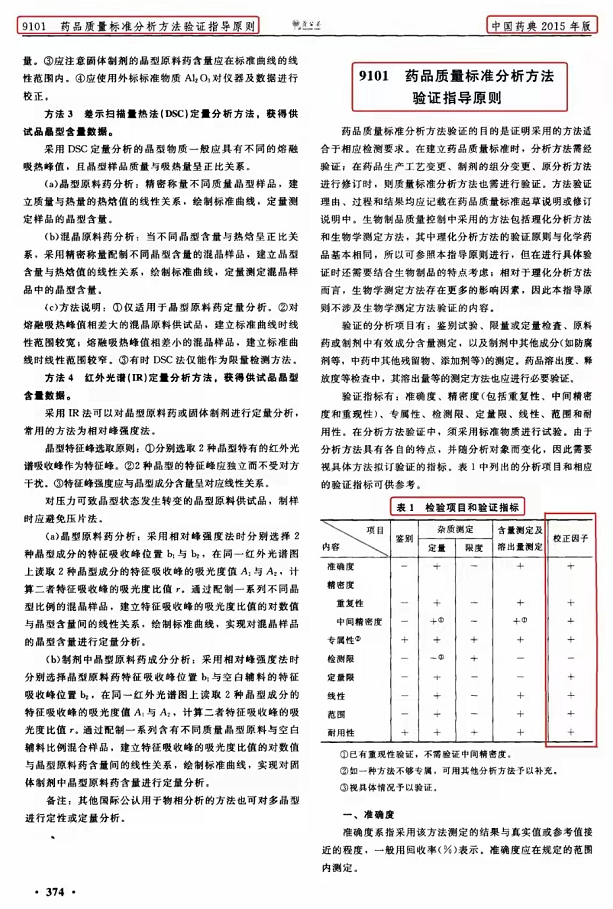
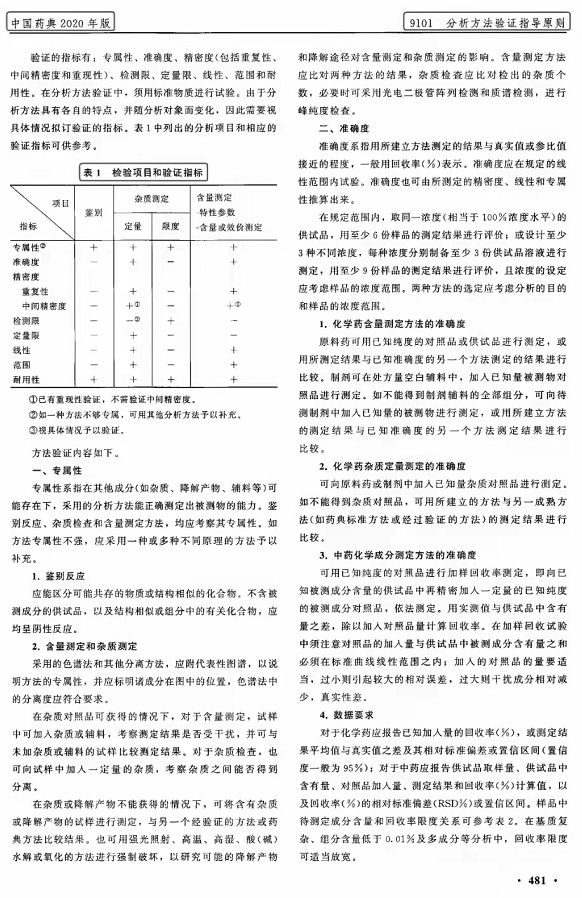
★最后一位同仁最棒:指出《2020年版中国药典-分析方法验证指导原则》已将2015年版验证指标中的“校正因子栏”删除,就是明确可以直接采用、无需再验证。在此,为起草该内容的药典委员点赞!
总之,分析工作没那么累人,相反是轻松快乐的,因为无需获得真值。不知各位读者怎么看?
【注】关于“参比制剂进口质量标准色谱条件为何一定适用于仿制原料药和仿制制剂(最多流动相微调)”属于杂质研究顶层设计范畴,不在本文讨论。
【声明】以上认知仅代表个人思考,不代表所在单位。还请异议者海涵,在此叩谢。
<END>






































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论