一、胃癌流行病学数据
1. 胃癌是全球及我国新发癌症第五位,发病率及死亡率均位居前列
2022年我国癌症新发病例数情况:新发病例数482.47万,其中胃癌35.87万人,排名第五;其中男女的发病率分别为:34.20/10万人、16.23/10万人。
2022年我国癌症死亡情况:死亡总人数257.42万人,其中胃癌26.04万人,排名第三。其中男女的死亡率分别为:25.18/10万人、11.41/10万人。
2022年全球新增癌症病例数达到1,996万例,其中胃癌(96.84万例,占比4.9%),排名第五。男性胃癌患者占总新增癌病病例数的比例为6.1%,女性为3.5%。
2022年全球癌症死亡病例共974万例,其中胃癌65.99万例,占比为6.8%,排名第五。男性肺癌患者死亡数量占所有癌症死亡病例数的比例为7.9%,女性为5.4%。

2. 靶向治疗和免疫治疗联合化疗正在成为晚期转移性胃癌的一线治疗标准
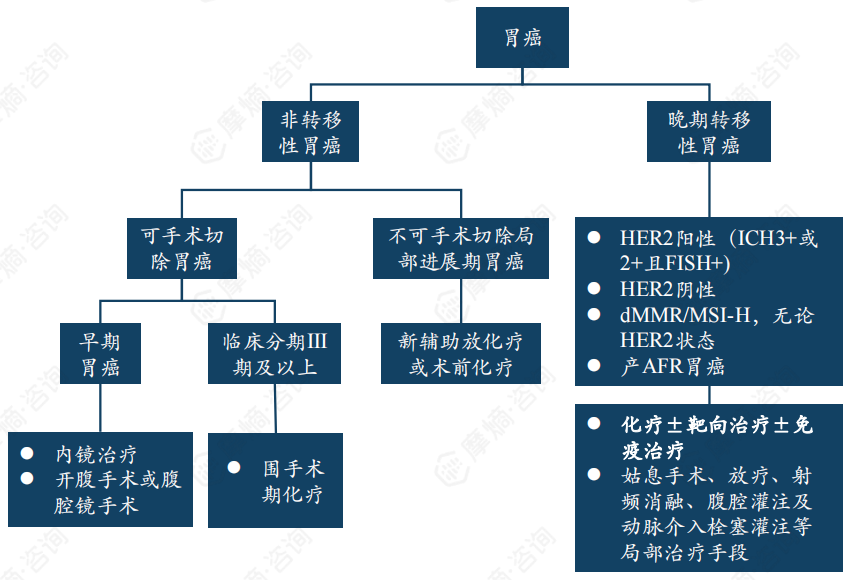
胃癌按照是否转移可分为非转移性胃癌和晚期转移性胃癌。
非转移性胃癌治疗通常比较直接,包括手术、化疗、放疗等,预后相对较好。
转移性胃癌治疗相对比较复杂,主要采用全身抗肿瘤药物治疗(化疗±靶向治疗±免疫治疗),治疗方案需要根据不同分子诊断结果制定个体化治疗方案。
胃癌靶向药物临床研究较多,已获批适应症的药物包括靶向HER2的曲妥珠单抗和维迪西妥单抗;VEGFR2药物雷莫西尤单抗及阿帕替尼。
免疫检查点抑制剂PD-1单抗单药疗效欠佳,PD-1单抗联合化疗成为不可切除局部晚期或转移性食管胃结合部/胃癌患者的一线治疗新标准。
3. 经病理学确诊晚期胃癌后根据分子分型指导治疗
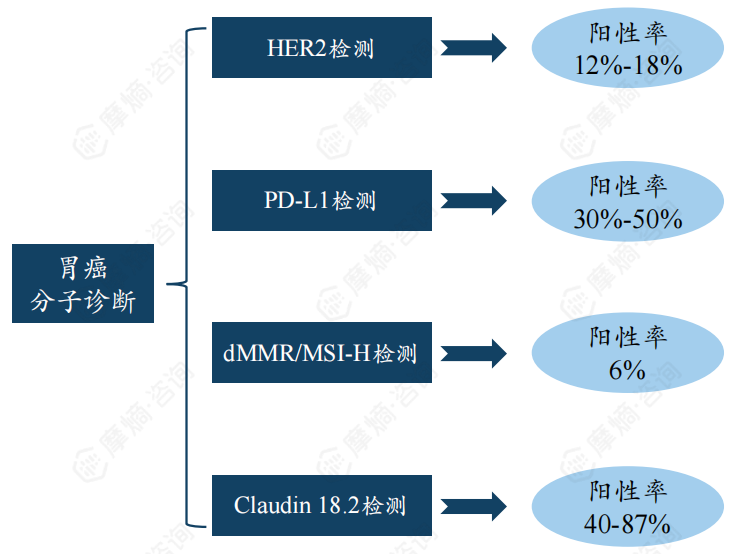
HER2:HER2阳性晚期胃癌患者可以从抗HER2治疗中获益,所有胃癌患者都应进行HER2检测。
PD-L1:通常检测肿瘤组织中的PD-L1表达情况预测免疫治疗疗效,PD-L1表达越高,免疫治疗效果越好。
dMMR/MSI-H:微卫星是指人类基因组中的短串联重复序列。肿瘤细胞中的微卫星常常由于重复单位的插入或缺失而导致微卫星的长度改变,称为微卫星不稳定性(MSI)。而错配修复蛋白(MMR)的缺失(dMMR)可造成肿瘤细胞DNA复制过程中的碱基错配修复功能缺陷,进而导致MSI的发生。目前MSI可分为三类:微卫星高度不稳定(MSI-H)、微卫星低度不稳定(MSI-L)和微卫星稳定(MSS)。通常MSI-H的肿瘤患者其TMB也较高,免疫治疗疗效会更好。
Claudin18.2:目前Claudin18.2检测阳性判断标准仅来自临床实验,不同的临床实验采用不同的判读标准。相较于HER2,Claudin18.2在胃癌人群中有更高的表达率。
二、胃癌诊疗指南及市场竞争格局分析
1. HER2
(1)曲妥珠单抗为基础的治疗方案仍是一线治疗标准选择
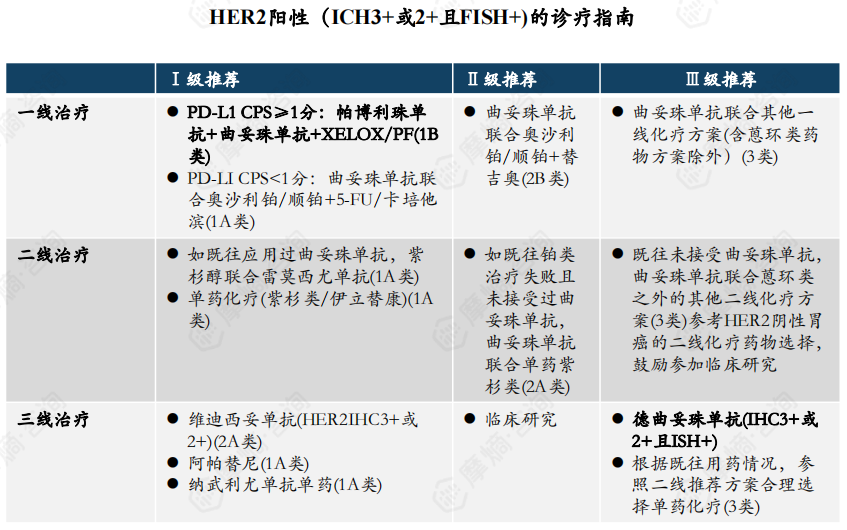
HER2是表皮生长因子受体家族重要成员,作为酪氨酸激酶受体在调节细胞增值、分化和生存等众多过程中发挥重要作用,胃癌中HER2阳性率约为12%-18%。
曲妥珠单抗为基础的治疗方案仍是一线治疗的标准选择。三线治疗中既往ADC只有维迪西妥单抗,本次将新型ADC德曲妥珠单抗(T-DXd/DS-8201)正式纳入指南推荐。目前在HER2阳性晚期胃癌三线治疗中国际上以德曲妥珠单抗为代表,国内以维迪西妥单抗为代表,但随着德曲妥珠单抗可及性提高,其他药物的份额可能被蚕食。
(2)曲妥珠单抗原研市场逐渐被生物类似药蚕食
2010年ToGA研究首次证明曲妥珠单抗结合化疗可以延长患者生存期,开启了胃癌HER2靶向治疗时代。但随后10年里针HER2靶点的药物帕妥珠单抗、拉帕替尼、奈拉替尼等多种药物在HER2阳性的胃癌患者中均未达到研究终点,这也造就了曲妥珠单抗的霸主地位。
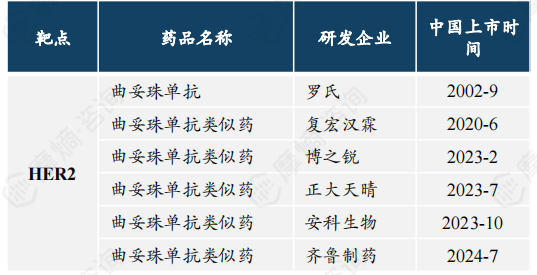
2002年曲妥珠单抗进入我国市场,但随着专利到期,2020年以来曲妥珠单抗生物类似药在我国相继上市,原研企业罗氏的市场份额已经下降至近60%,未来市场份额可能会被进一步蚕食。
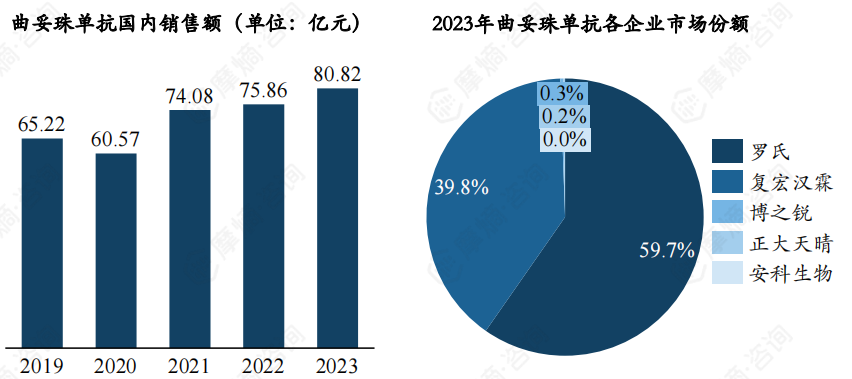
(3)曲妥珠单抗各级医院市场分析
据摩熵医药药物流向数据显示,以哈尔滨市为例,罗氏2023年各季度销售额均高于复宏汉霖。
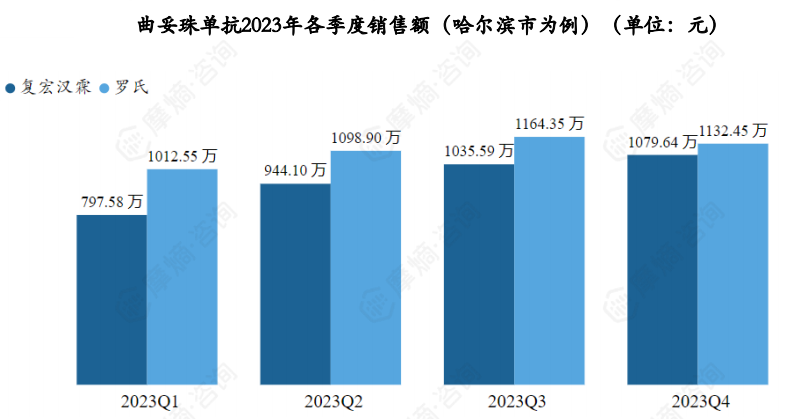

罗氏及复宏汉霖2023年销售市场主要在三级医院,其中复宏汉霖2023年未涉及一级及其它级别医院市场。
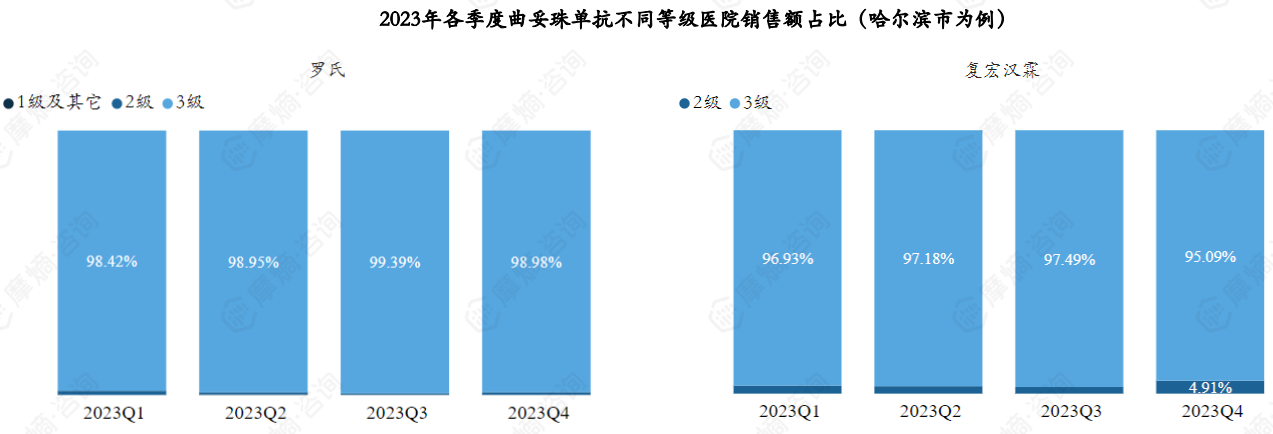
据摩熵医药药物流向数据显示,罗氏的曲妥珠单抗2023年销售额TOP3医院(哈尔滨市为例)分别为哈尔滨医科大学附属第三医院、哈尔滨医科大学附属第二医院、北大荒集团总医院。

复宏汉霖的曲妥珠单抗2023年销售额TOP3医院(哈尔滨市为例)分别为哈尔滨医科大学附属第三医院、北大荒集团总医院、宾县人民医院。

(4)ADC引领HER2阳性晚期胃癌精准治疗
近年来ADC药物在HER2阳性胃癌治疗领域蓬勃发展,打破了曲妥珠单抗独木难支的困境。多款创新ADC药物,诸如维迪西妥单抗、德曲妥珠单抗、anvatabartopadotin以及trastuzumabderuxtecan等,针对HER2阳性胃癌展现出了显著的治疗潜力与探索热情。推动了HER2阳性胃癌治疗向更加精准化、个体化的方向迈进,为患者带来了更多希望与选择。
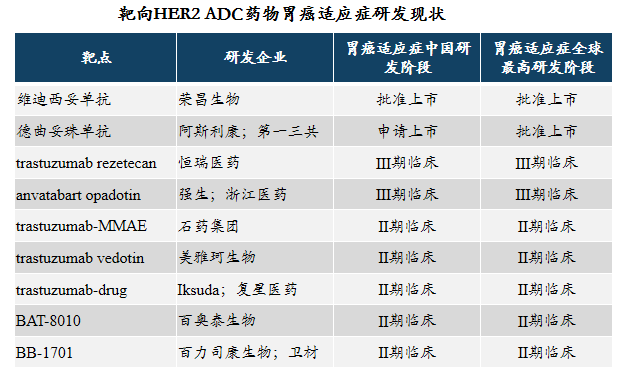
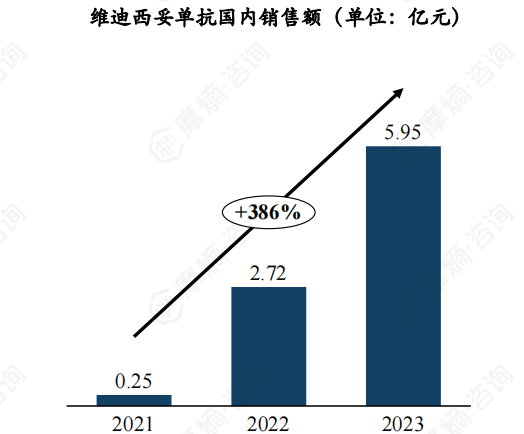
维迪西妥单抗是我国自主研发的HER2ADC类药物,在肿瘤抗HER2治疗中展现了广阔的应用前景,自上市以来销售额增长迅速,由2021年0.25亿增长至2023年5.95亿,年复合增长率达386%。
2. PD-(L)1
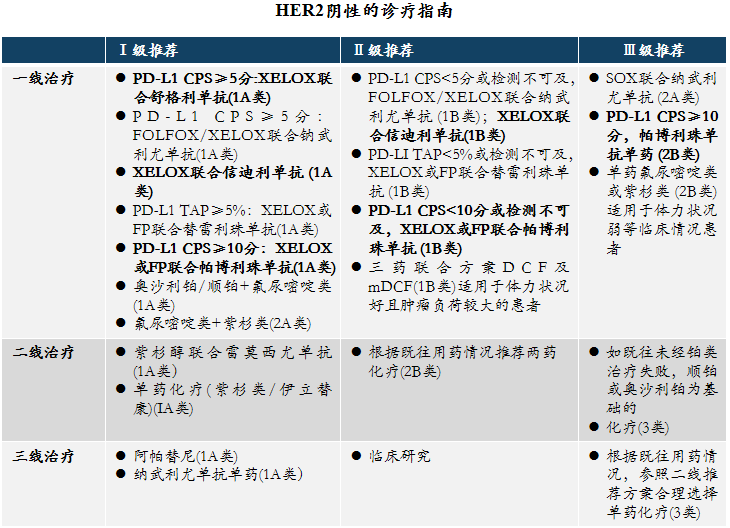
(1)PD-1/PD-LI单抗在HER2阴性胃癌治疗中快速发展
在精准医学时代,除HER2外,针对肿瘤细胞生长、浸润、血管生成的靶向治疗以及免疫治疗也显示出初步疗效,为HER2阴性患者带来新的希望。
针对HER2阴性胃癌,以PD-1和PD-L1为代表的国产免疫检查点抑制剂取得了快速发展。
2024CSCO指南新增舒格利单抗联合化疗作为PD-L1CPS≥5患者一线治疗方案;基于KEYNOTE-859研究,帕博利珠单抗联合化疗新增为PD-LICPS≥10患者的一线治疗方案。
PD-1/CTLA-4双抗卡度尼利单抗联合化疗一线治疗胃癌的III期COMPASSION-15临床试验,该研究证实PD-L1低表达患者仍能从免疫抑制剂治疗中获益,有望突破以往免疫联合治疗在胃癌PD-L1低表达人群中获益的限制。根据摩熵医药数据库显示,卡度尼利单抗胃癌适应症上市申请已在2024.1.5获CDE承办。
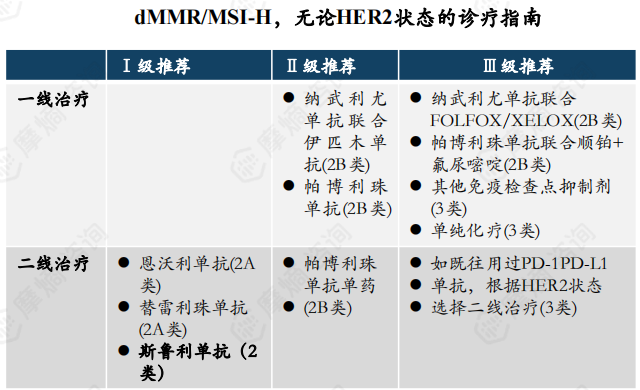
(2)dMMR/MSI-H患者中免疫单药长期生存获益更为明确
错配修复蛋白缺失(dMMR)/微卫星高度不稳定(MSI-H)胃癌约占晚期胃癌的6%。其分子分型特点、生物学行为、药物敏感性、肿瘤微环境、治疗模式及预后与pMMR/MSS患者存在巨大差异,主要特点为预后良好、化疗不敏感及免疫治疗获益明显。
在dMMR/MSI-H患者一线治疗中免疫单药及免疫联合化疗优于单纯化疗,免疫单药的长期生存获益更为明确。仅在免疫检查点抑制剂应用存在禁忌或不可及时考虑单纯化疗。
胃癌是高度异质性恶性肿瘤,其中产甲胎蛋白(AFP)胃癌约占3%,作为罕见亚型,具有易发生肝转移、淋巴结转移,伴AFP升高等特性。
2024年CSCO指南中首次提出对AFP胃癌予以SOX联合卡瑞利珠单抗/阿帕替尼一线治疗推荐。
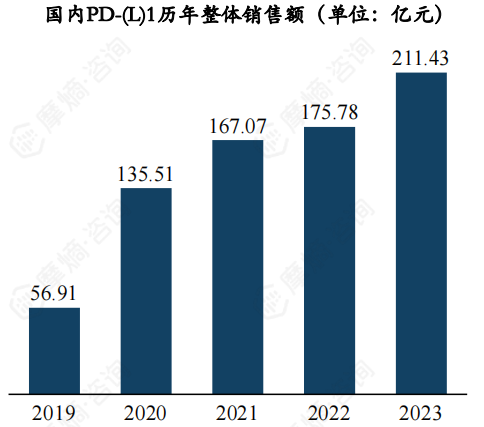
(3)PD-(L)1国内整体销售额突破210亿元,百济神州和信达生物名列前茅
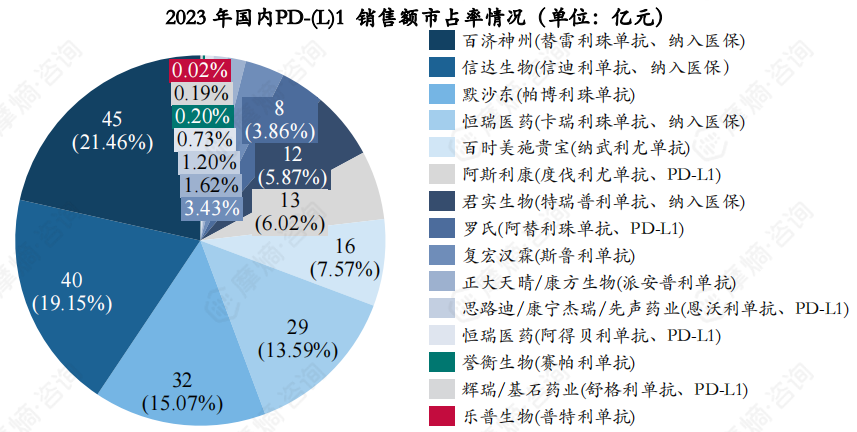
自2018年首款PD-(L)1在国内上市以来,截止目前已有15款PD-(L)1相继获批上市,销售额一路高歌猛进,从2019年57亿元增长至2023年211亿元。主要原因在于:1)显著的临床疗效;2)广泛的适应症范围,肺癌、肝癌、胃癌、黑色素瘤等多种肿瘤适应症都已获批上市。
从2023年国内销售额竞争格局来看,百济神州的替雷利珠单抗以45亿元的销售成绩市占率第一(21%),信达生物的信迪利单抗以40亿元的销售额排名第二,市占率为19%,排名第三的为默沙东的帕博利珠单抗,32亿元(15%),未纳入医保能有这么好的成绩在于帕博利珠单抗先发优势,广泛获批的适应症和默沙东超强的销售能力。
(4)信迪利单抗各级医院市场分析
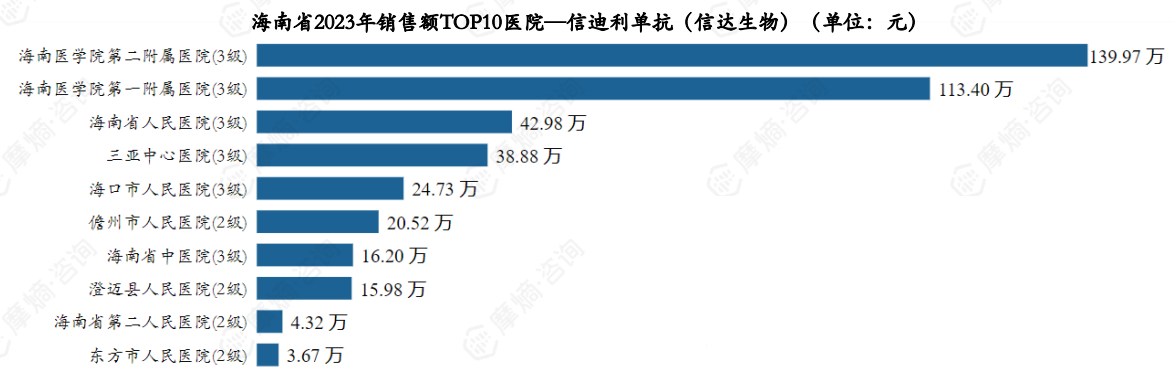
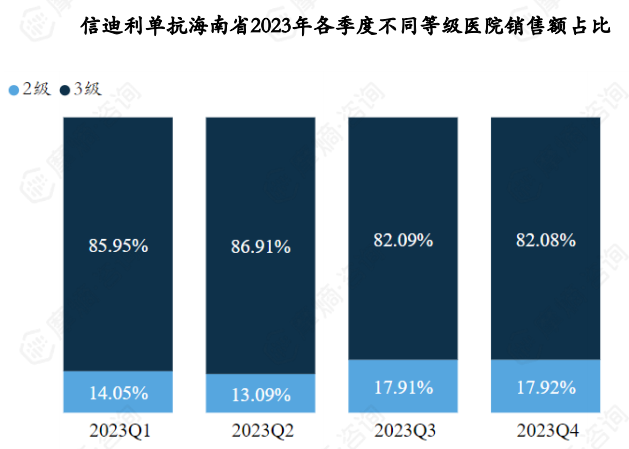
据摩熵医药药物流向数据显示,以海南省为例,信迪利单抗2023年销售额TOP3医院(海南省为例)分别为海南医学院第二附属医院、海南医学院第一附属医院和海南省人民医院。
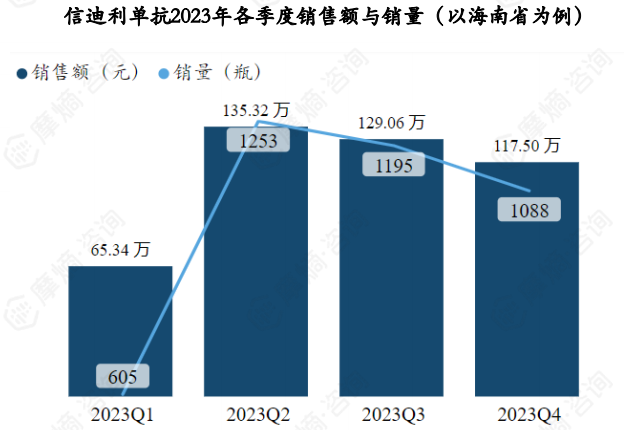
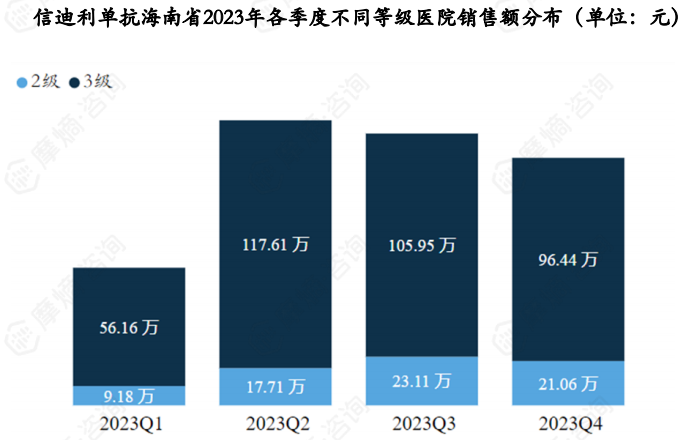
信迪利单抗2023年各个季度销售额主要在三级公立医院,2023Q2占比达到87%,2023Q4占比为82%。
3. VEGFR2
(1)阿帕替尼巅峰已过,雷莫西尤放量在即
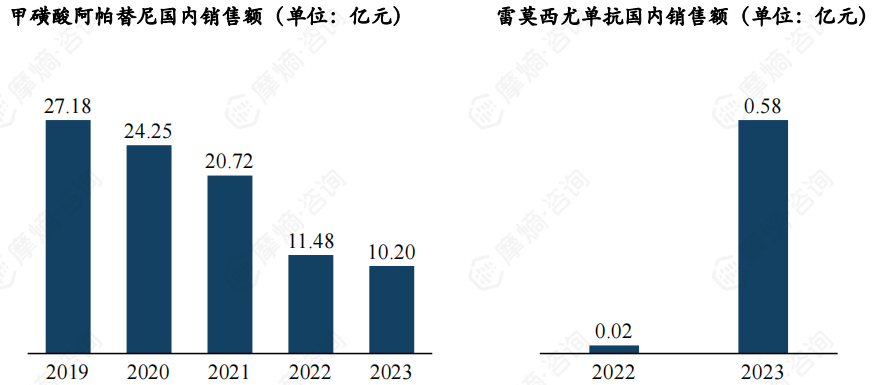
甲磺酸阿帕替尼由恒瑞研发,是全球第一个晚期胃癌小分子靶向药物,也是恒瑞自主创新转型的见证。阿帕替尼销售额峰值为2019年27.1亿元,近年来销售额持续下降,截至2023年仅为10亿元。
国内胃癌已获批VEGFR2药物

雷莫西尤单抗由礼来开发,信达生物负责商业化,与2022年3月在我国获批上市,是国内首个且唯一被批准用于晚期胃癌二线治疗的抗血管靶向药物,因其上市时间较短,2023年销售额仅0.58亿元。
三、胃癌市场趋势分析
1. CLDN18.2有望成为胃癌靶向治疗理想靶点
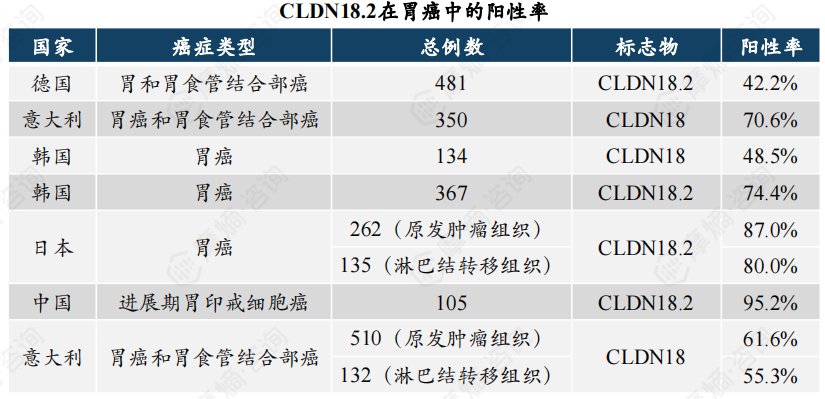
紧密连接蛋白(Claudin,CLDN)在邻近细胞间可形成紧密通道,调控离子、溶质等物质流通。CLDN18.2在胃癌、食管癌等恶性肿瘤中特异性高表达,且肿瘤细胞因增殖快、易侵袭转移等特性丧失紧密连接结构,导致其表面的CLDN18.2分子表位更易暴露出来。因此CLDN18.2在众多潜力型靶点中脱颖而出,有望成为胃癌靶向治疗理想靶点。CLDN18.2可开发成多种不同类型药物,包括单抗、双抗、ADC、CAR-T。
ICH是目前应用最广泛的检测手段,不同研究中CLDN18.2的表达值存在较大差异,不同种族之间阳性率差异性较高。在一项中国人群的研究中,胃印戒细胞癌CLDN18.2的阳性率高达95.2%。
2. 佐妥昔单抗是首个上市的CLDN18.2靶向药物
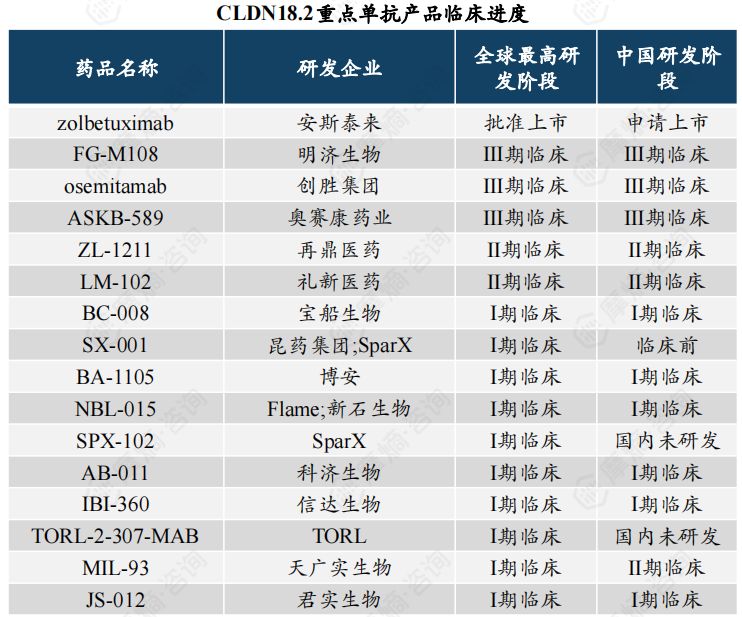
单克隆抗体可特异性结合表达CLDN18.2的肿瘤细胞从而诱导ADCC和CDC效应并导致细胞裂解。目前全球共有4款三期以上CLDN18.2单抗产品。
2024年3月安斯泰来宣布其创新药物佐妥昔单抗(Zolbetuximab)获日本厚生劳动省批准,用于治疗不可切除晚期或复发性CLDN18.2阳性胃癌,这是首个针对CLDN18.2的靶向疗法。
2023年10月创盛集团osemitamab临床数据优越,具备BIC潜力。
2024年1月奥赛康药业ASKB589+CAPOX+PD-1抑制剂的Ⅰb/Ⅱ临床研究中ASKB589表现出良好的有效性、安全性及耐受性。
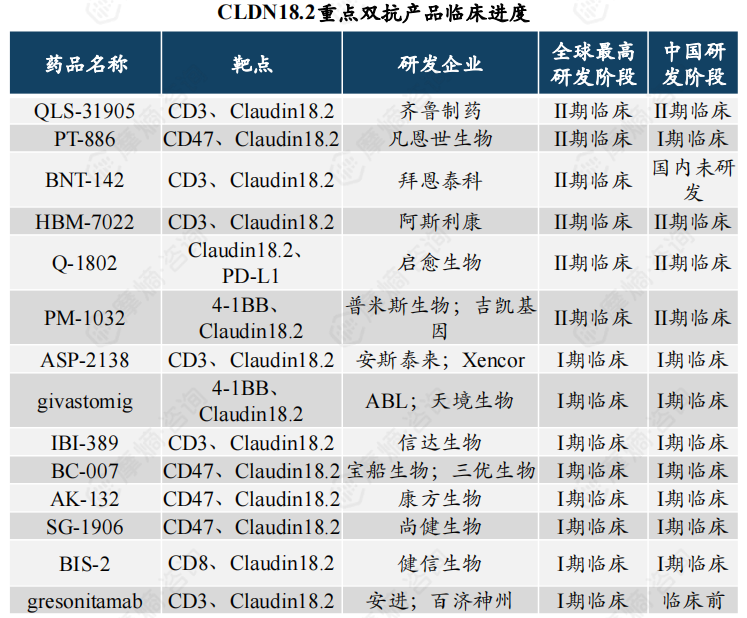
3. CLDN18.2双抗另一个靶点设计大多针对免疫细胞,如CD3、CD47、4-1BB
双抗药物可以同时特异性结合2个抗原或抗原表位的人工抗体,已成为近几年新药研发的热点。
目前关于CLND18.2双抗的另一个靶点大多针对免疫细胞相关分子设计,旨在发挥抗肿瘤免疫作用。主要为CD3/CLDN18.2、CD47/CLDN18.2、4-1BB/Claudin18.2、PD-1/CLDN18.2这几类。
研究表明CD47-SIRPα信号轴是是癌症的先天免疫检查点,抗CD47和抗SIRPα可以阻断CD47-SIRPα抑制信号并促进巨噬细胞对肿瘤细胞的吞噬。目前已有多个CD47/CLDN18.2双抗进入临床阶段。如PT-886已进入Ⅱ期临床,BC-007、AK-132、SG-1906也已进入Ⅰ期临床。
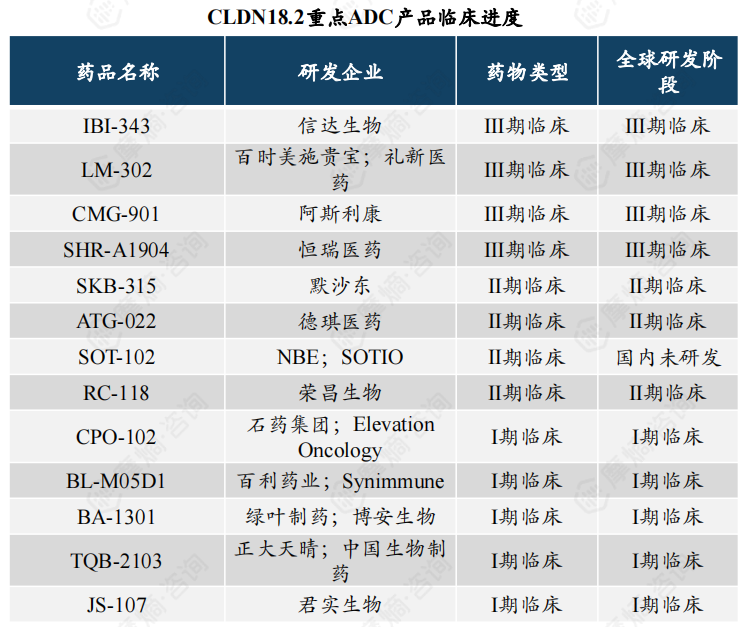
4. ClDN18.2ADC陆续进入临床阶段
ADC药物是最近几年抗肿瘤领域非常火热的领域,由具有生物活性的细胞毒性药物和mAb通过化学键连接而成,并由mAb搭载细胞毒性药物进入特定细胞发挥肿瘤杀伤作用。
胃癌领域目前研究最多的ADC药物主要聚焦在HER2靶点上,但靶向CLDN18.2的ADC药物也在陆续进入临床阶段。
部分ADC药物由CLDN18.2单抗与单甲基澳瑞他汀E结合而成,如CMG-901、LM-302、COP-102;部分ADC药物由CLDN18.2单抗与DNA拓扑异构酶抑制剂结合而成,如SHR-A1904、SOT-102等。
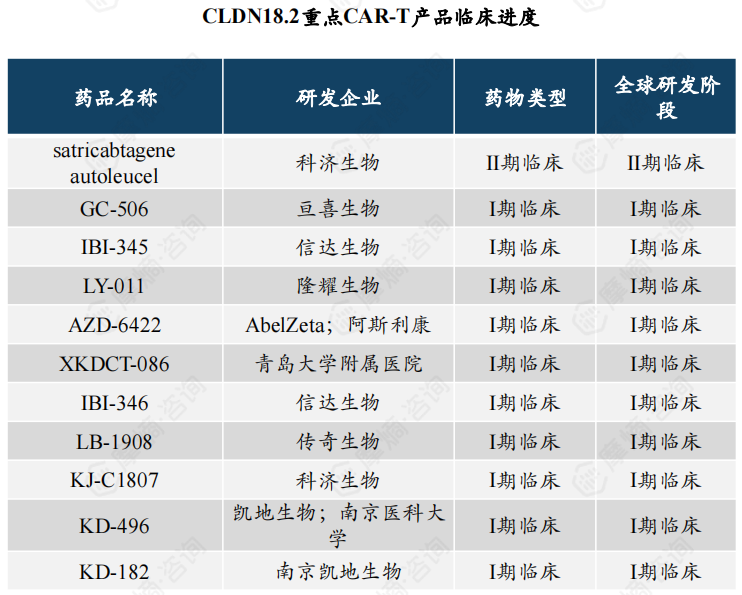
5. satricabtageneautoleucel是目前研发进展最快的CLDN18.2CAR-T疗法
CAR-T是通过基因工程手段,在T细胞的细胞膜上嵌合某种特定肿瘤抗原受体基因,形成修饰的T细胞,进而可特异性识别和结合肿瘤细胞表面的抗原,并引导T细胞杀伤特定的肿瘤细胞。
Satricabtagene autoleucel是目前研发进展最快的CLND18.2靶向的CAR-T,也是在胃癌领域取得较好结果的CAR-T。在中国人群中开展了Ⅰ期临床试验,中期分析结果显示,CT041治疗既往接受过治疗的CLDN18.2阳性消化系统肿瘤患者的耐受性良好,总体人群ORR为48.6%,DCR为73.0%;在胃癌患者中,ORR为57.1%,DCR为75.0%,6个月OS率为81.2%。
6. 胃癌仍有较大的未满足临床需求
晚期胃癌整体预后不佳,单纯化疗效果提升进入瓶颈期,靶向药物选择有限,免疫单药在整体人群中疗效不佳,PD-1单抗联合化疗已成为一线治疗优先选择,但免疫联合策略有待进一步优化和提升。
基于已公布的临床数据,CLDN18.2有望成为胃癌的第二个精准治疗靶点,左妥昔单抗已验证其胃癌成药性,国产药物研发势头正盛。2024 CSCO胃癌指南也推荐患者在术后进行IHC检测以评估CLDN18.2表达情况,在CLDN 18.2靶向药物获批上市后,晚期复发患者能够根据既往检测结果及时接受相应靶向治疗。一线治疗方案预计为CLDN18.2单抗联合化疗联合/不联合PD-1单抗。
国内多款药物胃癌适应症处于申请上市阶段,有康方生物的卡度尼利单抗、阿斯利康的德曲妥珠单抗、和记黄埔医药的呋喹替尼和安斯泰来的左妥昔单抗。
卡度尼利单抗:临床结果显示无论PD-L1表达,卡度尼利联合方案对比化疗可大幅度延长患者总生存周期和降低死亡风险,即使对于PD-L1低表达人群也具有同样优异的疗效,有望弥补PD-1单抗一线治疗PD-L1低表达胃癌疗效有限的短板。
德曲妥珠单抗:临床结果显示德曲妥珠单抗是首个且唯一治疗HER2阳性晚期后线胃癌mOS超越1年的方案,ORR51%。基于此数据2024版COSO胃癌指南也将德曲妥珠单抗推荐用于HER2阳性晚期胃癌后线治疗。
左妥昔单抗:GLOW(中国注册研究)实验结果显示与接受安慰剂和含铂化疗的患者相比,佐妥昔单抗与含铂化疗联合使用的患者PFS显著改善,疾病进展或死亡风险降低了31.3%。GLOW达到了无进展生存期的主要终点,中位PFS为8.21个月(对照组为6.80个月)。同时,组合疗法还显著延长了患者的OS,中位OS达到14.39个月(对照组为12.16个月)。首个且唯一获得世界监管机构批准的CLDN18.2靶向疗法,开创了晚期CLDN18.2阳性、HER2阴性胃癌治疗新纪元。
以上内容均来自摩熵咨询{市场研究专题报告—胃癌药物},如需查看或下载完整版报告,可点击!
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!



















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论