
2022年有哪些生物医药领域值得期待?4月份又有哪些疾病领域比较热门?有哪些潜力靶点值得关注呢?来看看药融云《4月全球在研新药与靶点月报》——热门疾病领域与潜力靶点的扫描与解析。
一、2022年4月热门疾病领域扫描
截至2022年4月29日,新冠肺炎在全球已有累计确诊病例约5.10亿,已造成死亡人数约625万人。目前奥密克戎毒株在全球新增感染患者中的占据比例已经接近100%,其具有高传染性、轻症特征,综合考虑奥密克戎变异毒株的特性和全球新冠肺炎疫情走势,可以确定新冠肺炎疫情仍然呈现反复和不确定性较大的特点。
自新冠疫情爆发以来,全球各大制药企业和科研机构致力于开发可有效预防新冠病毒感染的疫苗以及新冠的有效治疗药物。根据药融云数据统计,目前全球已有50余款药物(含疫苗)获批新冠适应症,其中包括12款小分子化药,30余款生物药。
从作用机制上来看,已获批小分子化药中,RdRp抑制剂(RNA以来的RNA聚合酶抑制剂)共有3款,分别为吉利德的瑞德西韦、 富山化学的法匹拉韦、默沙东的molnupiravir;此外,还包括辉瑞的3CL蛋白酶抑制剂Paxlovid 、COVID19复制酶多蛋白1a抑制剂组合药物奈玛特韦+利托那韦,Incyte的JAK抑制剂巴瑞替尼等。
获批小分子化药对比图
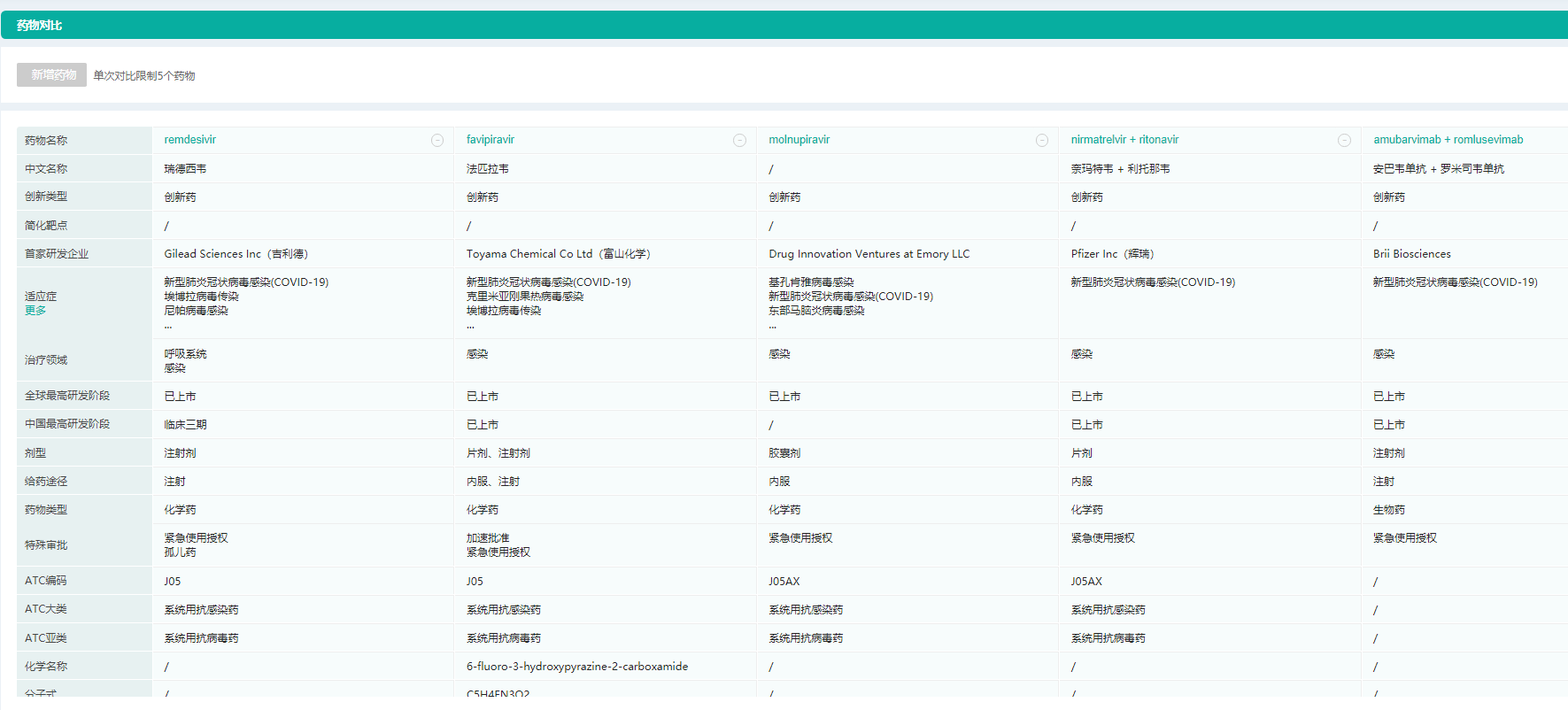
图片来源:药融云全球药物研发数据库—药物对比
生物药大类中,作用机制为COVID19刺突糖蛋白调节剂的药物数量占比最高(约为50%);从疗法类型来看,除疫苗以外,中和抗体占多数,包括sotrovimab、卡西瑞单抗+伊德单抗、巴尼韦单抗等,此外,tozinameran、elasomeran、ZyCoV-D等核酸类药物也被批准用于新冠治疗。
COVID19研发阶段及原研企业统计图
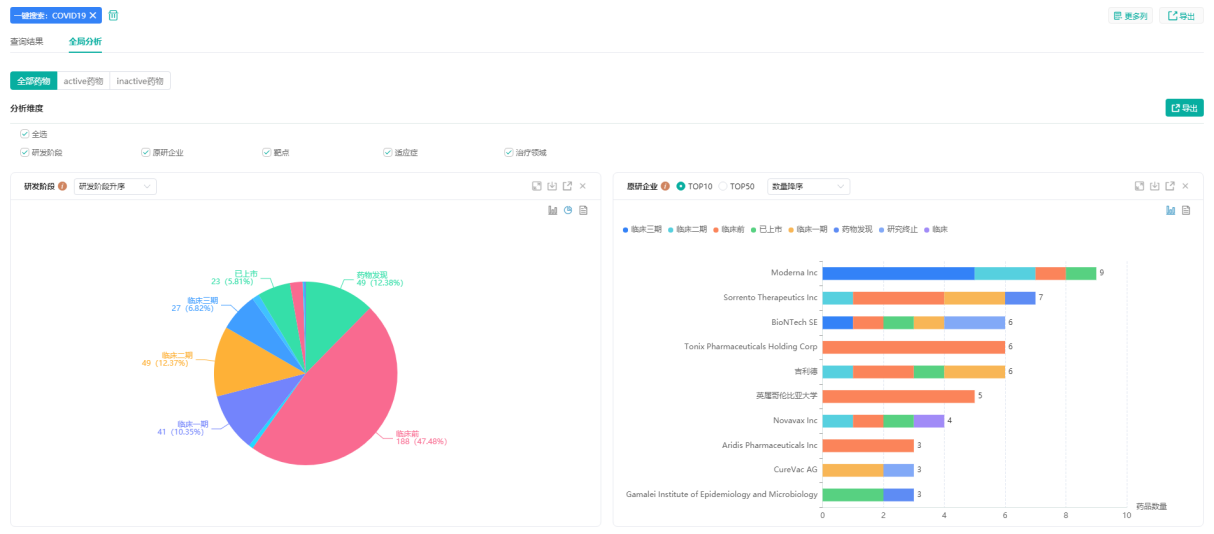
图片来源:药融云全球药物研发数据库—全局分析
目前国内共上市十余款新冠药物(含疫苗),包括口服药物法匹拉韦、奈玛特韦+利托那韦,中和抗体安巴韦单抗+罗米司韦单抗等,其中多数为紧急使用授权/附条件批准。从市场表现来看,2020年5月由FDA批准上市的瑞德西韦在其上市首年全球销售额就达到了28.11亿美元。
据药融云数据统计,截至2022年5月5日全球在研新冠药物共有1200余个,IND及以上研发阶段的项目占比近50%,其中临床一期132个,临床二期275个,临床三期161个,提交上市申请15个,涉及企业1000余家,由此可见,新冠药物已然成为全球药企争相布局的热门赛道。
从疗法类型来看,随着默沙东公司和辉瑞公司先后递交Molnupiravir和Paxlovid的紧急授权申请,口服小分子药物已成为抗COVID⁃19药物研发热点。
默沙东Molnupiravir上市时间轴及研发状态
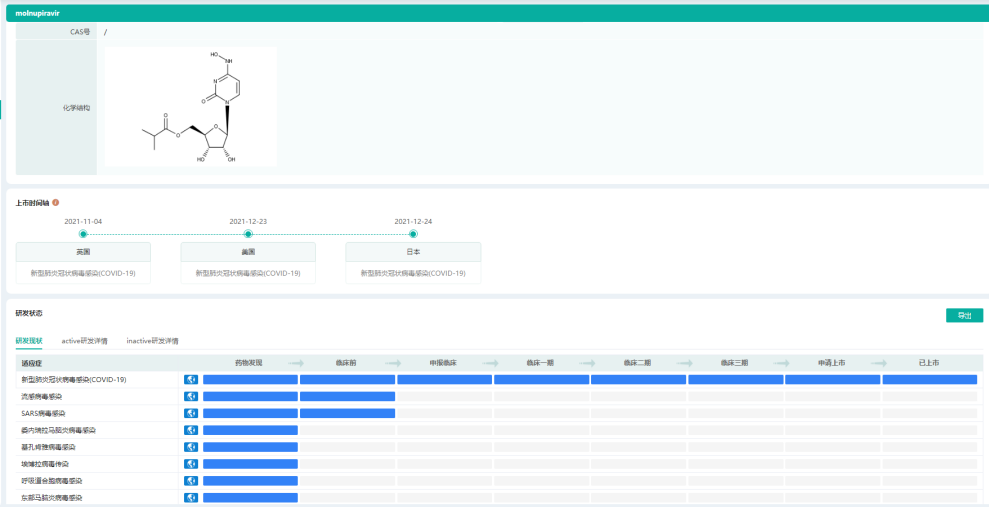
图片来源:药融云全球药物研发数据库
相比于需要注射给药的瑞德西韦和中和抗体药物,口服小分子药物具有更多优势:
①患者耐受性高,依从性好,便于在患者感染早期就抑制病毒的增殖,避免转化为重症。
②价格低廉,莫匹那韦在美国的定价为700美元/人,仅为中和抗体的三分之一。
③便于运输,易于分发。相较于需要静脉注射的抗体药物,口服小分子药物无疑方便许多,在疫情严重、医疗条件落后的不发达国家,口服小分子抗病毒药物更为实际。与中和抗体相比有较大的优势与应用前景。
从国内企业参与情况来看,目前国内共有100余家企业参与新冠药物研发,涉及研发项目150余个,仅四月以来,包括君实生物、开拓药业、科兴制药、歌礼制药等在内的多家公司就其口服新冠药物披露最新消息,研发势头正盛。
君实生物—各适应症药品数量统计图
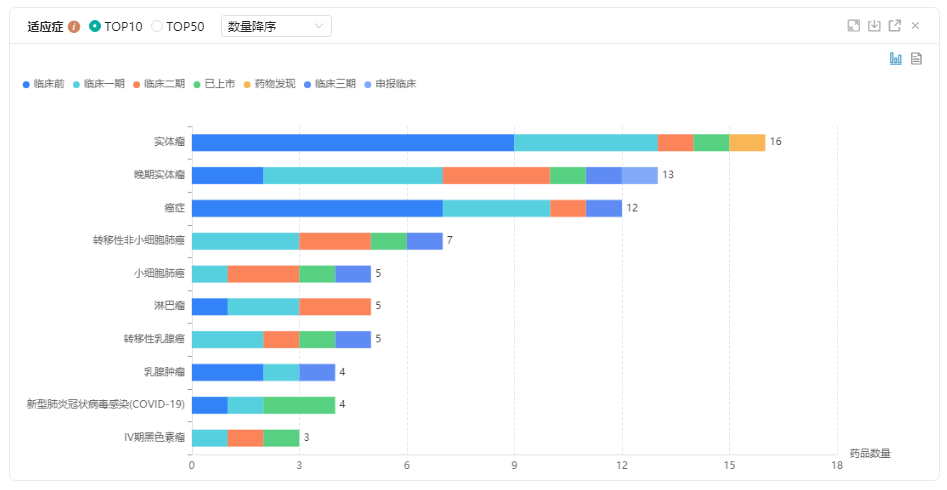
君实生物—各靶点药品数量统计图
图片来源:药融云全球药物研发数据库
君实生物的VV116为一款RdRp抑制剂,由中国科学院上海药物研究所、中国科学院武汉病毒研究所、中国科学院新疆理化技术研究所、旺山旺水、中国科学院中亚药物研发中心共同研发。
2021年10月,君实生物宣布与旺山旺水达成合作,共同承担该药物在全球范围内的临床开发和产业化工作。这款药物已在乌兹别克斯坦获紧急使用授权,这是继默沙东、辉瑞新冠口服药获批之后,全球又一个获批上市的新冠口服药。
开拓药业的普克鲁胺为雄激素受体拮抗剂,原本为治疗前列腺癌的药物,新冠疫情发生后,临床试验证实该药对新冠具有治疗作用。2021年12月27日,开拓药业发布了其新冠口服药普克鲁胺治疗新冠非住院患者全球多中心临床试验的进展报告,但情况并不理想。
据显示,该项III期临床试验的中期分析未达到统计学显着性,对此,开拓药业表示将调整方案继续推进。2022年4月6日,开拓药业公布了普克鲁胺疗新冠肺炎轻中症的全球多中心三期临床积极结果。
pruxelutamide研发状态及临床试验信息
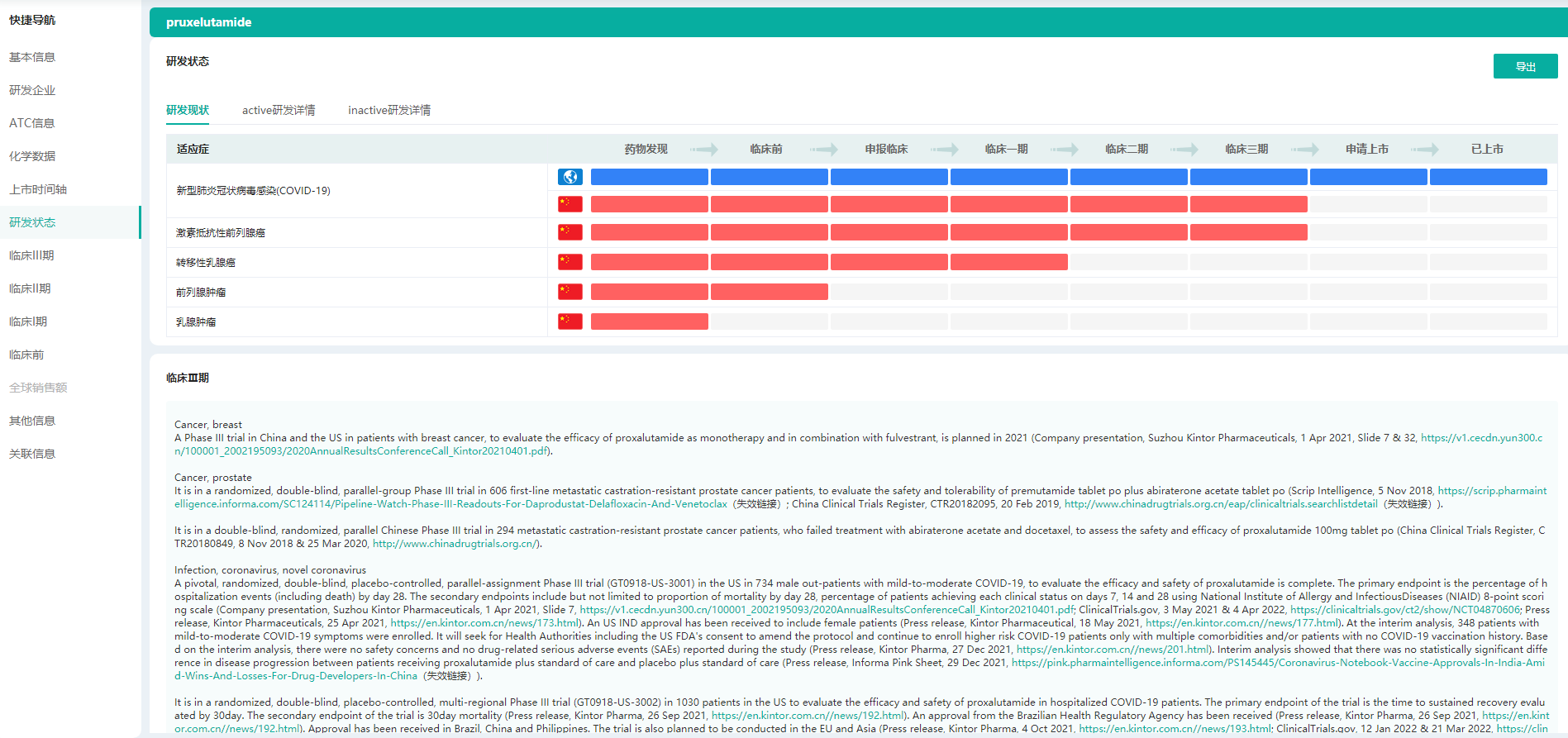
图片来源:药融云全球药物研发数据库
国产新冠口服药争分夺秒,激烈的角逐背后,谁将率先突围?我们拭目以待。
除了新冠,以下重点资讯也值得关注:
(1)FDA撤销GSK/Vir新冠抗体疗法紧急使用授权
(2)开拓药业普克鲁胺全球多中心三期临床成功
(3)君实生物新冠口服药VV116可用于治疗RSV感染
(4)歌礼制药新冠口服药3CLpro抑制剂ASC11拟报临床
(5)君实启动新冠口服药VV116对比辉瑞Paxlovid头对头III期临床
(6)WHO更新COVID-19治疗指南 强烈推荐辉瑞新冠口服药Paxlovid
(7)盐野义:新冠口服药S-217622可快速清除病毒
(8)首个用于12岁以下儿童的新冠药物!吉利德Veklury获美国FDA批准
(详细内容请前往“药融云(gh_d20f87bd52d9)”公众号查看报告全文)
二、2022年4月潜力靶点扫描
- 1.KRAS抑制剂
RAS是肿瘤中突变最为广泛的癌基因, 大约30%的肿瘤中含有RAS突变。 KRAS、 HRAS和 NRAS 3种亚型均被发现在肿瘤中存在突变, 其中以 KRAS 突变最为常见, 占RAS突变的80%左右。
KRAS突变在胰腺癌、非小细胞肺癌和结直肠癌中最为常见, 特别是在胰腺癌中高达 90%。尽管 KRAS 突变在肿瘤中的重要作用已经得到了广泛共识,但长期以来并无靶向 KRAS的药物获批上市。一度被认为是“不可用药”。
KRAS 抑制剂难以成药的原因,一是由于 KRAS 蛋白的空间结构缺乏较深的疏水口袋, 阻碍了高亲和力抑制剂的识别;二是 KRAS 作为 GTP 酶,相对一般激酶(Kinase)的纳摩尔级别结合亲和力,KRAS与底物皮摩尔级别的结合亲和力是非常高的。而且 KRAS 的底物 GTP在细胞内的浓度又很高,这也使得直接靶向GTP口袋的核苷酸竞争抑制剂难以开发。
直到 2013年,UCSF(加州大学旧金山分校)的Kevan Shokat 教授在 Nature 上首次发表 KRAS G12C的小分子共价靶向策略,这一进展推动了相关在研新药进入下一个开发阶段。
2021年5月29日,美国 FDA 宣布,加速批准安进(Amgen)公司开发的 Lumakras (Sotorasib,AMG510)上市,用于治疗肿瘤携带 KRAS G12C 突变的非小细胞肺癌(NSCLC)患者,这些患者至少接受过一种前期全身性治疗。
Lumakras基本信息/ATC信息/化学数据/上市时间轴
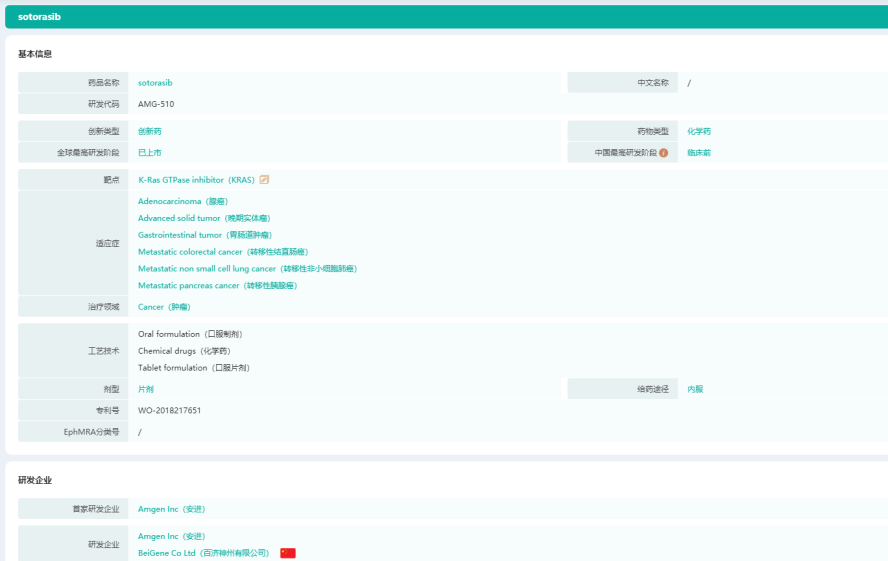
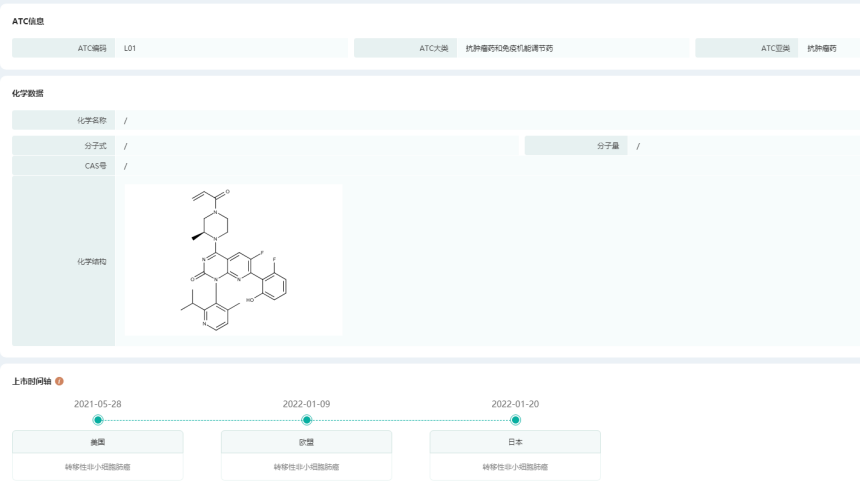
图片来源:药融云全球药物研发数据库
从 1982~83年,KRAS被确定是人类肿瘤的致癌基因,到2021年新药上市,科学家花了整整40年,才第一次成功开发出了针对这个基因的靶向药,也是全球首款靶向特定 KRAS 基因突变的抗癌药物。2021年,Sotorasib全球销售额达到 2952.47万美元,未来有望持续放量。2021年1月, Sotorasib被 NMPA 纳入“拟突破性治疗药物品种”。
根据药融云数据统计,截至2022.05.05,全球针对KRAS靶点的在研项目共有103个,其中药物发现阶段28个,临床前51个,临床一期12个,临床二期10个,临床3期1个,提交上市申请1个,总体来看,IND及以上研发阶段的药物数量占比不到四分之一。
KRAS靶点不同研发阶段药品数量
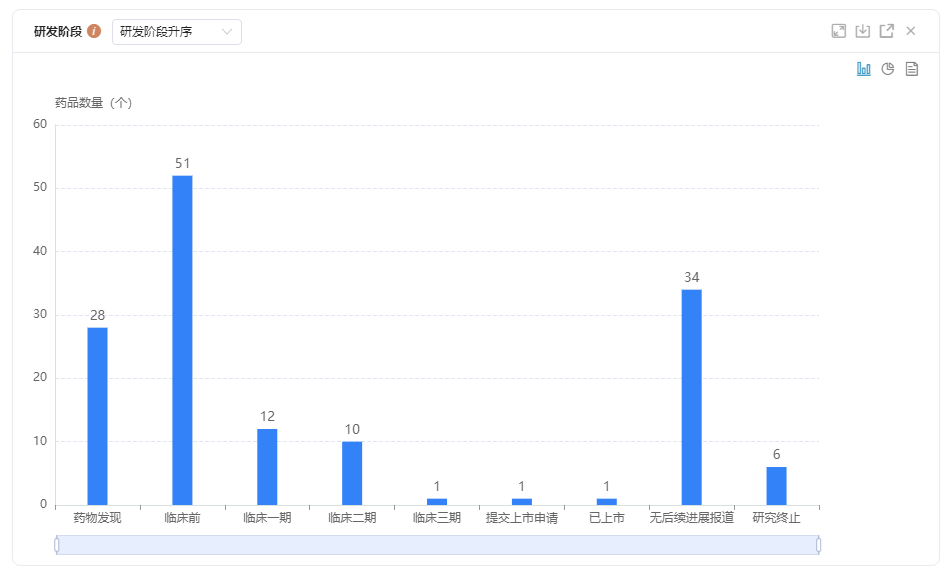 图片来源:药融云全球药物研发数据库
图片来源:药融云全球药物研发数据库REVOLUTION Medicines、北京加科思、PhoreMost、Mirati Therapeutics、Cellworks Group等为全球研发参与度较高企业,其中Mirati公司(MRTX)的Adagrasib在相关临床研究中表现不俗,有望成为继Sotorasib之后第二款上市的KRAS抑制剂。
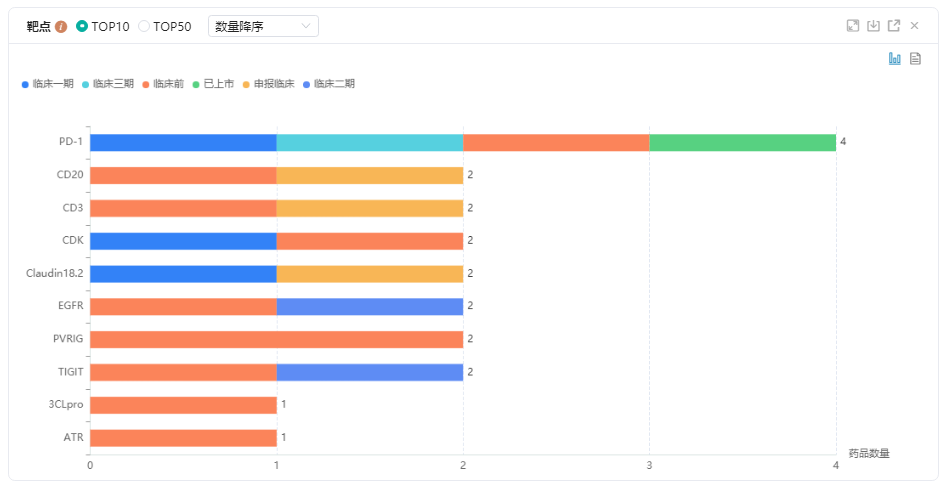
KRAS抑制剂原研企业TOP10
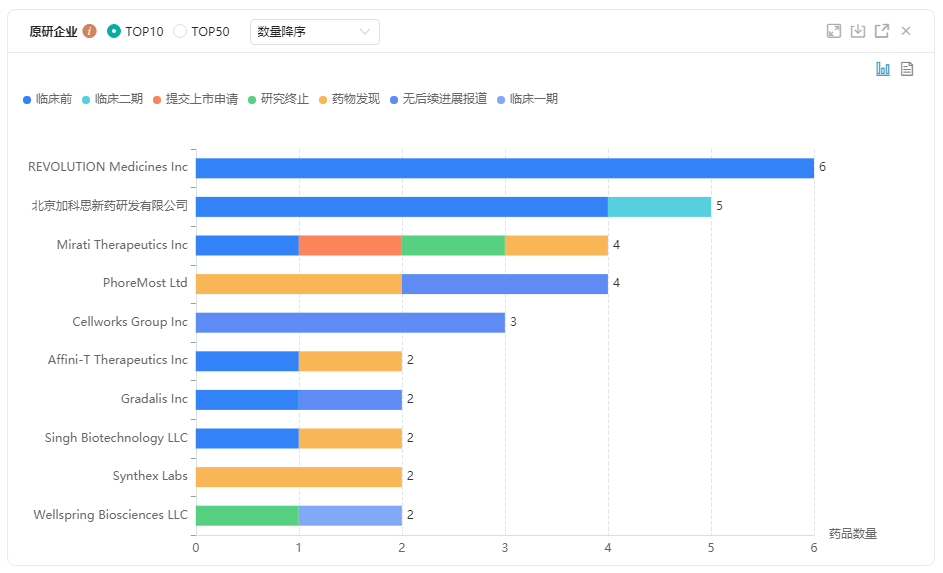
图片来源:药融云全球药物研发数据库
在研适应症中,胰腺癌、大肠癌、非小细胞肺癌等为研发热度较高的领域。KRAS抑制剂目前面临的挑战在于,KRAS G12C驱动的肿瘤可通过多种方式对其靶向抑制剂产生抵抗性,从而导致靶向治疗策略失效,主要包括对KRAS信号依赖性低等引起的固有耐药性,以及药物作用过程中KRAS再次突变、或旁路代谢途径的反馈性激活等引起的获得性耐药。
KRAS抑制剂针对适应症TOP10
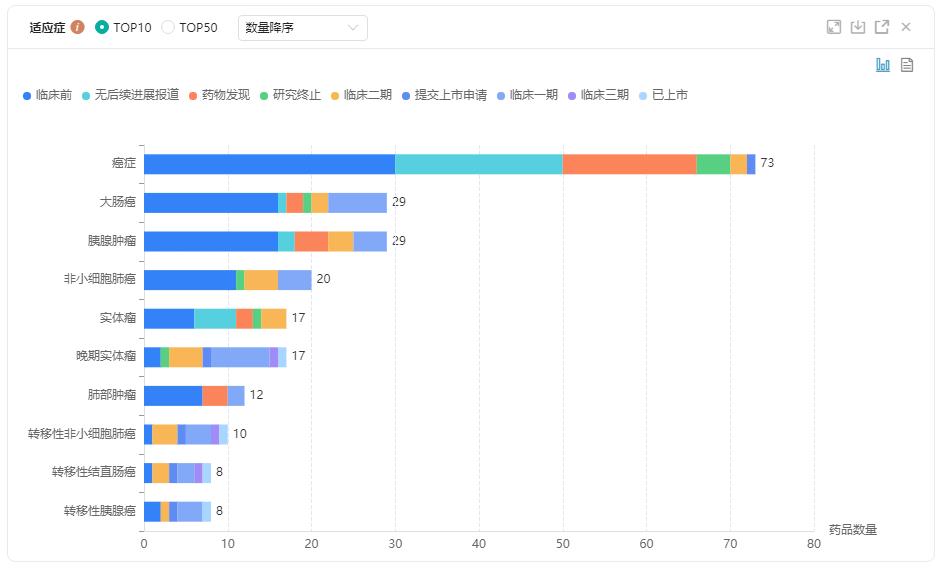
图片来源:药融云全球药物研发数据库
针对不同耐药机制,研究者正在积极探索相应的克服策略,例如共靶向下游信号传导(RAF二聚体、MEK、ERK),共靶向细胞周期检查点(CyclinD:CDK4/6),共靶向上游信号转导(RTK、SHP2),共靶向免疫检查点(PD-1),共靶向并行信号(PI3K,AKT,MTOR)等。
国内外开发KRAS抑制剂的企业大多有布局联合用药,且已取得一定进展,例如Sotorasib虽然在治疗非小细胞肺癌患者时表现出积极的疗效,但是在单药治疗结肠癌患者时的效果却并不显著,而其与EGFR单抗Vectibix(panitumumab)联用已取得积极临床结果。总体来看,联合用药为KRAS抑制剂未来重要发展方向。
4月重要资讯概览
(1)安进公布KRAS抑制剂Lumakras长期积极数据
(2)益方生物新型KRAS G12C抑制剂1期临床获积极成果
(3)治疗听力损失 BDNF疗法2a期临床结果积极
(详细内容请前往“药融云(gh_d20f87bd52d9)”公众号查看报告全文)
- 2. Claudin18.2
胃癌是目前全球因癌症导致死亡的第三大病因,也是我国第二大高发肿瘤。在我国,每年有近50万人死于胃癌,因其早期症状不明显难以诊断,确诊时多发展为中晚期胃癌。目前大多数临床治疗过程中,手术、化疗、放疗仍是胃癌的首选治疗方式。
但因为胃癌进展快和癌细胞转移快,其预后和总体生存率仍不理想。近几年,靶向治疗由于其具有定位准确、针对性强、不良反应小等特点,成为胃癌治疗的研究热门之一。其中,Claudin-18蛋白因为在胃组织细胞中独特的表达模式,成为近年来靶向治疗中研究的新型热门靶点。
Claudinl8基因定位于人的3号染色体3q22.3,由于基因中第一个外显子存在两个等位基因从而产生两种剪切突变体,可表达出N端69个不同氨基酸序列的两种蛋白亚型,分别为Claudinl8.1蛋白和Claudinl8.2蛋白。
其中Claudinl8.1蛋白特异性表达于肺上皮细胞,而Claudinl8.2蛋白在正常组织中表达高度受限,仅表达于胃的正常分化的黏膜上皮细胞中,有高度的组织特异性。Claudin18.2蛋白与胃癌的发生发展密切相关,高表达于各种胃癌组织,且在胃癌转移灶中也有相似的表达。随着研究的不断拓展,在乳腺癌、肝癌、结肠癌、头颈癌以及非小细胞肺癌等多种原发恶性肿瘤中也发现。
Claudinl8.2蛋白的异常激活和过度表达,尤其好发于消化系统恶性肿瘤,包括胃癌(70%),胰腺癌(50%),食管癌(30%)等。此外,Claudinl8.2蛋白的异常激活还可能与某些癌前病变相关,Jovov等发现,Barrett食管患者病变组织Claudinl8.2蛋白表达明显上调,且表现出与远端食管癌发生的相关性,表明Claudinl8.2蛋白表达上调可能是食管癌的早期事件。
目前Claudin18.2靶点暂无相关药物获批上市,根据药融云数据统计,截至2022.05.05,该靶点全球在研药物共有56个,其中IND以上研发阶段药物数量占比为45%,包括临床一期18个,临床二期6个,临床三期1个。
目前被批准进入临床试验的靶向 Claudin 18.2疗法主要有三类,分别为单克隆抗体、CAR-T 细胞和双特异性抗体。安斯泰来的Zolbetuximab是靶向CLDN18.2药物中研发进度最快的品种,是一种嵌合的IgG1单克隆抗体,在肿瘤细胞表面与CLDN18.2特异结合,从而引发抗体依赖性细胞毒性(ADCC)、补体依赖性细胞毒性(CDC),凋亡和抑制细胞增殖,目前该品种全球最高研发阶段为临床三期。
安斯泰来Zolbetuximab适应症研发现状

图片来源:药融云全球药物研发数据库
CT041是科济生物自主研发的一款人源化抗CLDN 18.2自体CAR-T细胞注射液,拟开发用于治疗CLDN18.2表达阳性、既往经系统治疗后出现进展或复发的晚期胃腺癌/食管胃结合部腺癌、胰腺癌等适应证。2022年ASCO大会上,CT041有2项临床研究进展报告摘要入选:一项为在美国进行的CT041治疗晚期胃癌和胰腺癌患者的多中心1b期试验;另一项为评估CT041在晚期胃癌/食管胃结合部腺癌患者中安全性、耐受性和初步疗效的1b/2期研究结果。
早在2021年ESMO大会上,科济药业就已发布其积极临床试验结果:在既往接受至少2线治疗失败、接受Ⅱ期推荐剂量(RP2D)2.5×108CT041细胞治疗的18例胃癌患者中,客观缓解率达61.1%。Claudin18.2赛道中,国内企业参与度较高,全球涉及的44家企业中,国内企业占比近80%,除科济生物以外,创胜集团、奥赛康、传奇生物等纷纷加入。
4月重要资讯概览
(1)靶向Claudin 18.2 康诺亚生物ADC疗法获FDA孤儿药资格
(2)针对胃癌康诺亚Claudin 18.2 ADC获FDA快速通道资格
(详细内容请前往“药融云(gh_d20f87bd52d9)”公众号查看报告全文)
结语:
药融云咨询团队联合药学数据分析团队开辟了《全球在研新药与靶点月报》专栏,专栏主要内容包括分析监测每月新药注册申报和药物研究进展,追踪国内医药大健康投融资与发展动向,关注国内企业创新药出海/跨国企业在华新药布局动态,解读热门/潜力靶点、疗法、适应症领域最新重大事件。
想要获取《4月全球在研新药与靶点月报》完整内容,关注公众号“药融云”(gh_d20f87bd52d9),回复“4月创新”关键词进行领取。
<END>







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论