
12月17日,据CDE官网显示,烨辉医药自主开发的BN104片拟纳入突破性治疗品种,用于治疗携带KMT2A重排和/或NPM1突变的复发/难治性急性白血病。这是国内首个纳入拟突破性疗法的口服Menin抑制剂,也是临床进展最快的国产口服Menin抑制剂。
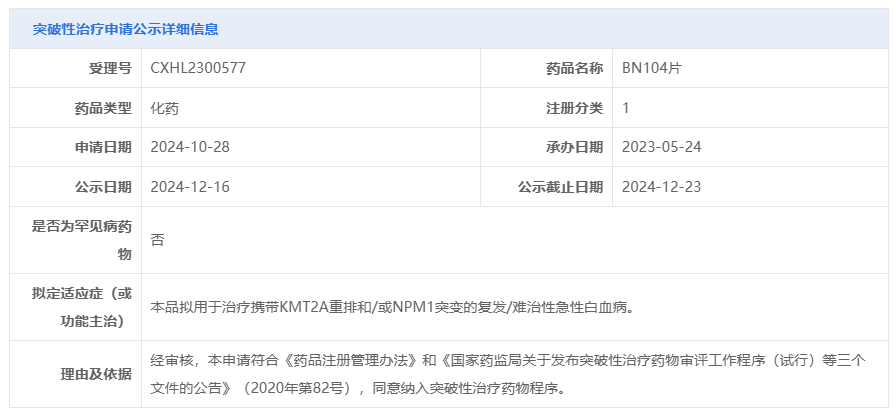
截图来源:CDE官网
据摩熵医药数据库显示,BN104是由烨辉医药自主开发的一款新型、高选择性的口服 Menin 抑制剂。临床前研究表明,与其他临床阶段的 Menin 抑制剂相比,BN104展现出更优异的疗效和明显更大的安全窗口,具备同类最佳的潜力。
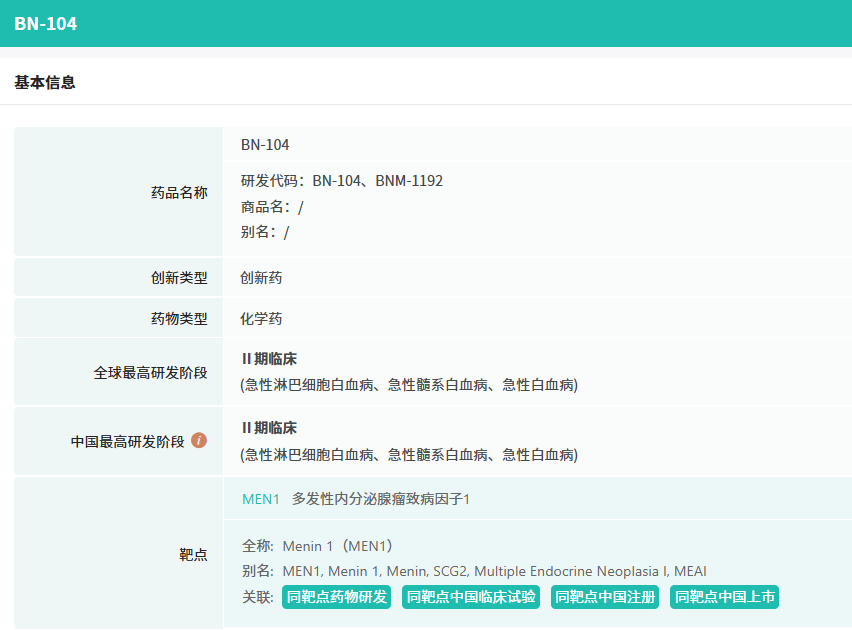
截图来源:摩熵医药全球药物研发数据库
2023年,BN104相继在中国和美国获批IND,并于2023年10月在中国完成首例患者给药。目前,BN104正在1/2期临床中评估治疗复发/难治急性白血病的疗效和安全性。本次该药拟纳入突破性治疗品种,是该产品研发进程的又一重要进展。
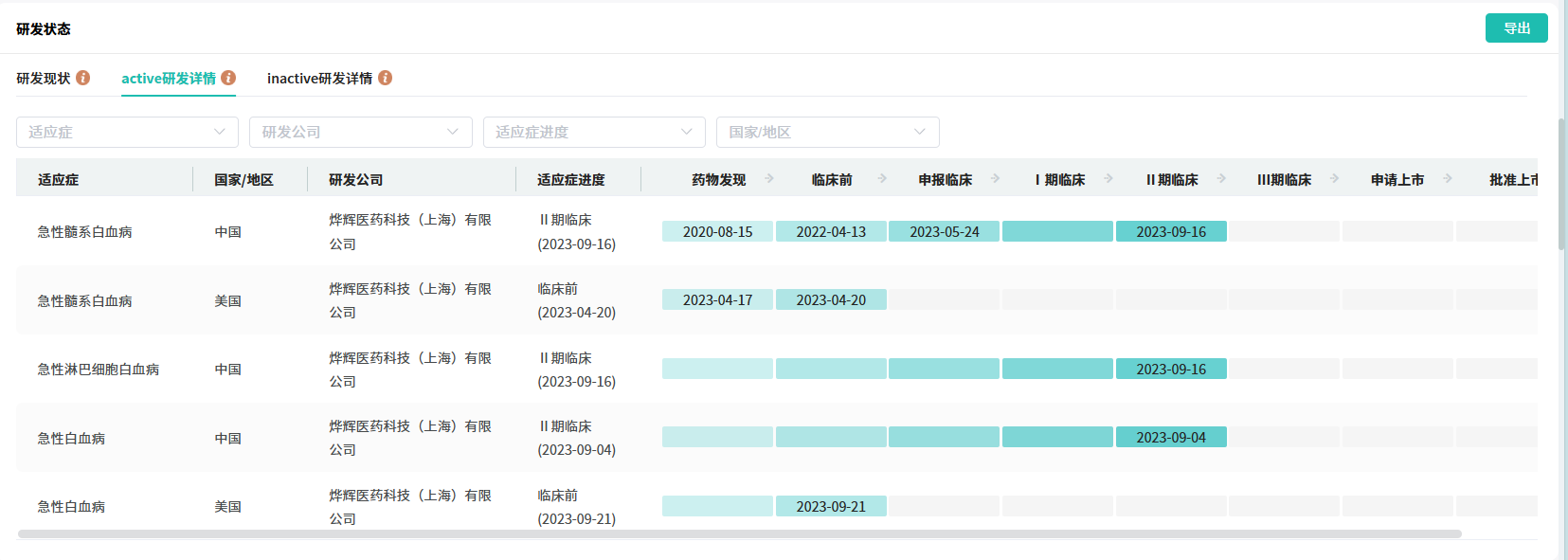
截图来源:摩熵医药全球药物研发数据库
全球共有16款口服Menin抑制剂正在研发中,其中,Revumenib已于今年11月成功获得美国FDA的上市批准,成为全球首个针对伴有KMT2A易位的复发或难治性急性白血病患者的口服Menin抑制剂。在中国,有6款口服Menin抑制剂正在研发,其中两款已进入临床阶段:烨辉医药的BN104(处于I/II期临床)以及和黄医药的HMPL-506(处于I期临床)。
参考来源:
[1] CDE官网
[2] 摩熵医药(原药融云)数据库
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论