
据CDE官网显示,10月共有5款药品(6品规)通过公示纳入优先审评品种目录,涉及5家企业,其中礼来苏州制药有限公司1个品种、锐康迪(北京)医药有限公司1个品种、长春金赛药业有限责任公司1个品种、北京浦润奥生物科技有限责任公司1个品种(2品规)和德琪(浙江)医药科技有限公司1个品种。

1.Pirtobrutinib 片
Pirtobrutinib片(吡托布鲁替尼)是礼来自主研发的 1 类创新药物、BTK抑制剂Pirtobrutinib片(吡托布鲁替尼)的上市申请拟纳入优先审评,用于既往接受过布鲁顿氏酪氨酸激酶(BTK)抑制剂治疗的复发或难治性套细胞淋巴瘤(MCL)成人患者。

Pirtobrutinib 可谓是新一代 BTK 抑制剂中的明星药。它是礼来花费 80 亿美元收购 LOXO 公司囊获的关键产品管线之一,礼来接连启动了 5 项头对头全球 III 期临床,在血液瘤上分别挑战同领域「前辈」伊布替尼、阿卡替尼和泽布替尼,以证明其 BIC 潜力。Pirtobrutinib 今年 1 月已经在美国获批上市,上半年全球销售额为 1950 万美元。
2.磷酸奥西卓司他薄膜衣片
磷酸奥西卓司他薄膜衣片(Isturisa)是Recordati集团旗下锐康迪医药新型皮质醇合成抑制剂,用于治疗成人内源性库欣综合征(CS,内源性皮质醇增多症)。Isturisa通过抑制11-β羟化酶发挥作用,抑制皮质醇过量产生,以恢复患者的皮质醇正常水平。今年8月,该新药已获批落地乐城博鳌超级医院,为中国CS患者提前带来新的治疗选择。
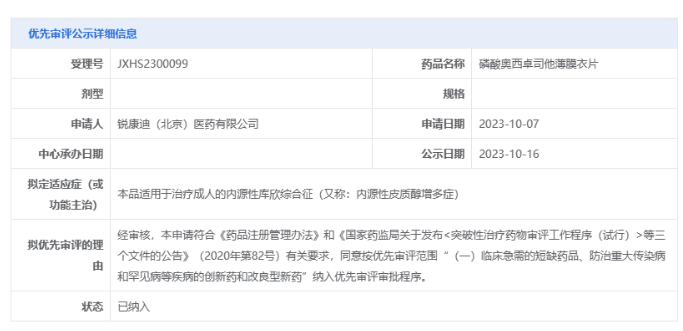
根据中国药物临床试验登记与信息公示平台,此前诺华已完成两项磷酸奥西卓司他薄膜衣片治疗库欣病的3期试验:其中一项是为期48周含头12周安慰剂对照的多中心、随机、双盲3期研究;另一项是24周单臂、开放、剂量递增后8周双盲随机撤药的3期多中心研究。此外,该产品还在开展一项开放性多中心承接研究,以评价其继续治疗的长期安全性。值得一提的是,磷酸奥西卓司他薄膜衣片已于今年8月落地乐城博鳌超级医院,为中国库欣综合征患者提前带来了治疗选择。
3.聚乙二醇重组人生长激素注射液
聚乙二醇重组人生长激素注射液(商品名:金赛增)是长春高新旗下的金赛药业研发,于2014年1月首次获批上市,是我国首个且目前唯一市场在售的长效人生长激素。据悉,该产品每周仅需注射一次,能有效避免漏针情况的同时,提高患儿的耐受度、依从性和治疗效果。

适应症为内源性生长激素缺乏所引起的儿童生长缓慢,以及特发性身材矮小(ISS)、先天性卵巢发育不全综合征(Turner综合征)所致的儿童生长障碍。金赛增是一种注射频率为每周1次的长效生长激素,于2014年1月在中国获批上市,规格为54IU/9.0mg/1.0ml/瓶,适应症为内源性生长激素缺乏所引起的儿童生长缓慢。今年1月,金赛增的适应症扩大至慢性肾脏疾病(CKD)所引起的青春期前儿童生长障碍。目前,金赛增正在开展两项III期临床试验:ELEVATE研究(GenSci004-301):一项随机、开放标签、阳性药物对照、非劣效性临床试验,旨在评估金赛增对比somatropin(商品名:诺泽,诺和诺德)在未接受过治疗的儿童生长激素缺乏症患者中的有效性和安全性。
GenSci034-301:一项随机、开放标签、安慰剂对照临床试验,旨在评估金赛增对比安慰剂在成人生长激素缺乏症(AGHD)患者中的有效性和安全性。
4.伯瑞替尼肠溶胶囊
伯瑞替尼肠溶胶囊(25mg/100mg)是北京浦润奥生物科技有限责任公司研发,伯瑞替尼是一款小分子选择性MET抑制剂。根据今年7月鞍石生物发布的新闻稿,该公司已递交脑胶质瘤新适应症的pre-NDA申请,拟用于治疗经放疗和替莫唑胺治疗后复发或不可耐受的,具有PTPRZ1-MET融合基因的IDH突变型WHO 4级星形细胞瘤或既往有较低级别病史的胶质母细胞瘤(GBM)成人患者。

伯瑞替尼是一种运用人源肿瘤移植模型(PDX),通过转化医学平台开展新药研究筛选获得的候选分子。与其它c-MET抑制剂相比,它具有高度专一(靶向)性,并能通过血脑屏障,且在不同的肿瘤模型中都表现出很好的药效。
伯瑞替尼治疗MET基因异常(PTPRZ1-MET融合和/或MET ex14跳跃)脑胶质瘤的Ⅰ期临床研究结果已于2018年发表在国际顶级期刊《CELL》杂志。该研究结果显示,PTPRZ1-MET融合阳性和/或MET ex14跳突的复发高级别脑胶质瘤患者的疾病控制率(DCR)达到 66.7%。其中继发胶质母细胞瘤的客观缓解率(ORR)为33%,中位总生存期为11.7个月,对比标准stupp方案中位生存期的6.8个月,伯瑞替尼为MET基因异常的脑胶质瘤患者带来更长的生存获益与治疗的希望。
早在2022年9月,伯瑞替尼就被CDE纳入优先审评,拟用于治疗具有METex14跳变的局部晚期或转移性非小细胞肺癌成人患者。目前其针对非小细胞肺癌适应症的上市申请目前已完成补充资料的提交,正在审评中,预计将在今年获批上市。
5.塞利尼索片
塞利尼索由Karyopharm Therapeutics公司研发,德琪药业通过引进的方式获得其中国地区的商业化权益。是全球首个全新机制的口服选择性核输出蛋白(XPO1)抑制剂,具有“全新机制、协同增效、快速起效、深度缓解”四大特点。通过抑制核输出蛋白XPO1,塞利尼索可促使肿瘤抑制蛋白和其他生长调节蛋白的核内储留和活化,并下调细胞浆内多种致癌蛋白水平。

塞利尼索发挥抗肿瘤作用机制的三条通路为:1)使抑癌蛋白在细胞核中明显聚集,再激活发挥抗肿瘤作用;2)使致癌基因mRNA滞留在细胞核,降低胞浆内致癌蛋白水平;3)激活糖皮质激素受体(GR)通路,恢复激素敏感性。
2021年12月,塞利尼索已在中国大陆获批联合地塞米松用于治疗既往接受过治疗且对至少一种蛋白酶体抑制剂,一种免疫调节剂以及一种抗CD38单克隆抗体药物难治的复发/难治性多发性骨髓瘤(R/R MM)成人患者。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论