

停止试验的决定是基于独立数据监测委员会 (DMC) 的建议,该委员会得出结论:中期数据结果符合提前停止试验以提高疗效的预设标准。
Ozempic基本信息
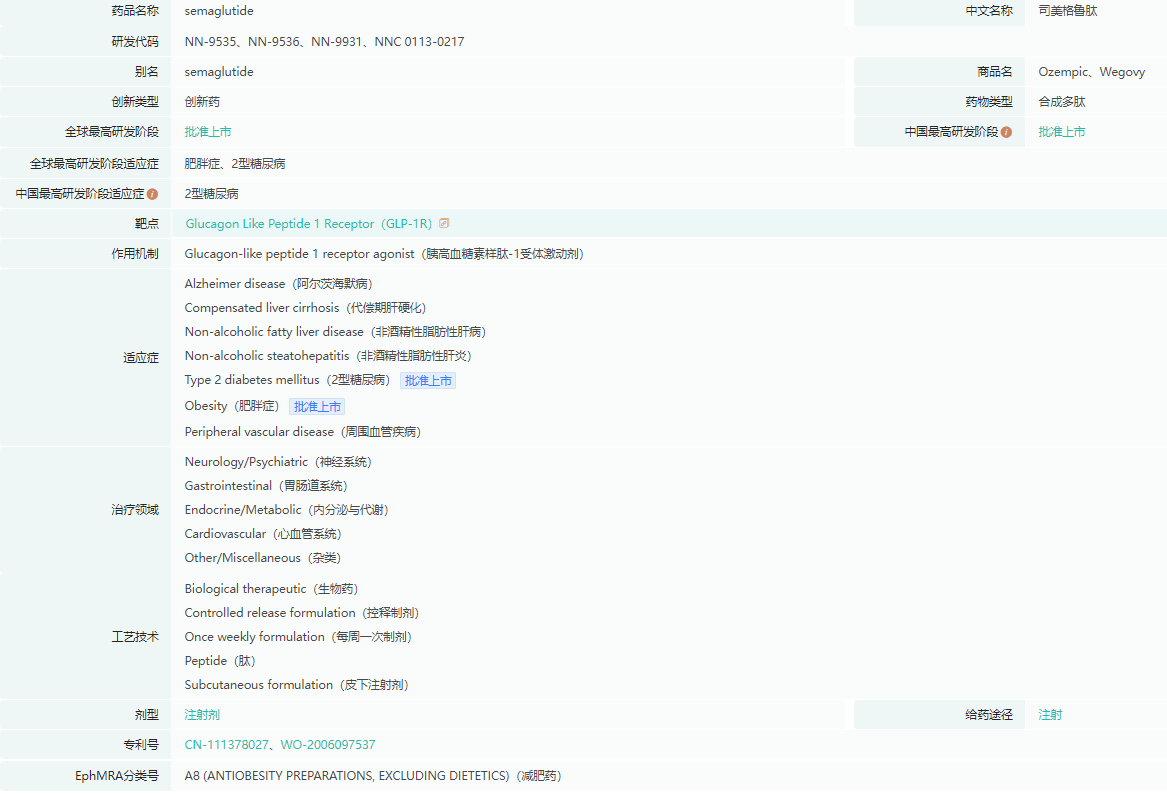
截图来源:药融云全球药物研发数据库
根据停止试验的决定,将启动试验结束程序。为了保护试验的完整性,诺和诺德在试验完成之前对结果不知情。诺和诺德预计 FLOW试验数据将于 2024 年上半年公布。
司美格鲁肽作为GLP-1药物,已用于糖尿病、减肥等领域,未来将在更多领域应用。就2023年来看,国内外各大药企争相布局GLP-1药物。国外有诺和诺德、礼来、辉瑞等制药巨头,国内有华东医药、恒瑞医药、联邦制药、派格生物、仁会生物、银诺医药、甘李药业、常山药业等多家企业布局。
2023年国内GLP-1药物研发进展情况如下:
- 7月25日,NMPA批准上海仁会生物的贝那鲁肽(BEM-014/HYBR-014)的适应症为超重/肥胖,用于成年人的体重管理。商品名为菲塑美®。
- 9月26日,据CDE官网显示,派格生物长效GLP-1受体激动剂维派那肽注射液的上市申请获得NMPA受理。
- 9月20日,华东医药通报其长效GLP-1受体激动剂司美格鲁肽注射液Ⅲ期临床试验首例受试者入组。
- 恒瑞医药管线中GLP-1类产品颇为丰富,5月5日,恒瑞医药1类新药HRS9531注射液已获批临床,用于减重。
- 9月26日,联邦制药宣布其GLP-1/GIP/GCG三重激动剂UBT251注射液或美国FDA新药临床试验批准,用于2型糖尿病、超重及肥胖。
- 9月27日,银诺医药 GLP-1 受体激动剂苏帕鲁肽上市申请获食品药品监督管理局受理。
- 9月20日,甘李药业口服版GZR18的临床试验申请获得NMPA受理。GZR18是自主研发的长效GLP-1R受体激动肽药物,目前正在进行二期临床试验。
- 9月18日,常山药业公布GLP-1药物艾本那肽III期2型糖尿病临床试验主要疗效分析结果良好。
除此之外,2023年1-9月,GLP-1相关药企也融资不断。据不完全统计,这段时间国内外共发生7起融资,融资总金额高达4.6亿美元。
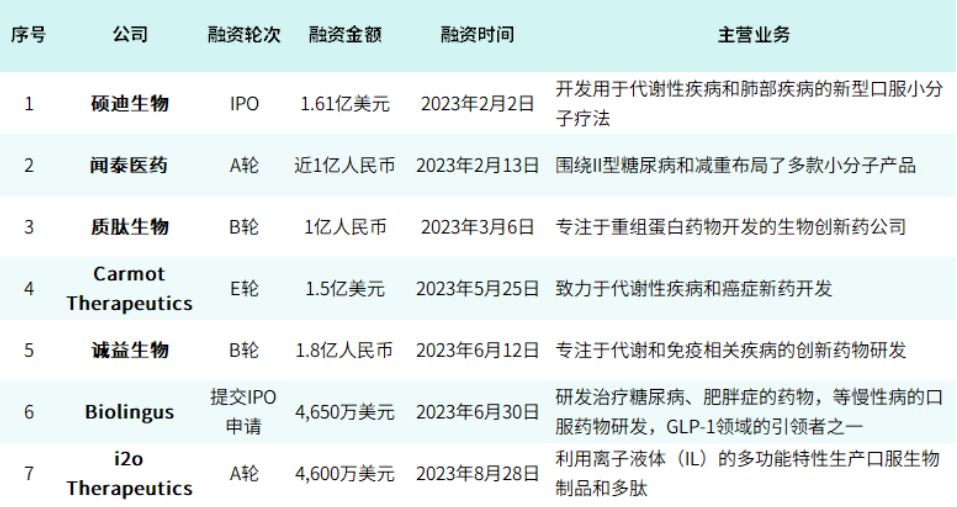
来源:生物药大时代整理
关于司美格鲁肽(商品名:Ozempic)
每周皮下注射一次的司美格鲁肽于2017年12月获得美国FDA批准,剂量分为 0.5mg、1.0mg 和 2.0mg,可作为饮食和运动的辅助药物,以改善 2 型糖尿病成人患者的血糖控制并降低患糖尿病的风险。
关于FLOW试验
FLOW 是一项随机、双盲、安慰剂对照试验,旨在对比司美格鲁肽 1.0 mg 与安慰剂预防肾功能不全的进展以及治疗肾病的疗效。该试验共有 3,534 人参加,该试验在 28 个国家的 400 多个研究地点进行。FLOW 试验于 2019 年启动。
参考资料:
1.https://www.novonordisk.com/news-and-media/news-and-ir-materials/news-details.html?id=166327
2.药融云数据库
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论