6月2日,武田宣布将于7月30日结束与Poseida Therapeutics的合作,终止开发6种体内基因疗法。
2021年10月,武田与Poseida签署了一项合作协议,开发6种肝脏导向和造血干细胞导向的体内基因疗法。作为交易的一部分,武田公司向Poseida公司支付4500万美元的预付款,Poseida公司也有资格获得超过1.25亿美元的与六个项目有关的临床前里程碑。
这次合作终止并不出人意料。武田曾在4月份宣布,计划停止AAV基因疗法的发现和临床前工作,以及罕见血液学的研究和临床前工作(相关阅读:《武田制药暂停一款AAV基因治疗药物研发,退出赛道!》)。武田的一名代表证实,合作关系终止是因为公司的管线调整。
此前,武田发布2023财报,财报显示,公司2022财年全年营收40275亿日元(约合298.33亿美元,财报里公布的固定汇率),同比增长12.8%。研发投入6333亿日元(46.91亿美元),占总营收的15.72%,净利润3170亿日元(23.48亿美元)。
Poseida Therapeutics, Inc.是一家临床阶段的生物制药公司,专注于利用其专有的下一代非病毒基因工程技术为患者创造有效的疗法。
此前,公司发布Q1财报,2023财年第一财季收入1034.30万美元,去年同期收入为143.50万美元,同比增长620.77%。
公司研发管线
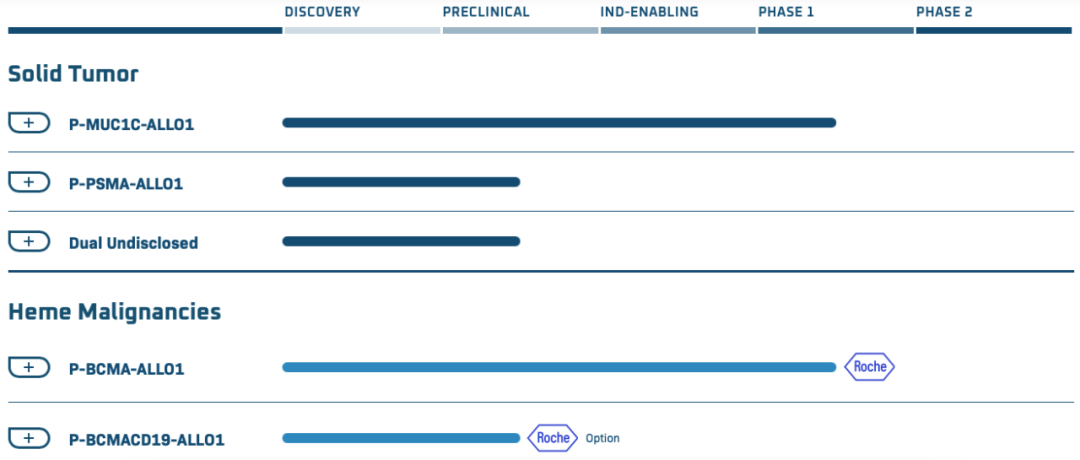
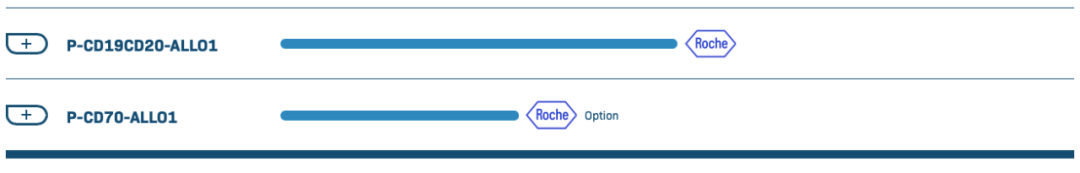

参考资料:
www.endpts.com
www.poseida.com
<END>








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论