
3月14日,在报告了严重的不良事件后,Bellicum宣布停止其管线中2款CAR-T细胞疗法的1/2期临床试验,该试验正在评估其GoCAR-T细胞候选产品联合rimiducid用于接受过治疗的癌症患者的安全性和初步疗效。在公司评估了BPX-601联合rimiducid的风险/效益后,BPX-601和BPX-603的试验都将被终止。

Bellicum研发管线 来源:官网
该公司的GoCAR-T®技术旨在增强T细胞增殖和功能持久性,重新激发宿主免疫,并抑制肿瘤微环境,以克服传统细胞疗法治疗实体瘤的局限性。
BPX-601与BPX-601都是公司在研的CAR-T细胞疗法(嵌合抗原受体T细胞疗法),BPX-601是Bellicum打造的一款靶向前列腺干细胞抗原(PSCA)的自体GoCAR-T候选产品,而BPX-603是靶向HER2的GoCAR-T疗法,治疗HER2阳性实体瘤。
截图来源:药融云全球药物研发数据库
而最近在转移性去势抵抗性前列腺癌(mCRPC)1/2期试验中,接受BPX-601治疗的患者发生了严重的副作用,包括4级细胞因子释放综合征(CRS),这是在剂量递增队列观察到第2例剂量限制性毒性事件。
受此影响,Bellicum周三股价下跌50%。
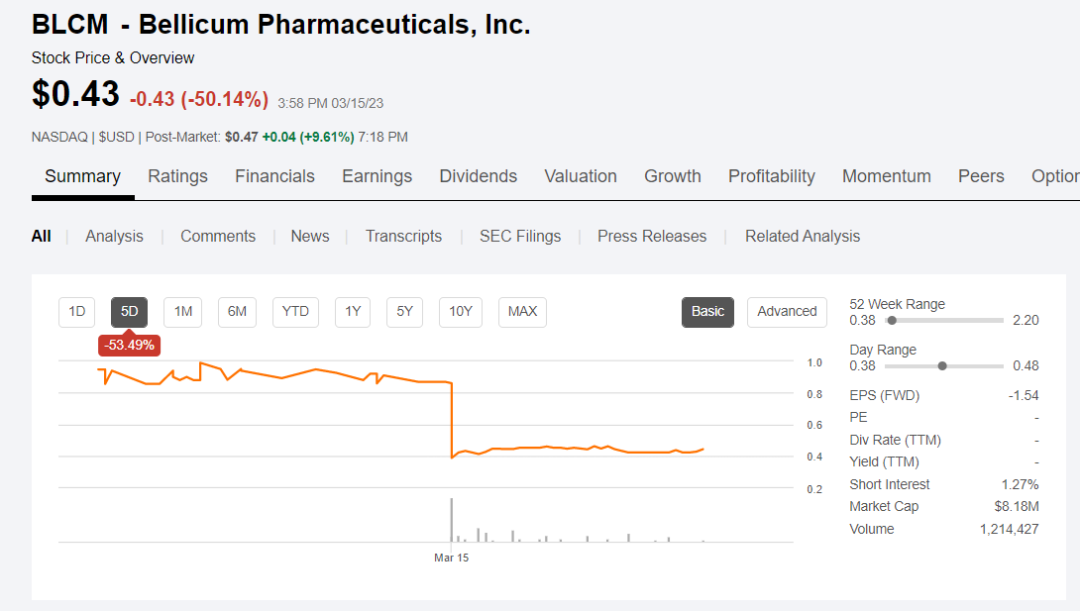
对于Bellicum来说,其CAR-T细胞疗法BPX-601的研发之路漫长且曲折。
2020年,在报告BPX-601治疗胰腺癌令人失望的结果后,Bellicum宣布裁员79%,停止研发新产品,集中精力开发BPX-601和BPX-603。

Bellicum总裁兼首席执行官Rick Fair
今年2月份,虽然报导了一些不良事件,例如骨髓抑制3级细胞因子释放综合征和4级免疫效应细胞相关神经毒性综合征。但是Bellicum总裁兼首席执行官Rick Fair仍表示BPX-601的早期数据“令人鼓舞”并充满希望。然而经过了短短一个月,BPX-601临床试验就遭遇停止。仅有的2款研发产品遭遇如此沉重打击,看来Bellicum又要重新调整公司发展战略了。
CAR-T细胞疗法是近年来晚期肿瘤疗法的一个重要突破,但目前仅限于血液肿瘤,对于实体瘤的治疗结果往往不尽如人意,且常伴随毒性。目前国内外药企都希望CAR-T细胞疗法能在实体瘤领域取得新突破,让我们拭目以待。
截图来源:药融云投融资数据库
Bellicum制药公司于2004年7月在特拉华州成立,是一家临床阶段的生物制药公司,专注于针对各种癌症,包括血液癌症与固体肿瘤,以及孤儿遗传性血液病发现和培养新的细胞免疫疗法。公司正在开发一些细胞免疫治疗的最重要的领域的新一代产品候选,包括造血干细胞移植(HSCT)或CAR-T细胞疗法和树突状细胞疫苗。
据药融云投融资数据库显示,截至目前,Bellicum最高已完成至IPO后其他轮次融资,总融资金额近4亿美元。丰厚的资金是底气,将会助力Bellicum的药物研发。
Bellicum融资信息
截图来源:药融云投融资数据库
参考资料:
[1] Bellicum官网
[2] 药融云数据库
想要解锁更多药企信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发情况、年度报告、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论