
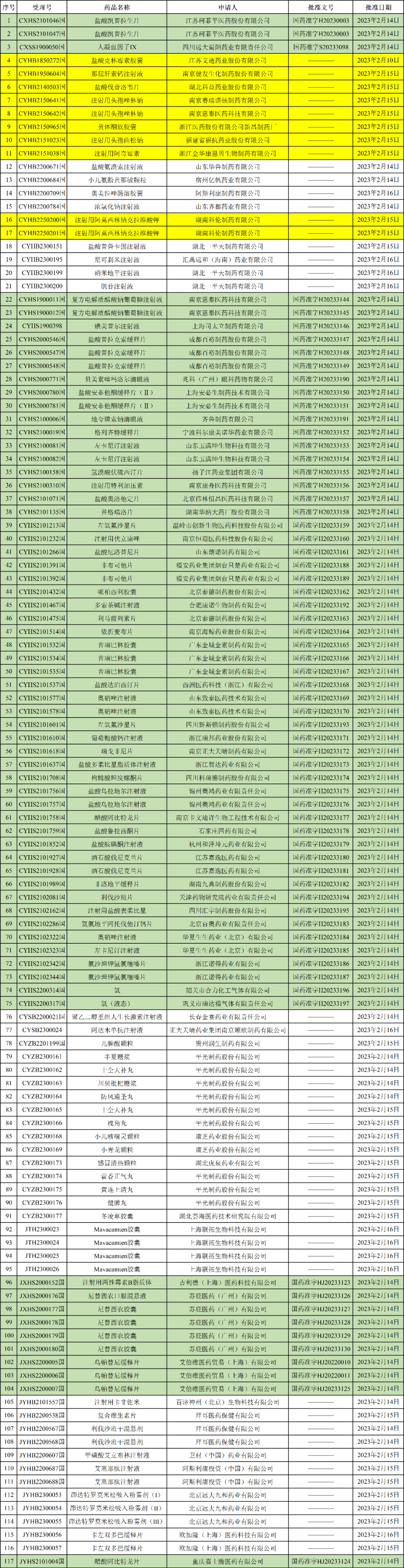
NMPA发布2023年02月20日药品批准证明文件送达信息,本批次共有117个受理号获批,其中10个为一致性评价受理号获批,包括:
- 湖北科益药业股份有限公司,盐酸伐昔洛韦片(首家过评)
- 浙江医药股份有限公司新昌制药厂,黄体酮软胶囊
- 浙江金华康恩贝生物制药有限公司,注射用阿奇霉素
- 湖南科伦制药有限公司,2品规注射用阿莫西林钠克拉维酸钾
- 等
- 成都百裕制药股份有限公司,3品规盐酸普拉克索缓释片(视同过评,首家)
- 扬子江药业集团有限公司,氢溴酸伏硫西汀片
- 南京正大天晴制药有限公司,瑞戈非尼片(第二家过评,首家为扬子江药业)
- 湖南九典制药股份有限公司,非洛地平缓释片
- 等
此外,苏柯菲平医药股份有限公司的1类创新药盐酸凯普拉生片获批上市,用于十二指肠溃疡和反流性食管炎的治疗。
苏庇医药申报的尼替西农原研药在中国获批上市。尼替西农由Swedish Orphan Biovitrum AB(SOBI)公司开发,该药本次获批了口服混悬液和胶囊两个剂型,用于治疗成人和儿科患者的1型遗传性酪氨酸血症。
2023年02月20日药品批准证明文件送达信息
<END>







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论