
近日,康诺亚生物开展并公示了TSLP单抗——CM326注射液的II期临床试验(登记号:CTR20222170),适应症为中重度特应性皮炎。此前的I期临床试验结果数据显示,CM326注射液组的总体安全性、耐受性特征和安慰剂组相当。康诺亚是继正大天晴之后,国产第2家TSLP单抗进入II期临床试验的企业。
CM326注射液临床试验信息
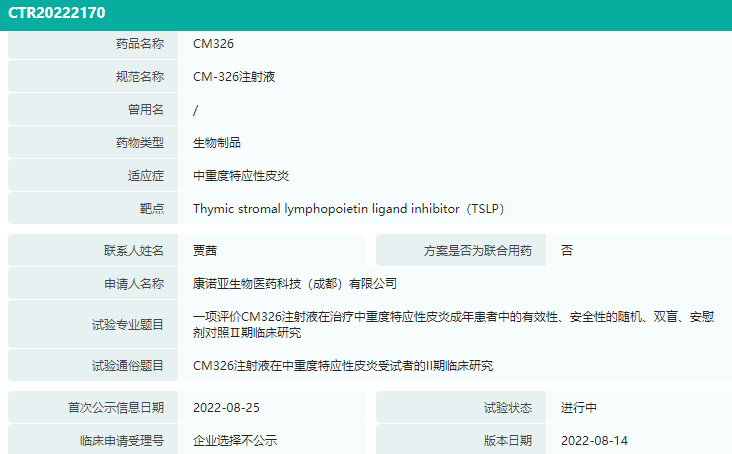
截图来源:药融云中国临床试验数据库
特应性皮炎(Atopic dermatitis, AD)是一种常见的慢性过敏性皮肤病,目前针对AD治疗仍以外用糖皮质激素、钙调神经磷酸酶抑制剂为主,而长期外用激素常出现各种副作用,钙调神经磷酸酶抑制剂也可出现一定不良反应,且对中重度特应性皮炎疗效不佳,因此存在大量未被满足的临床需求。
据公开资料,CM326是由康诺亚研发、具有全新作用机制和全球自主知识产权的1类创新药,靶向胸腺基质淋巴细胞生成素(TSLP)。TSLP是炎症级联反应的启动因子之一,与特应性皮炎、哮喘、慢性鼻窦炎等过敏性疾病的发生密切相关,是目前唯一被证明对低Th2型哮喘有效的靶点。
在TSLP单抗药物中,安进/阿斯利康的tezepelumab全球进度最快,已于2021年底获批在美国上市,作为附加维持疗法,治疗12岁以上儿童和成人严重哮喘患者;在中国也已进入III期临床试验阶段。
tezepelumab中国临床试验情况
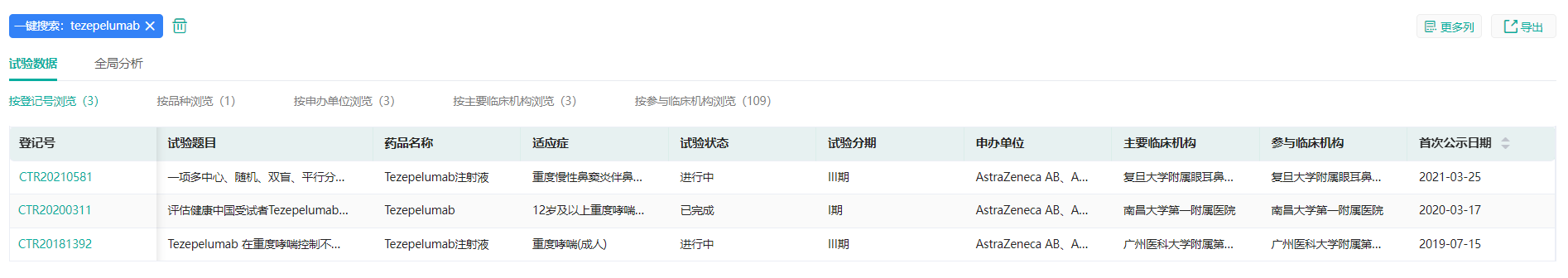
截图来源:药融云中国临床试验数据库
正大天晴、康诺亚生物的TSLP单抗进度也领先于其他企业,TQC-2731和CM326均已进入II期临床试验阶段,对应适应症分别为哮喘和中重度特应性皮炎。其次就是江苏荃信生物的QX-008-N和博奥信生物的BSI-045B,均处于I期临床阶段。启愈生物、上海恒瑞、四川科伦博泰等本土药企也有TSLP单抗在布局开展,尚处于临床前或药物发现阶段。
除了中重度特应性皮炎外,康诺亚还对CM326开展了适应症为慢性鼻窦炎伴有鼻息肉、中重度哮喘的临床试验,进度最高分别为Ib/IIa期和I期临床试验阶段。
CM326已公示的中国临床试验
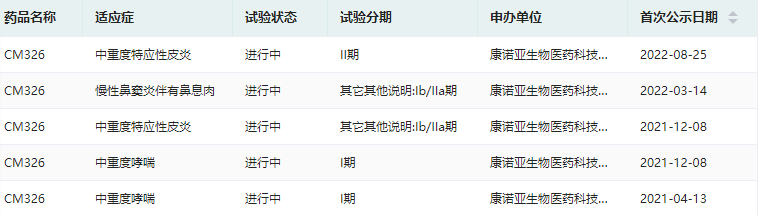
截图来源:药融云中国临床试验数据库
2021年11月22日,康诺亚与石药就CM326在中重度哮喘和慢性阻塞性肺病等呼吸系统疾病独家授权开发及商业化正式签订协议。
根据协议,康诺亚将授予石药CM326的独家许可,在中国(不包括香港、澳门及台湾地区,以下简称“该地区”)进行该产品于该领域开发与商业化,并成为上市许可持有人。康诺亚将获得石药支付的人民币1亿元首付款及根据开发进度支付的最高人民币1亿元开发里程碑付款。未来康诺亚将根据该产品于该地区达成的销售额获得销售里程碑付款和销售提成。
想要解锁更多药企创新药临床试验信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、临床试验情况、研发阶段、最新进展、申报获批情况、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

—END—








































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论