
一、深度概述
近日,据Madrigal Pharmaceuticals公司宣布,美国FDA加速批准了Rezdiffra(resmetirom)药品。据新闻稿报道,这款药物是首个获得FDA批准的NASH疗法,代表着该领域发展的一座重要里程碑。

药融资咨询团队深入剖析了NAFLD/NASH的治疗领域市场和研发格局。全面分析了全球及中国在NASH治疗领域的药物市场格局与新药研发趋势,并紧密追踪了在研的重点产品及临床试验的最新进展。通过本报告,读者将能够全面把握NAFLD/NASH行业的发展动态、市场现状以及研发格局。
二、NAFLD/NASH概览及背景介绍
NAFLD是一种严重的慢性肝脏疾病,NASH是NAFLD的严重类型。NAFLD是严重的慢性肝脏疾病,其中NASH为其严重类型。NAFLD与胰岛素抵抗和遗传易感密切相关,可导致单纯性肝脂肪变、NASH,进而可能发展为肝硬化和肝癌。2020年,国际专家提出用代谢性相关脂肪肝病(MAFLD)替代NAFLD,只要患者存在脂肪肝并伴随超重/肥胖、2型糖尿病或代谢功能障碍等任一条件,即可诊断为MAFLD。

全球NAFLD患病率预计为25%-30%,因地区、诊断和种族差异而异。中东地区患病率最高(32%),亚洲地区紧随其后(27%),已超过北美(24%)和欧洲(24%)。在亚洲,东南亚NAFLD患病率最高(42%),印度尼西亚更是高达51%,而日本最低(22%)。中国患病率29.8%,处于亚洲中等水平。NASH患病率因诊断与地区而异,预期2030年中国患者数量将大幅上升。
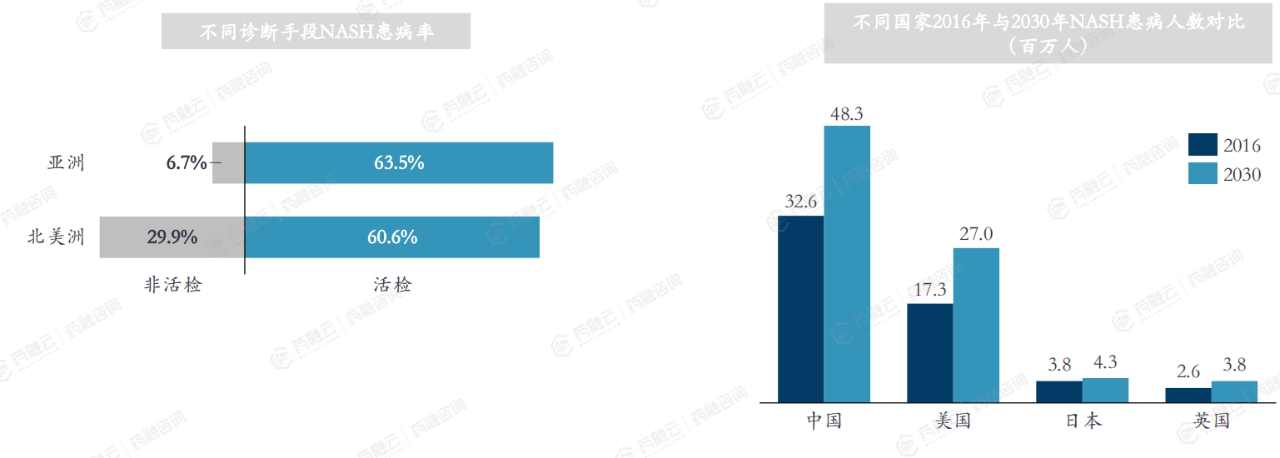
自先前的前瞻性患病率研究发表以来,临床显著纤维化(2期或更高阶段纤维化)的患病率增加了>2倍。预计到2030年,晚期肝纤维化(定义为桥接纤维化(F3)或代偿性肝硬化(F4))患者将不成比例地增加。预计到2030年与NASH肝硬化相关的肝失代偿、HCC和死亡的发生率预计也将增加2- 3倍。

NAFLD的进展为肝炎、肝纤维化,最终发展为肝硬化甚至肝细胞癌。肝纤维化程度按弹性数值分为F0、F1、F2、F3和F4五个等级。

NAFLD和NASH患者多合并有二型糖尿病和肥胖等代谢类疾病。NAFLD/NASH和肥胖、2型糖尿病、高血脂,高甘油三酯、和高血压以及Mets类疾病密切相关。尤其是在NASH人群中,有高达81.8%的人群肥胖,NASH糖尿病患者的比例是NAFLD的大约一倍。
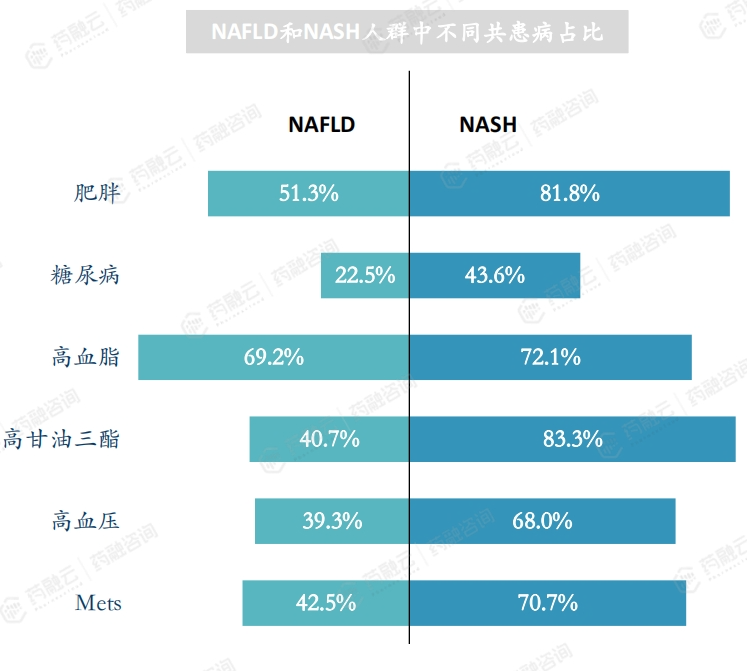
全球约55.5%的T2DM人群合并患有NAFLD,其中欧洲最高,达68.0%。

三、全球及中国药物市场格局
PPARα/PPARγ双重激动剂-Saroglitazar 2020年在印度获批。 Saroglitazar是2020年3月印度药企Zydus-Cadila Group在印度获批上市非脂肪型肝炎适应症的一款药物。此药目前在印度已获批了包括非酒精性脂肪肝病和非酒精性脂肪肝炎在内的共计5个适应症。

但目前该药物未在美国,欧盟和日本等国家地区获批。是一款PPARα/PPARγ的双重激动剂,属于过氧化物酶体增殖物活化受体(PPAR)家族的两名成员,该靶点与脂肪代谢、氧化应激作用有关,已经多款用于治疗代谢性疾病的药物上市。

万众瞩目的“first-in-class” NASH治疗药物 Resmetirom 2024年3月获FDA批准上市。

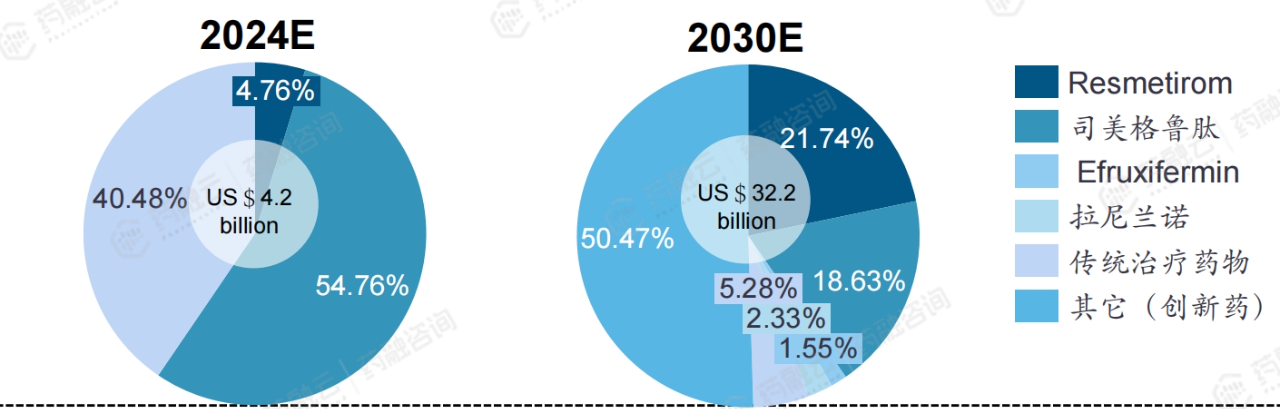
预计全球和中国NAFLD/NASH市场将持续增长,至2030年国内市场将达到355亿人民币。全球目前没有药物可直接治疗 NAFLD/NASH,许多公司已加速布局这一领域。全球NASH 市场从 2016 年的 17 亿美元增至 2020 年的 19 亿美元,复合年增长率为 3.2%。预计未来会呈现快速增长的趋势,到 2025 年将达到 107 亿美元,并于 2030 年达到 322 亿美元,期间复合年增长率为 41.8%和 24.6% 。

NASH 药物市场从 2016 年的 5亿人民币增至 2020 年的 7 亿人民币,复合年增长率为 5.5%。未来随着创新药走向大众化,会呈现明显的增长,到 2025 年预计将达到 32 亿人民币,并于 2030 年达到 355 亿人民币,期间复合年增长率为 37.0%和 61.4% 。

市场关键驱动因素:在肥胖、糖尿病等疾病因素的作用下, 患病人数持续上升。

市场关键驱动因素:新药不断获批上市,非侵入诊断方式推动药物开发。预计未来10-15年内,将有10余种NASH药物获批。进展最快的THR-β激动剂Resmetirom2024年3月14日获FDA加速批准上市。FGF21 类似物 Efruxifermin 改善NASH患者肝脏纤维化水平为对照组2倍,并且显著改善NAS评分,具有同类最优(Best-in-class)潜力,FDA已授予其突破性疗法资格认定(临床Ⅱ期)。目前Efruxifermin 已进入III期临床。正大天晴引进的 PPAR 激动剂拉尼兰诺为首个同时能改善纤维化和炎症的口服 NASH 新药,美国FDA已授予该药用于NASH的突破性疗法认定和快速通道资格(临床Ⅲ期)。

四、全球及中国药物研发格局
抗NAFLD/NASH药物可以分为调节代谢、抗纤维化和抗炎三类机制。根据靶点作用机制不同,可以将NASH研发的主流靶点分为3类:代谢类、抗纤维化类和抗炎类,代谢类靶点是目前研究最多也是临床进展最快的靶点。

目前NAFLD/NASH领域全球有百余个靶点正在研发,但成熟靶点相对较少。
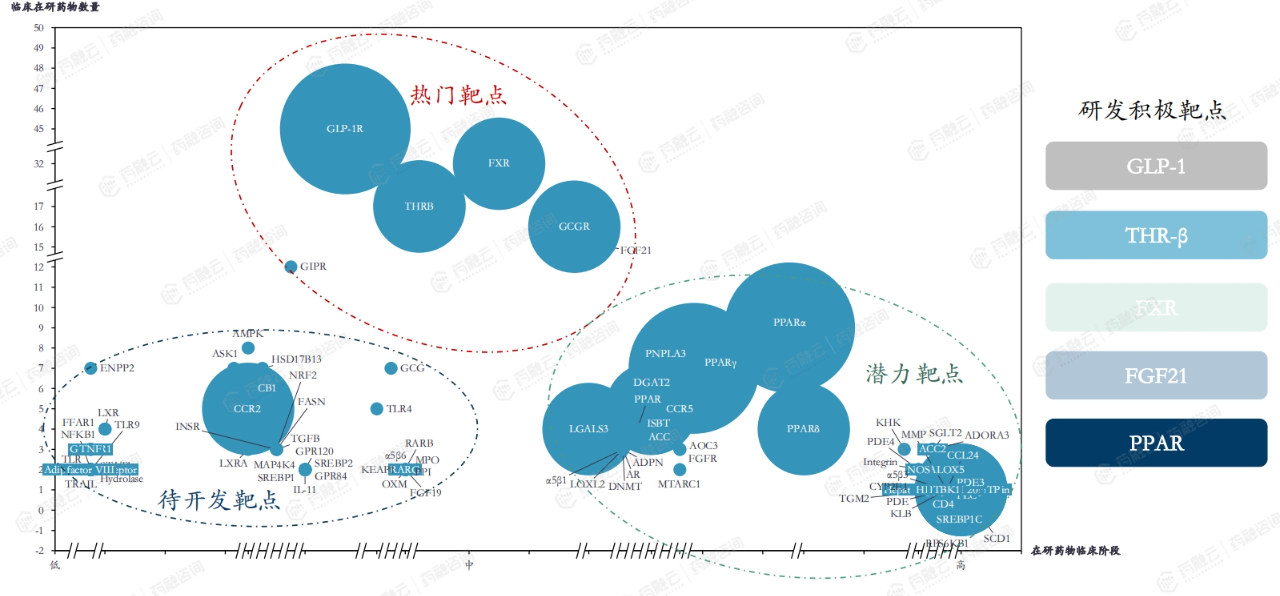
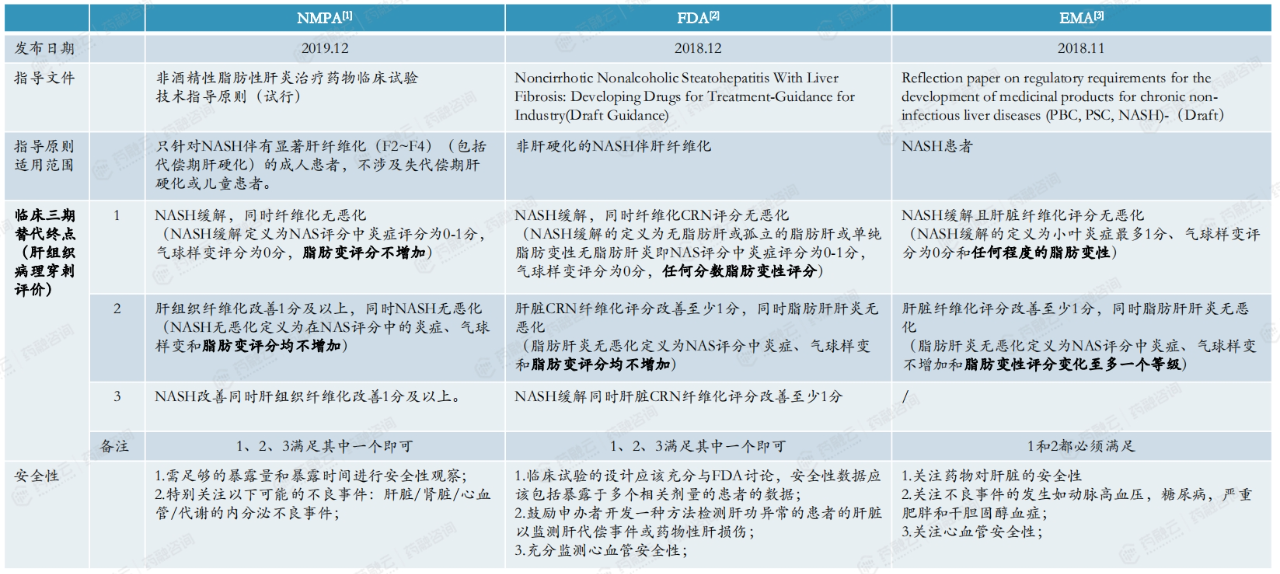
NMPA、FDA和EMA都规定NASH晚期确证性临床试验须使用肝组织活检进行疗效确证。
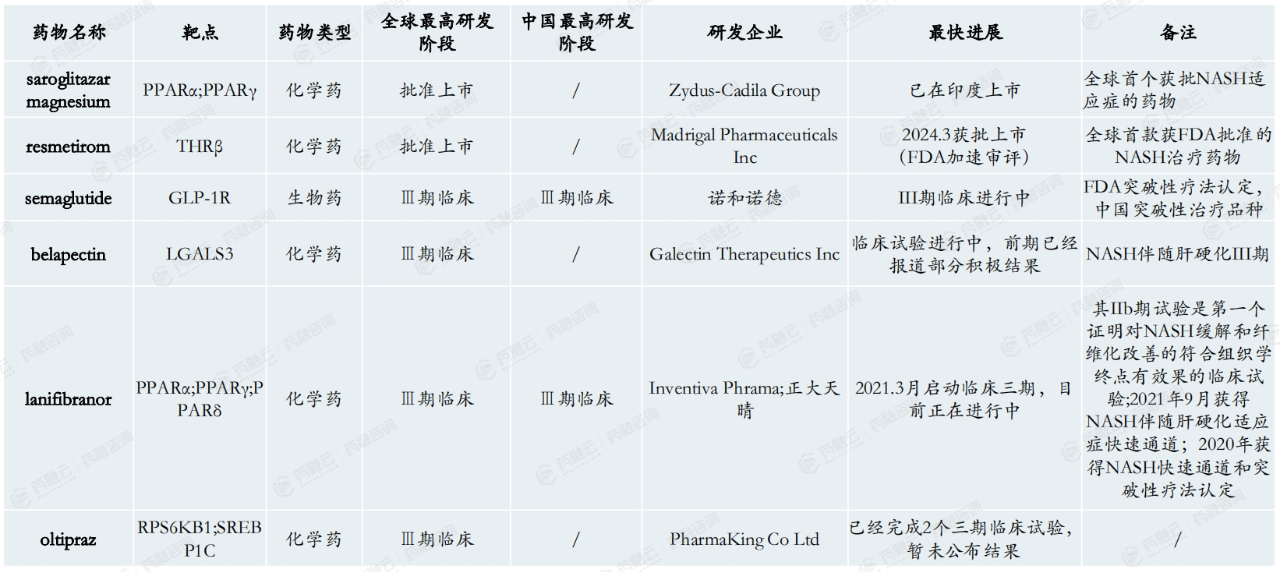
全球共有不到10个药物进入临床三期试验且目前进展积极。
中国多个药企布局NAFLD/NASH,整体开发进度落后于全球-1。

中国多个药企布局NAFLD/NASH,整体开发进度落后于全球-2。

五、重点产品临床试验追踪
THR-β-专注于NASH疾病的脂代谢靶点。甲状腺激素通过激活肝细胞中的β受体,在肝功能中起着核心作用,影响从血清胆固醇和甘油三酯水平到肝脏中脂肪的病理性堆积等一系列健康参数。THR-β作用是正常肝功能的关键,包括调节线粒体活性,如肝脏脂肪分解和控制正常、健康的线粒体水平。NASH患者肝脏中的THR-β受体活性水平降低。


GLP-1R优秀的降糖减重效果也成为NASH的热门靶点。

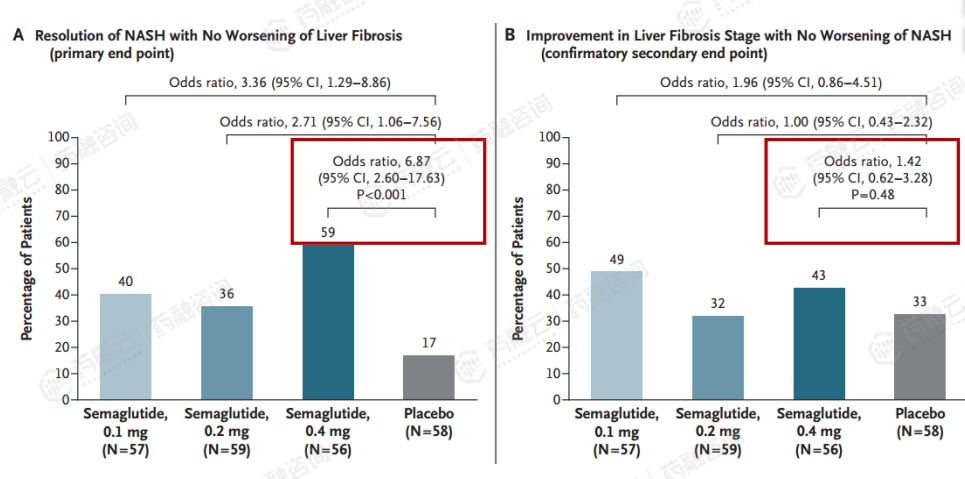
NASH有望成为司美格鲁肽继二型糖尿病,减重后的第三个适应症。semaglutide是诺和诺德开发的一款靶向GLP-1R的新型长效胰高糖素样肽-1(GLP-1)类似物药物,其注射液和口服制剂已经获批用于治疗二型糖尿病和肥胖。研究发现GLP-1与肝脏细胞受体结合后能降低肝脏脂肪变性等疗效而拓展GLP-1类药物在治疗NASH中的应用。目前semaglutide正在进行三期临床试验中。
PPAR靶点研发进度靠前,目前已有药物获批上市。

Lanifibranor-NASH疾病领域进度最为领先的pan-PPAR抑制剂药物。Lanifibranor是Inventiva SA公司研发的一款口服pan-PPAR小分子抑制剂。Lanifibranor在2b期完成后,正在进行一项NASH适应症III期临床研究。

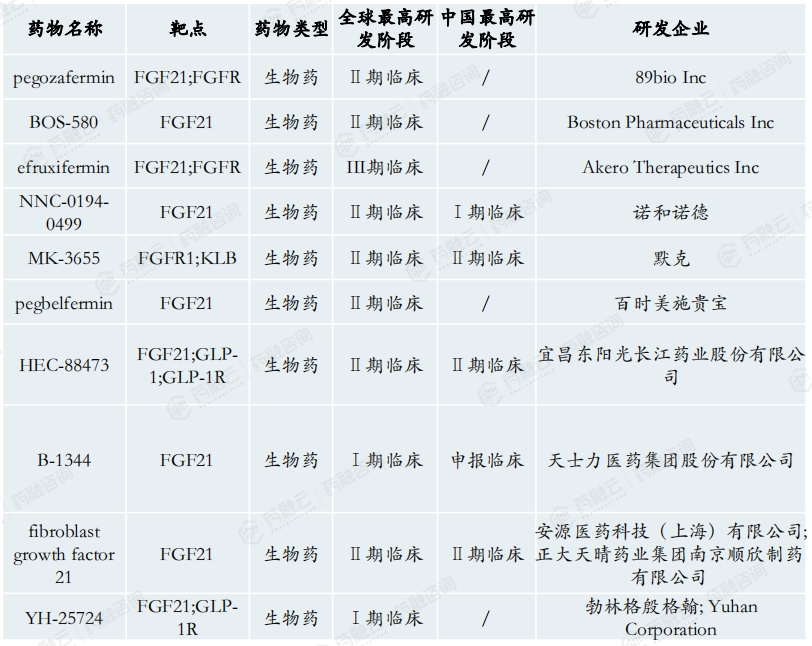
FGF21在NASH研发火热,多个药物临床II期达到终点。

Efruxifermin潜力巨大,IIb期临床结果疗效优于对照两倍。Efruxifermin是Akero Therapeutics公司开发的一款长效FGF21-Fc融合蛋白,通过模拟成纤维细胞生长因子FGF21的生物活性作用于FGF21受体,在肝脏和脂肪组织中传递持续的和平衡的信号来调节代谢。
具有3-4天的半衰期,可实现每周一次皮下注射。目前Efruxifermin已经完成两项临床IIb临床研究,正在进行一项为期36周的NASH伴肝硬化的临床IIb临床研究,另外两项III期临床研究也预计在2023年下半年启动。

Pegozafermin超长半衰期,处于FGF21靶点研发前列。

尽管奥贝胆酸被拒,FXR仍是NASH的热门研发靶点之一。
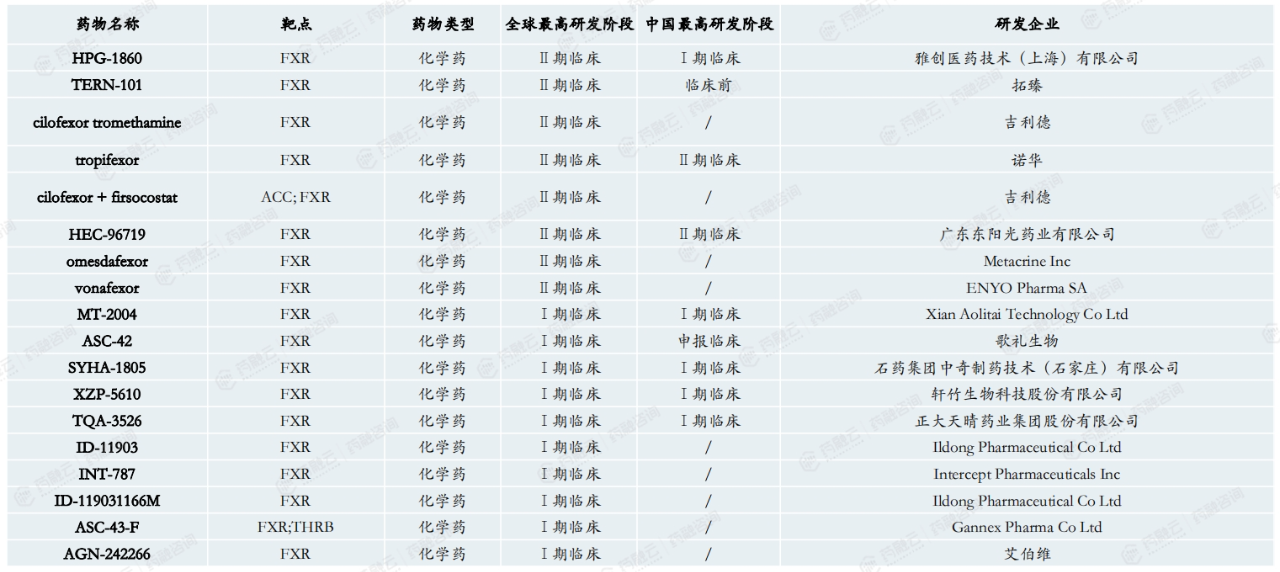
表-热门靶点进展积极药物临床有效性对比

小结:
NAFLD/NASH是一种复杂的,由多种致病因素导致的严重的慢性肝脏疾病,和二型糖尿病和肥胖密切相关,患病率近年来呈不断上涨的趋势;当前NAFLD/NASH患病人口巨大,且需要长期用药,目前全球只有一款药物专门用于治疗NASH,存在巨大的未满足的临床需求。全球有百余个靶点和企业进行研药物研发,随着Madrigal Pharmaceuticals Inc口服小分子药物Resmetirom已经获FDA加速审评批准上市,研发热度会更高。
前往药融云公众号后台回复「NAFLD/NASH」,可获取完整《NAFLD/NASH治疗领域市场和研发格局分析报告》PDF版。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!







































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论