
2023年10月27日,NMPA发布药品批准文件送达文件,奥希替尼首仿——江苏万邦生化医药,获得批准文号。
仿制获得注册证号,就能直接上市销售么?
摆在仿制面前的第一道也是核心关卡,中国该产品的原研化合物专利,2032-07-25到期。也就意味着,如果仿制想要合法上市销售,需要等待近九年。
本文通过梳理原研在中国的化合物专利、中国竞品情况、美国仿制的申报及专利挑战情况,以及分析中国原研核心专利的壁垒,以期为行业提供一些思考。
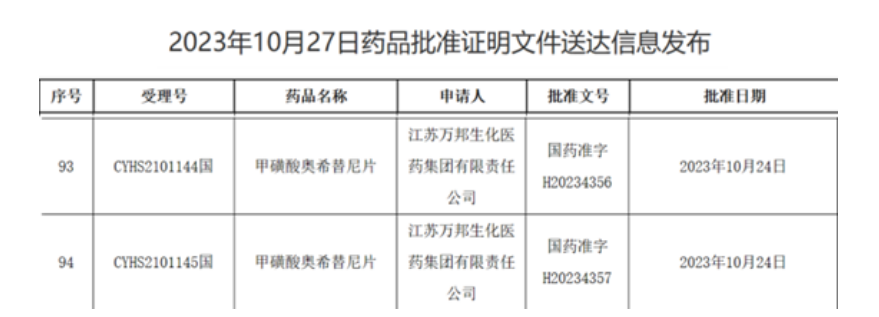
截图来源:NMPA
1.1原研在中国核心化合物专利情况
原研阿斯利康,在中国拥有多项核心专利,核心化合物到期届满日在2032-07-25。
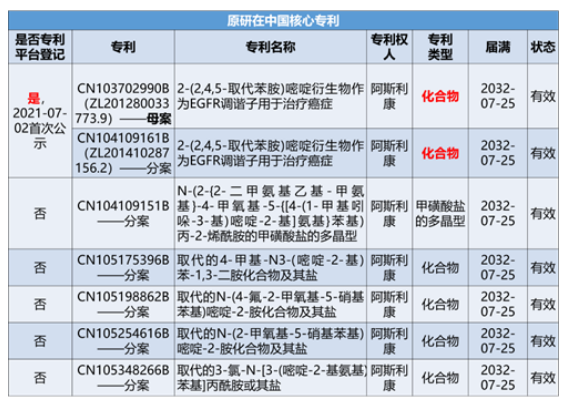
参考来源:中国上市药品专利信息登记平台、欧专局、国家知识产权局
1.2中国竞品
经查看CDE及中国临床登记平台,奥希替尼,截止2023-10-27,仅有1家BE和上市申请且获批上市的厂家,正是今日首仿获批上市的江苏万邦生化医药。
值得注意的是,中国上市药品专利信息登记平台是2021年7月才开始启用,而江苏万邦生化医药的上市提交早于2021年7月,故此截止目前,平台上暂未收录任何厂家的专利声明。
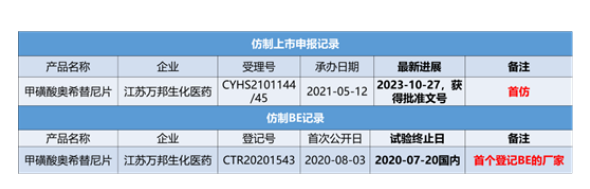
参考来源:CDE、NMPA、中国临床登记排平台
1.3美国竞品及专利挑战情况
在美国,截止2023年10月,已有2家公司获得暂时批准。从美国仿制厂家的策略可知,中国的万邦生化医药不是孤舟,美国的MSN和ZYDUS亦选择提前10年的时间进行注册申报。
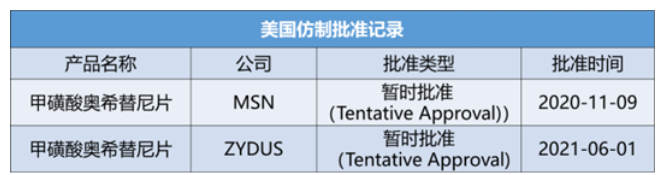
参考来源:FDA
1.4美国核心专利及专利挑战情况
1.4.1美国核心专利
奥希替尼,美国OB登记原研2项化合物及1项组合物专利,其中核心化合物专利US8946235B2于2032-08-08到期。经查看,该专利涉及PTA,延长14天。
PTA简介:专利权期限调整制度(PTA),用于补偿因专利授权审查流程导致的延误时间,美国专利期限调整计算方式可表示为PTA=A类延误+B类延误+C类延误-三类延误重叠时间-因申请人原因延误的天数。
每一类别的具体解释如下:A类延误是指USPTO未在规定期限内发出相应的通知书或做出回应。B类延误是指USPTO未在专利申请实际提交日起 3 年内颁发专利做出授权决定。C类延误是指因派生诉讼、保密令或上诉程序且经审查推翻了对可专利性的不利决定的裁决而授予专利。
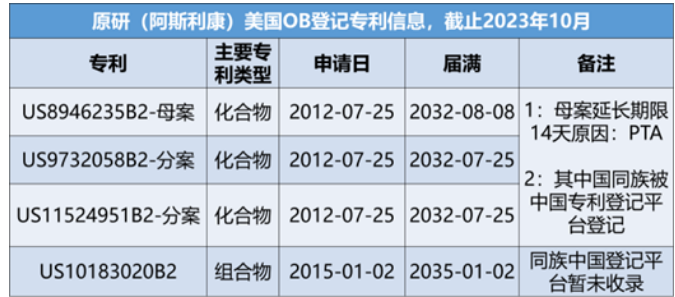
参考来源:药融云美国橙皮书数据库
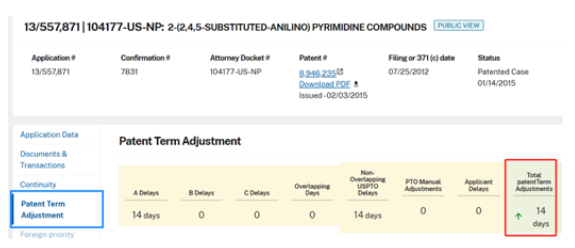
参考来源:美国商标局官网
1.4.2美国专利挑战情况
经检索,截止2023-10月,暂无任何仿制企业对化合物专利进行挑战。经查看,FDA在Zydus的tentative approval letter中提到,Zydus对两个登记的化合物专利进行了III类声明,但对组合物专利US10183020B2进行了IV类专利挑战声明。类似地,截止2023-10月,已有多家仿制在美国对组合物专利US10183020B2提出PIV挑战,包括MSN Group、Zydus Group和Alembic Pharmaceuticals Limited。

参考来源:FDA,Zydus的tentative approval letter
1.5距离专利到期近10年,仿制的上市策略,留给仿制企业不少思考
在中国,于奥希替尼项目上,目前可知首仿江苏万邦生化医药一骑绝尘,在明知化合物专利2032年到期前提下,2023年首仿获得注册证号,暂无后来者追逐。
在美国,已有2家仿制暂时批准,在明知化合物专利2032年到期前提下,2家仿制分别于2020年及2021年获得批准,且2家企业亦未提出化合物专利挑战。
专利到期前抢仿市场规模庞大的重磅炸弹药物是常见现象,而且立项确实宜早不宜迟,但是提前近10年时间,对于仿制企业,我们不经思考,原研的核心专利壁垒有多高?仿制药的申报策略是什么?
原研的核心专利壁垒
首先,原研阿斯利康,在中国拥有7项授权核心专利,到期届满日均在2032-07-25。也就是说,作为仿制厂家,如果想要突破,成就2032年之前上市销售,必须至少同时跨越这7项专利。
其次,我们不经思考,这7项专利的内在关系,显而易见的是,这是母案与一系列分案的关系。
再者,我们需要仔细分析,这几项专利与奥希替尼上市产品的关系,是否均是其上市销售的障碍。
第一项专利,CN103702990 B,中国专利平台登记,类型是化合物。经查看奥希替尼说明书和该专利要求保护的范围,奥希替尼落入该专利的保护范围。
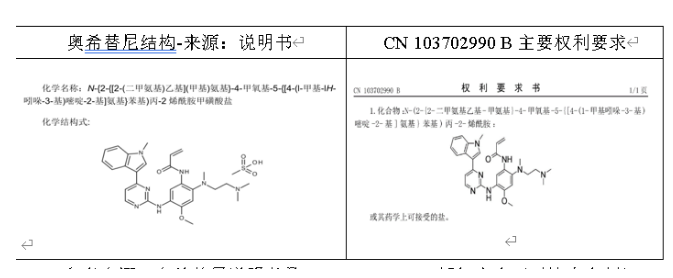
参考来源:奥希替尼说明书及CN 103702990 B授权文本(对比表自制)
第二项专利,CN 104109161 B,中国专利平台登记,类型是化合物。经查看奥希替尼说明书和该专利要求保护的范围,奥希替尼落入该专利的保护范围。
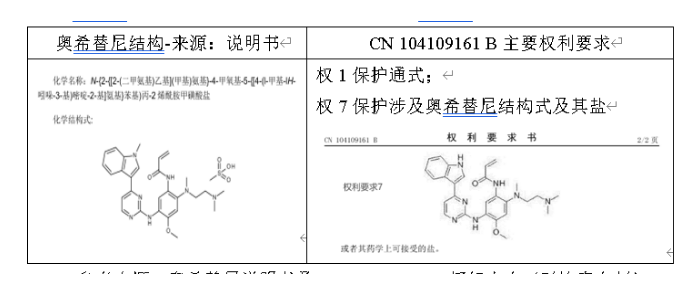
参考来源:奥希替尼说明书及CN 104109161 B授权文本(对比表自制)
第三项专利,CN104109151B,中国专利平台未登记,类型是涉及保护奥希替尼甲磺酸盐的多晶型。而且值得注意的是,本专利涉及保护奥希替尼结构式的多晶型A、多晶型B、多晶型C、多晶型D、多晶型E、多晶型F、多晶型K;本专利还涉及保护奥希替尼甲磺酸盐(即上市产品)的多晶型A、多晶型B;
经查看奥希替尼说明书和该专利要求保护的范围,该专利保护奥希替尼及其甲磺酸盐特定的多晶型,相关企业可以和自身的晶型进行对比,判断是否有规避/无效的空间,这部分需要结合研发技术信息进行沟通和判断。

参考来源:奥希替尼说明书及CN104109151B授权文本(对比表自制)
第四项专利,CN105175396B,中国专利平台未登记。但经仔细对比,奥希替尼结构式并未落入该专利的保护范围,但还需继续查看是否是制备中间体或者相关衍生物,如果仿制制备过程中出现该结构,亦有侵权风险。具体可见下图标注。
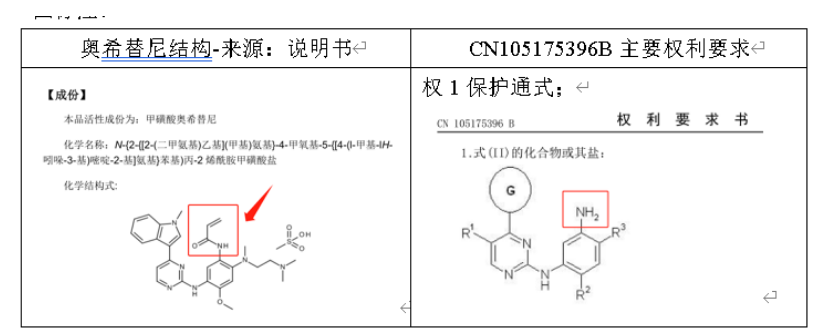
参考来源:奥希替尼说明书及CN105175396B授权文本(对比表自制)
第五项专利,CN105198862B,中国专利平台未登记。但经仔细对比,奥希替尼结构式并未落入该专利的保护范围,但还需继续查看是否是制备中间体或者相关衍生物,如果仿制制备过程中出现该结构,亦有侵权风险,具体可见下图标注。
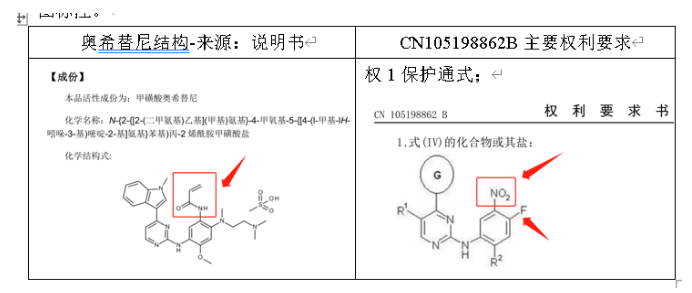
参考来源:奥希替尼说明书及CN105198862B授权文本(对比表自制)
经查看,上述这5项专利与奥希替尼上市产品的关系,也许并不是这5项专利均是其上市销售的障碍。最核心的还是专利登记平台上登记的2项专利。
基于本篇篇幅有限和受众考虑,同行可自行查看奥希替尼最核心的2项中国化合物专利的具体保护范围。首先,查看方向主要从专利本身稳定性,如专利审查过程、实验数据的呈现、创新性或新颖性、该专利能否满足现有审查标准;其次,从全球维度查看其化合物同族是否存在专利挑战以便获得启示、中国企业是否存在专利挑战等潜在可能,从这些维度收集信息进行思考和深入分析。
并且,本文预计讨论的第二个问题,在面临化合物专利非常长的情形下,仿制药申报策略的问题,对于已上市厂家,我们不得而知是否存在交易或其具体市场/专利策略。而留给其他仿制厂家的问题和主要探讨的方向,是针对此类产品,集中于研发初期的立项时机问题。这就需要主要从市场、竞品、该专利稳定性、化合物专利预计时长、剩余其他专利壁垒情况等角度进行分析讨论。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!





































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论